欢迎光临吉康旅!
※研究方案
诱导治疗阶段:( ),第一次60分钟,之后30分钟;贝伐单抗抗体7.5mg/kg,第一次90分钟,第二次60分钟,之后30分钟;培美曲塞/m 2 ,每次10分钟;卡铂 AUC5,每次 15-60 分钟,每 3 周一次,共 6 个疗程或疾病进展或其他原因。
输注顺序:阿特珠单抗→贝伐单抗→培美曲塞→卡铂。
维持治疗期:阿特珠单抗、贝伐单抗7.5mg/kg、培美曲塞/m 2 每三周一次,直至疾病进展或无法耐受的不良反应或其他原因。
输注顺序:阿特珠单抗→贝伐单抗→培美曲塞。
阿特珠单抗和贝伐单抗不允许减量,培美曲塞和卡铂允许减量。
※临床疗效
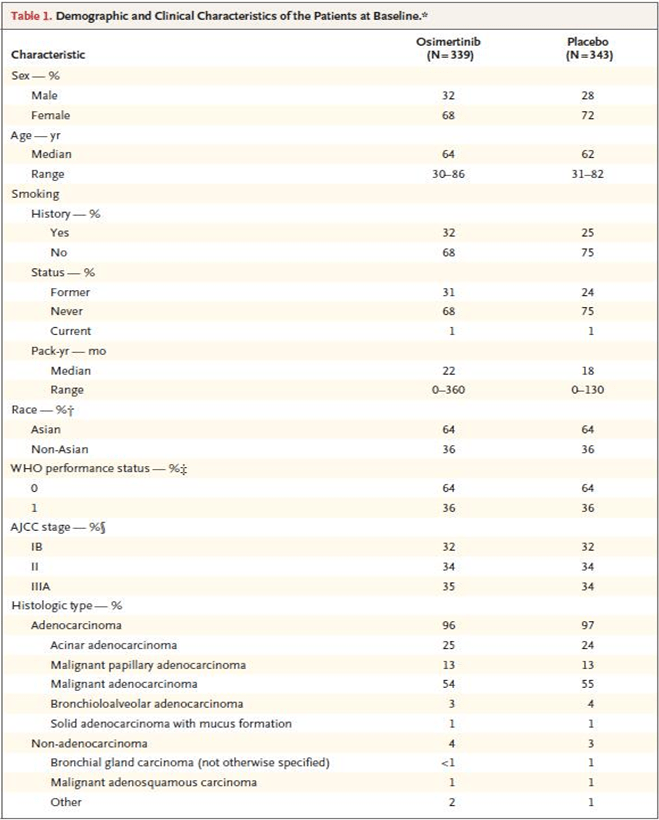
40 名患者被纳入研究,中位年龄为 62 岁,50% 为女性,85% 有吸烟史,ECOG PS 评分 0 分 17.5 %,1 分 62. 5%,2分20%,85%腺癌,22.5%脑转移(稳定),15%肝转移,42.5%,55%,55%,1例。
表达,21例(52.5%),9例(22.5%)1-49%,4例(10%)>50%,6例不详。
入组前EGFR-TKI使用史,吉非替尼47.5%,厄洛替尼60%,阿法替尼20%,奥希替尼57.5%,60%的患者使用过2个以上EGFR -TKI。
客观缓解率62.5%,疾病控制率100%,中位治疗起效时间5.0个月(范围2.8-8.0个月),中位无进展生存期 9.4 个月,中位缓解持续时间 5.2 个月,一年生存率 72.5%,中位总生存期尚未成熟。
在亚组分析中,奥希替尼耐药患者的中位无进展生存期比其他患者差(HR0.47, 95% CI:0.22–0.@ >95, p=0.04),Del 19 突变患者的中位无进展生存期弱于突变患者(HR 0.55, 95 % CI: 0.27 ——1.11,P=0.09)。未发现基线 PD-L1 表达和脑转移对中位无进展生存期有显着影响。
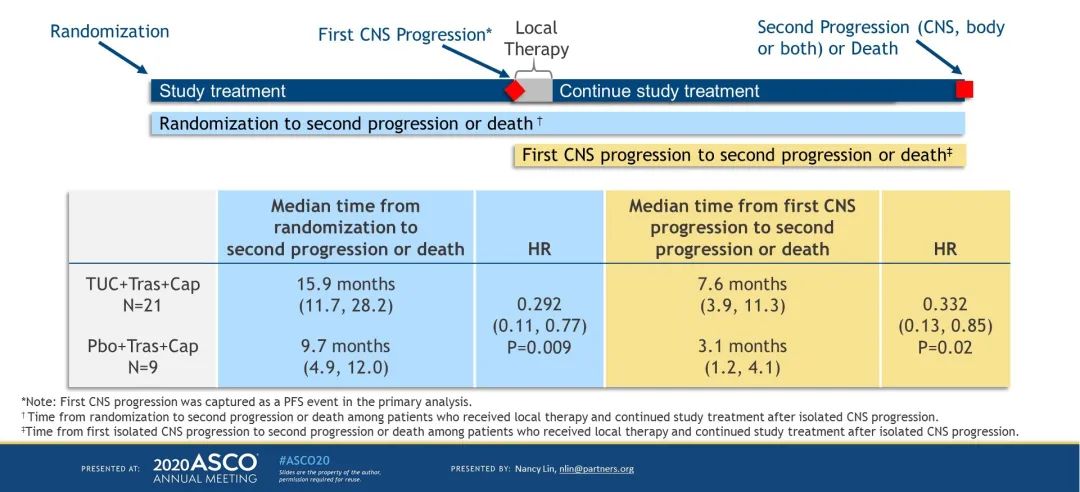
33 例疾病进展患者中,12 例(36.4%)发生脑转移,其中 7 例仅发生脑转移。基线脑转移与脑转移进展风险无显着相关性(HR 1.14, 95% CI 0.57–2.30, p=0.69)。
9例基线脑转移患者中,2例患者仍在临床组,1例患者在治疗7.4个月后因免疫性多发性神经病退出组,3例脑转移患者出现进展(治疗时间)。 6.4月,8.4月和10.3月),3例颅外病变进展(治疗时间为5.4月,12.1个月和1 5.8 个月)
※不良反应
15例患者(37.5%)发生3-4级不良反应,主要为发热(12.5%)、静脉血栓(5%)、晕厥(5%)、蛋白尿(2.5%)、血小板减少症 (2.@ >5%)、低钠血症 (2.5%)、蜂窝织炎 (2.5%)、气胸 (2. 5%)、免疫性肝炎 (2.5%) 和免疫性多发性神经病 (2.5%)。
一名 70 岁男性患者在疾病进展和停药三周后死于急性冠状动脉综合征。
因不良反应停药或减量7例,退组1例。
15例患者(37.5%)出现免疫相关不良反应,大部分为1-2级。
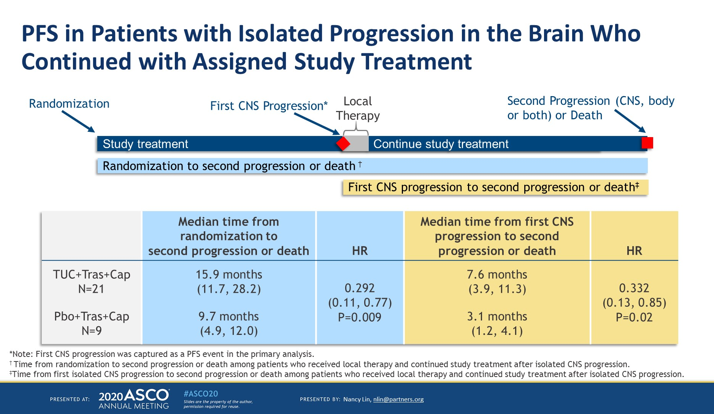
※进展后基因检测结果
截至 2020 年 10 月 20 日,34 名患者出现疾病进展。 3例患者行转移灶活检,1例发现小细胞肺癌转化。 24 名患者接受了二代测序,其中 22 名是血浆样本。结果如下表所示。
2.9@>
※进步再挑战EGFR-TKI
29例患者出组后接受全身治疗,中位治疗线程数为1,其中28例再次接受EGFR-TKI治疗(奥希替尼19例,阿法替尼8例,吉非替尼或厄洛替尼5例) )。
再次接受EGFR-TKI治疗的患者中,单药16例,联合贝伐单抗8例,联合西妥昔单抗6例,联合其他TKI 3例。 1例为联合化疗。中位无进展生存期为 5.8 个月,单药患者为 4.0 个月。大多数不良反应为 1-2 级,2 名患者发生 3 级皮炎和腹泻。返回搜狐,查看更多
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话