欢迎光临吉康旅!
EGFR突变是肺癌患者常见的突变类型。根据突变位点的不同,分为经典突变(或外显子21)或罕见突变。目前,对于经典突变,临床推荐使用第三代EGFR-TKI奥希替尼一线治疗。然而,作为靶向药物,奥希替尼将永远面临耐药的命运。奥希替尼耐药的治疗一直是临床研究的重点。今天小编就为大家报道首例肺腺癌脑转移患者。在对一线奥希替尼耐药后,通过2次化疗“复敏”,患者成功取得了奥希替尼的三战三胜。病例,截至今年4月,患者总生存期为40个月,
诊断:晚期肺腺癌伴脑转移+EGFR突变
患者,女,57岁,因刺激性咳嗽、胸痛于12月23日到医院就诊,无家族史。
实验室测试:
血常规、肝肾功能、电解质检查指标正常。血清癌胚抗原(CEA)水平为143.02 ng/mL(参考值
图像检查:
胸部计算机断层扫描 (CT) 扫描显示右上叶和中叶不规则高密度病变,纵隔多个肿大淋巴结,右胸胸腔积液。最大病灶的边界约为 37.2 mm × 17.8 mm,不清晰(图 1A)。此外,增强的头部 MRI 扫描显示大脑右顶叶有转移灶。
病理学检查:
胸水液体薄层细胞学证实了肺腺癌的诊断,胸水检测显示患者有EGFR突变。
最终诊断:
晚期肺腺癌,伴有多个淋巴结、胸膜和脑转移,临床 IVA 期和 EGFR 突变。
奥希替尼赢得三场战斗
完美实现40个月OS!

1. 奥希替尼一线治疗:
2018年1月,进行了奥希替尼(80mg)一线治疗。治疗期间,血清肿瘤标志物和CEA水平下降,CT扫描显示肿瘤病灶减少(图1C)。治疗5个月后,发现脑转移。消失(图 1D),肺部多处病变减少,表明奥希替尼的临床益处。
在奥希替尼治疗 11 个月后,2018 年 12 月,肺部 CT 扫描显示右侧胸膜出现多个新病变(以前从未发现),表明疾病进展(PD)(图 2B)。通过血浆分析,发现EGFR突变已经消失。奥希替尼停药。
2. 二线化疗复敏:
一线奥希替尼耐药后进行了三个疗程的培美曲塞+顺铂化疗。2019年3月影像学显示原发肿瘤稳定,但胸膜转移灶扩大并略有增大,再次用ARMS PCR法进行血浆检测,再次发现EGFR突变。
3.奥希替尼三线二次挑战
于是奥希替尼第二次用于三线治疗(再挑战)。治疗2个月后,胸膜癌灶几乎消失(图2D),说明培美曲塞+顺铂化疗复敏成功,肿瘤对奥希替尼复敏。但用了半年左右,2019年9月,胸膜转移瘤又开始扩大,病情又进展,但患者拒绝基因检测。
4. 四线化疗复敏:
因此,患者接受了 2 个周期的白蛋白结合型紫杉醇联合顺铂化疗(Q3W)。影像学显示原发肿瘤稳定,但右侧胸膜进展。
5.奥希替尼五线再挑战三度
2019 年 10 月 14 日,该患者在化疗进展后接受了第三次奥希替尼(80 mg,每天一次)的挑战。40天后常规胸部CT扫描显示胸膜病灶再次消失,原发灶稳定,脑转移灶未复发。截至2021年4月,患者的总生存期为40个月,生活质量良好。
治疗期间肿瘤标志物CEA的变化:

案例六点思考
1.奥希替尼耐药策略之一——穿插化疗
奥希替尼是目前EGFR突变肺癌患者的一线标准治疗药物。通过研究,一线使用奥希替尼可实现无进展生存期(PFS)和数月的总生存期。然而,作为靶向药物,奥希替尼的一大厄运就是耐药性。关于奥希替尼耐药的治疗,我们平台过去也推送过相关文章,有兴趣的患者可以再回顾一下。
解决奥希替尼耐药的主要机制之一是穿插化疗。之前的一项研究招募了 17 名接受奥希替尼再次挑战的患者,之前的治疗线中位数为 5。大多数患者在再次使用奥希替尼之前接受了化疗(14 名患者),4 名患者接受了免疫治疗。奥希替尼再次激发的 ORR 为 33%,DCR 为 73%。患者的中位 PFS 为 4.1 个月,中位 OS 为 9 个月。
目前,关于奥希替尼耐药机制的临床研究较多。很多对奥希替尼耐药的患者可以通过基因检测检测出靶点的突变,进而进行靶向治疗,获益更多。许多。如果奥希替尼基因检测耐药,没有可用的靶点药物,理论上应该积极转化疗。
2.化疗再敏化,TKI再挑战的机制
2019年,宋勇/吴一龙教授团队发表第一代TKI吉非替尼(易瑞沙)再挑战试验数据。一项前瞻性研究的结果首次证实,TKI 的使用可以在化疗后重新敏化。此外,一些临床研究指出,EGFR-TKI治疗晚期EGFR突变耐药的患者在穿插几个周期的化疗后,再重新开始EGFR-TKI治疗,效果更佳。从 EGFR-TKI 退出到重新激活的时间间隔称为 EGFR-TKI 的“退出期”。为什么在“停药期”可以通过化疗使肿瘤对EGFR-TKI重新敏感?临床实践中关于相关机制的讨论很多,其中比较被接受的说法是“
靶向治疗前,EGFR突变的癌细胞在整个肿瘤细胞群中的比例很高,所以在EGFR-TKI治疗后,EGFR突变的肿瘤细胞大部分被清除,剩下的癌细胞是少数耐药的。 EGFR-TKI。细胞,并逐渐成为优势群体,因此EGFR-TKI会产生耐药性。
化疗通过细胞毒性杀死肿瘤,而不是通过抑制EGFR通路,因此穿插化疗可以杀死许多对EGFR-TKI耐药的癌细胞,而对EGFR-TKI敏感的细胞可能会复活。用药后重新启动EGFR-TKI,构成EGFR-TKI耐药后化疗的“再敏化”机制。
3. 靶向耐药后哪些患者容易出现穿插化疗?
靶向再挑战可能是优势人群:两次靶向治疗间隔≥7个月;外显子 21 突变的女性;检测到两次低 EGFR 突变丰度;化疗药物培美曲塞。
本例患者被诊断为EGFR外显子21突变的肺癌患者,因此使用奥希替尼作为一线治疗。治疗11个月后首次PD时,分析中未发现EGFR突变,这间接反映了癌细胞中EGFR突变不再是优势组。因此,进行了化疗。化疗2个疗程后,血浆中再次出现EGFR外显子21突变,奥希替尼再次挑战成功。不幸的是,患者在第三次奥希替尼治疗期间拒绝了后续的基因检测,这使我们无法获得更多信息以更深入地了解这一现象,因此期待未来有更大样本量的进一步研究。中央前瞻性研究。
4.同EGFR经典突变,EGFR和突变不同
EGFR突变和突变都是EGFR的经典突变,但现在越来越多的临床研究对这两个亚型进行了分组和分析。2020年第十七次肺癌共识指出,对于EGFR突变阳性晚期,需细分EGFR敏感突变(外显子和外显子21)两种亚型以及是否伴有脑转移,给予不同的治疗分别:对于突变,优先推荐达克替尼、厄洛替尼+贝伐单抗和埃克替尼;对于外显子19突变,优先推荐奥希替尼和阿法替尼,一般推荐达克替尼。对于晚期EGFR突变,需要进一步细分不同的突变亚型进行精准个体化治疗。所以,
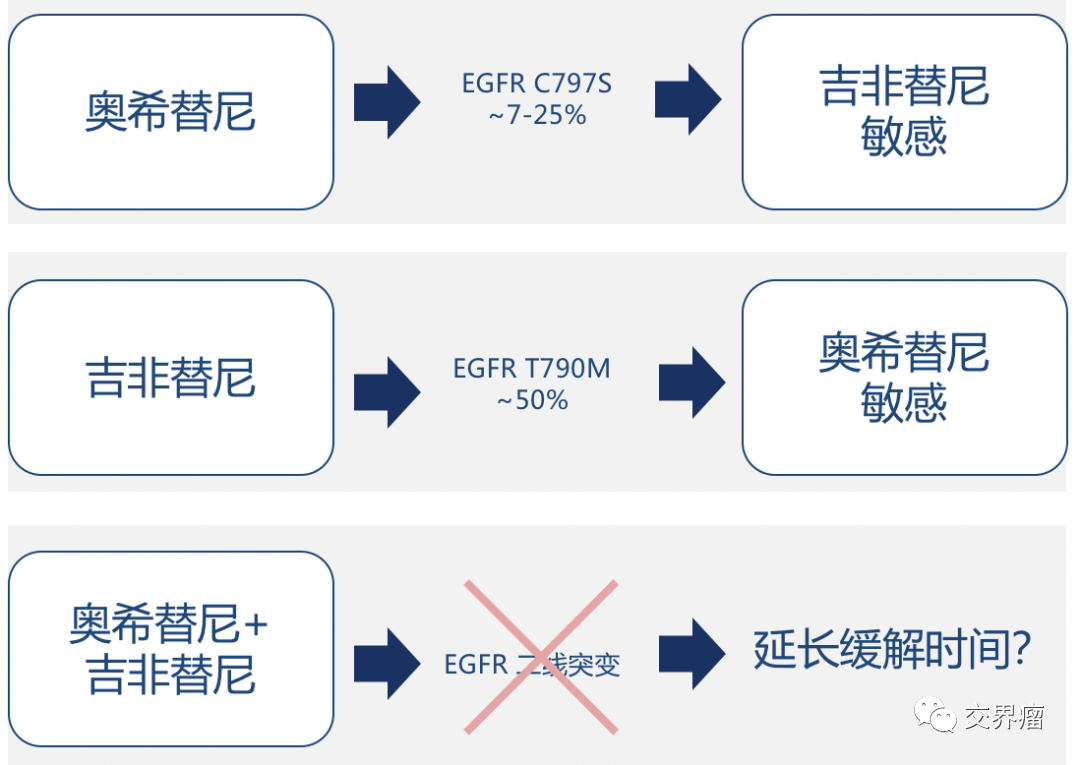
5. 靶向耐药通过化疗再敏化,靶向再挑战也适用于其他癌症!
来自先前在 JAMA 上发表的一项临床试验的数据,其中包括 28 名 RAS 和 BRAF 野生型晚期转移性结直肠癌 (mCRC) 患者,这些患者之前接受过伊立替康联合西妥昔单抗方案的一线治疗、奥沙利铂的二线治疗和贝伐单抗和爱必妥(500 mg/m2)联合伊立替康(180 mg/m2))治疗,每两周给药一次。
结果显示部分缓解6例,病情稳定9例,DCR达到54%,中位PFS3.4个月,中位OS9.8个月。本研究证实,在伊立替康和西妥昔单抗一线治疗后获得耐药的RAS和BRAF野生型mCRC患者,三线再应用西妥昔单抗和伊立替康可能有效,并得到医学关注。在世界范围内得到广泛认可。
6. 首次奥希替尼耐药后,该患者是否可以进行散布免疫?
有针对性的“再挑战”,顾名思义,就是对过去使用过的有效药物进行再利用。有很多方法,并且有很大的相似之处。TKI耐药后,先穿插其他治疗方案,待进展后再使用药物。在治疗中有效的相同 TKI。然而,现有的TKI“再挑战”穿插疗法大多是化疗。过去,我们也报道过EGFR靶向耐药的研究和病例,然后是穿插免疫治疗,然后是靶向再攻击。
但本例患者首次对奥希替尼耐药后,基因检测未发现EGFR突变。理论上可以穿插免疫治疗PD-1/PD-L1单克隆抗体。如果患者第一次穿插免疫治疗是否会影响后续的EGFR突变或再次使用奥希替尼尚不清楚。但相对免疫,穿插化疗,既便宜又安全。一般不推荐对EGFR突变进行PD1免疫治疗,不仅因为疗效有限、副作用严重,而且有增加超进展发生的可能性。因此,对于国内大多数无条件或不愿全力配合的患者来说,复敏化疗后的再挑战具有更广泛的适用性!
参考
的为
肺:一例
免责声明:本资料所含信息仅供参考,请听从您的医生或其他医疗保健专业人士的建议或指导。
本文版权归药典所有。任何个人或机构转载须经药典授权,在授权范围内使用,并注明出处为“药典”。
媒体合作请联系:
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话