欢迎光临吉康旅!
1、免疫+免疫——免疫检查点抑制剂+免疫检查点抑制剂协同抗肿瘤机制
PD-1抑制剂联合CTLA-4抑制剂有益于动物实验
CTLA-4+PD1:联合治疗复发性卵巢癌
96例复发性卵巢癌:缓解率:12.2%; + 缓解率:34.1%。
其他正在进行的免疫疗法 + 免疫疗法研究
2、免疫+瞄准
PD-L1+anti-VEGF:1、直接抑制T细胞功能;2、间接抑制T细胞功能;3、刺激免疫抑制调节性T细胞;4、抑制树树突细胞功能; 5、减少淋巴细胞与血管壁的粘附; 6、诱导异常的肿瘤血管。
PD-1/PD-L1+ anti-vEGF:(anti-PD-1):联合贝伐单抗治疗ROC的II期研究
11 名达到 PR 的患者中有 8 名 PD-L1 <1%。联合治疗可提高PD-L1低表达患者的治疗反应。
PD-1/PD-L1+TKI
联合铂类耐药卵巢癌的1b期数据
铂类耐药卵巢癌患者(20例),,q3w,qd
替雷利珠单抗联合多靶点酪氨酸激酶抑制剂的 ORR 为 23.5%,疾病控制率为 88.2%,中位无进展生存期 (PFS)达到18周,组合显示出良好的抗肿瘤活性。
PD-1/PD-L1+
临床前模型表明,PARP 抑制剂联合抗 PD-1 药物具有协同作用,无论 BRCA 突变/PD-L1 表达状态如何。
免疫激活:可导致细胞DNA损伤,如果修复过程是错误的路径,如非同源同源修复,或替代末端连接,DSBs可导致体细胞突变产生更多新抗原; DNA损伤可以通过途径激活先天免疫系统。
免疫抑制:PD-L1表达也可通过激活DSB检查点(ATM/ATR/CHK1))上调;PD-L1阴性肿瘤可通过激活ATM/CHK1松散检查点转化为PD-L1 ) 阳性,增加对 PD-L1 位点的敏感性。
1.+ vs
复发性晚期卵巢癌(32例):未接受或免疫治疗,对铂敏感,1次或多次含铂化疗; 4 周,+
在数据截止时,23 名患者有反应(未确认 0.9%;95% CI 53.3, 86.3)。共有 8 名 CR(25.@ >0%),其中 7 例发生在接受 1 或 2 线化疗的患者中,中位缓解时间为 2.7 个月(四分位距 {IOR1}1.0- 2.9 个月。

肿瘤细胞中PD-L1阳性表达(≥1%)的患者mPFS 13.6个月(95%CI8.2, 23.2) , PD-L1 阴性患者为 10.3 个月 (95% Cl0.9, 15.@>9).
主要终点是 12 周时的疾病控制率和安全性和耐受性,但遗憾的是没有达到。
2.+ 用于铂耐药复发性卵巢癌
其他正在进行的试验
3、免疫+化疗——化疗和免疫治疗有协同作用
+ 紫杉醇每周治疗,铂类耐药复发性卵巢癌 II 期
铂耐药(42例),q3w+紫杉醇80mg/m2 qw
结果:筛查55例,治疗42例,可评价37例,正在治疗10例,平均年龄63岁。
正在进行的临床试验
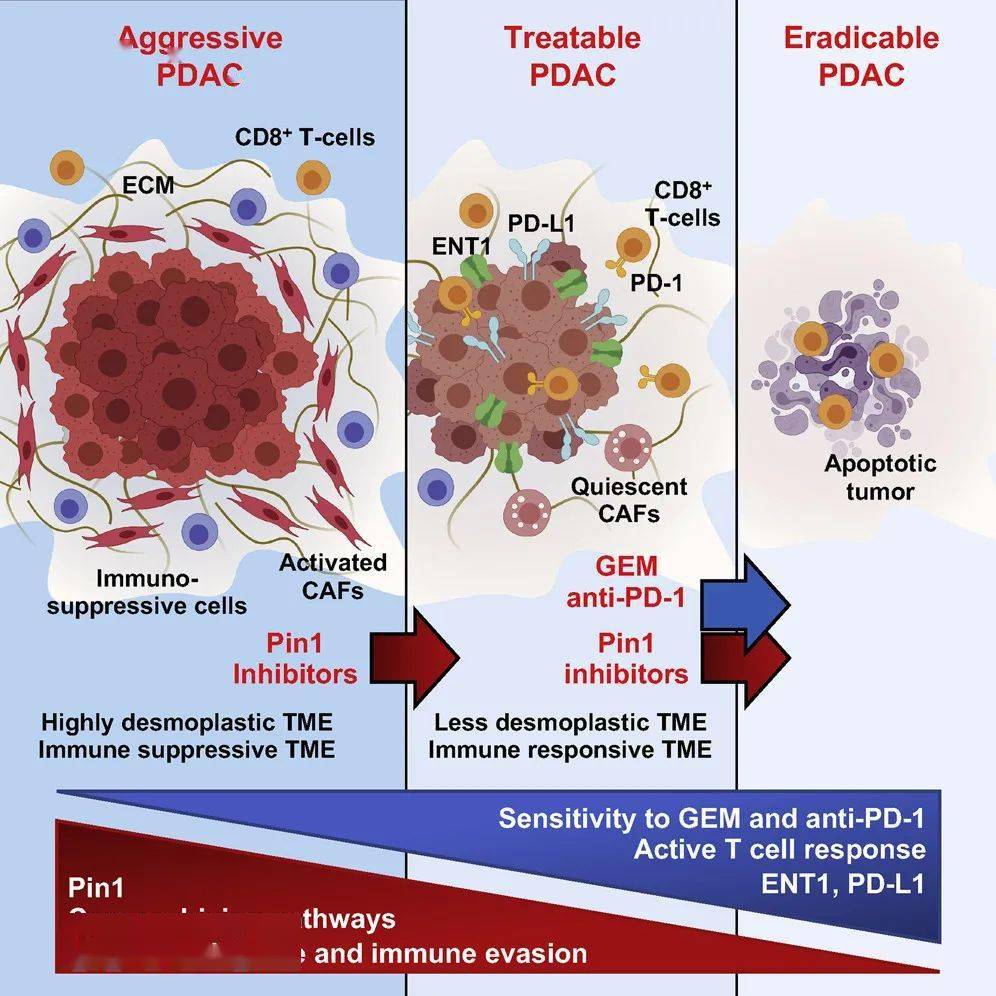
未来治疗方向:多药联合——+PD-1/PD-L1+anti-VEGF
探索性分析表明,三药联合组的ORR不依赖于基因组不稳定状态。
正在进行的多药联合——化疗+PD-1/PD-L1+抗VEGF
其他正在进行的临床试验
多药联合一线:化疗+PD-1/PD-L1+新治疗晚期卵巢癌
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话