欢迎光临吉康旅!
奥希替尼是第三种具有代表性的皮肤生长因子受体酪氨酸激酶抑制剂(EGFR-TKI),已被证明对早期EGFR-TKI耐药并患有非小细胞肺癌的患者具有显着的临床益处()已经变异了。我们研究的目的是确定奥希替尼/奥希替尼耐药的潜在机制,并将其与临床结果相关联。
方法:
我们回顾性分析了2017年3月1日至2018年12月31日期间因突变获得性耐药而接受奥希替尼/奥希替尼治疗的晚期患者。小细胞肺癌(SCLC)转化被纳入分子分析集。
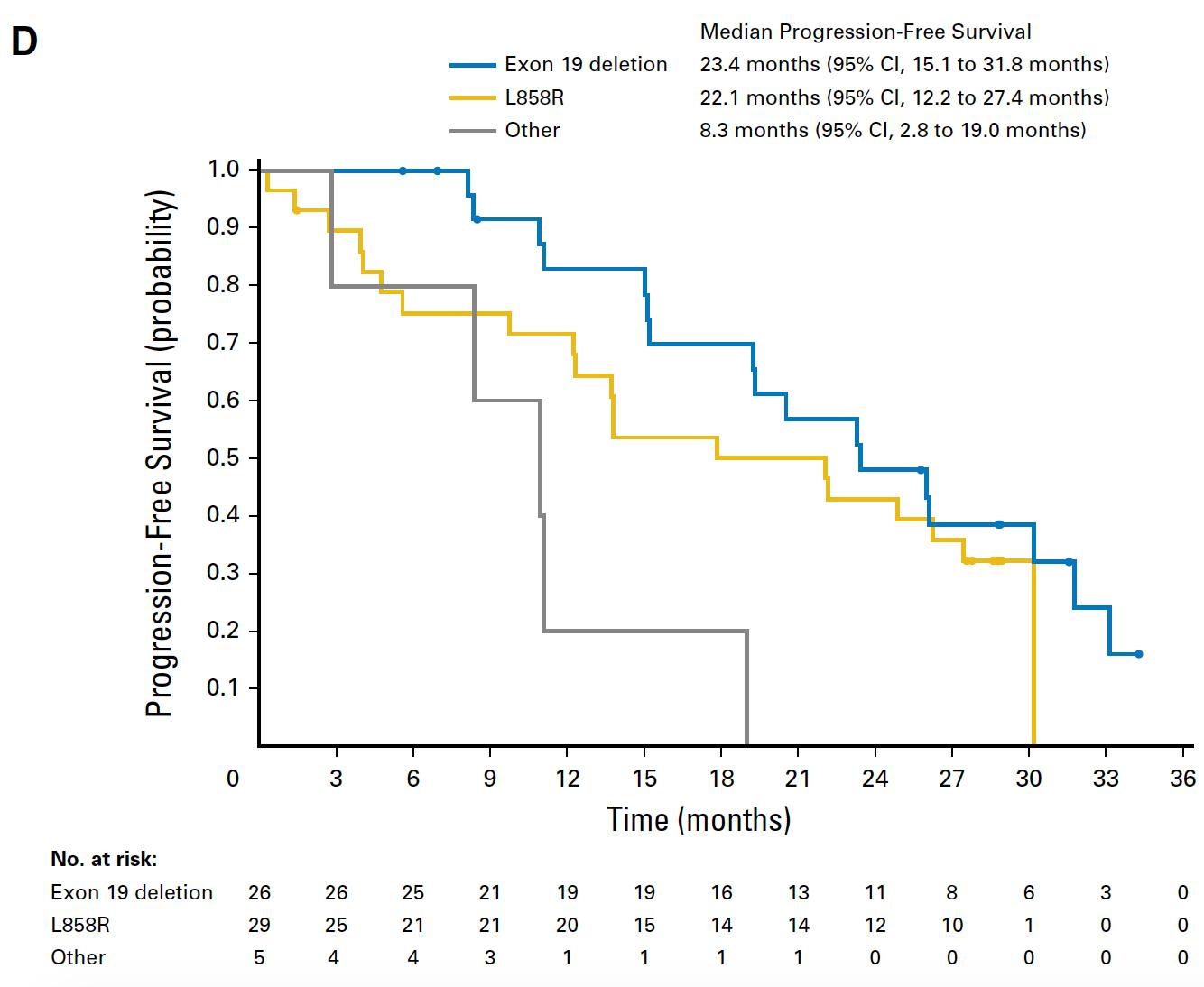
结果:
在通过分子分析进行密集评估的 49 名患者中,24 名患者保持突变,而 25 名患者显示缺失。49 例患者中有 27 例被鉴定出分子修饰,包括 EGFR 获得性突变(、、、、和)、非 EGFR 依赖突变(、ALK、BRAF、KRAS 和 EGFR 扩增,以及 MET 扩增。在数据截取时-off,保留组的中位无进展生存期(PFS)9.3 个月,损失组的中位无进展生存期(PFS)7.8 个月(P = 0.053). EGFR依赖耐药机制患者(13.5个月)的中位PFS显着长于替代途径激活患者(8. 2 个月;P = 0.012)。
综上所述:
该研究揭示了晚期患者奥希替尼/奥希替尼耐药的异质性机制及其与临床结果的关联。保持突变或具有 EGFR 依赖性耐药机制的患者具有更长的临床结果。
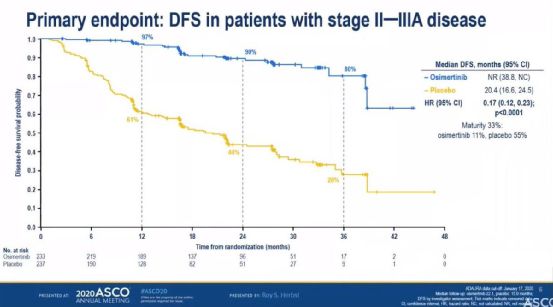
耐药性是靶向癌症治疗的主要挑战。多项研究报道了第三代EGFR-TKI奥希替尼耐药机制,包括突变、EGFR扩增、旁路激活、表型转化等。我们的数据补充了这些发现,提供了额外的中国数据集,各种分子修饰的关联,以及可能的耐药机制的临床结果。
27 名患者确定了基因组耐药性的假定机制。我们发现EGFR突变是我们研究中对奥希替尼/奥希替尼最常见的耐药机制,所有突变与突变同时发生。大约20-30%的奥希替尼获得性耐药病例中检测到这种突变,顺式执行有突变时,对多种EGFR-TKI耐药,包括吉非替尼和厄洛替尼、阿法替尼和奥希替尼。阿法替尼和西妥昔单抗的组合在对 EGFR-TKI 获得性耐药的患者中显示出有希望的临床活性和可控的安全性。无论突变状态如何,这都可以克服这种EGFR三重突变。EGFR依赖耐药机制的其他治疗策略尚缺乏研究,需要进一步研究。150 项研究中化疗、贝伐珠单抗和阿特珠单抗的组合对于 EGFR 突变和既往 EGFR-TKI 失败的患者是有希望的。EGFR非依赖性耐药机制主要是旁路激活,且大多与突变互斥,提示联合治疗的可能性。MET 扩增是一种常见的耐药机制,发生率为 10-30%。据报道,奥希替尼治疗在临床上取得进展后,EGFR-TKI与克唑替尼的组合可以有效对抗获得性MET扩增。RAS-MAPK通路的激活也有报道,如KRAS突变和BRAF突变。在对奥希替尼产生耐药性后,MEK 或 BRAF 抑制剂的组合可能会挽救这种机制。在我们的研究中,
-loss 和-是 PD 的两种基本模式。正如之前报道的那样,在我们的研究中,超过一半的患者观察到丢失,这主要与旁路激活的发展同时发生,可能与对奥希替尼的早期耐药有关。我们发现保留患者比丢失患者具有更好的奥希替尼临床结果,包括 PFS 和 TD。由于失踪患者更可能与旁路激活的发展有关,因此我们研究中旁路激活患者队列的结果与具有 EGFR 依赖性耐药机制的患者相似。旁路激活与奥希替尼治疗的临床结果之间的关联以前没有详细报道过。何勇等。分析了MET扩增与存活结果之间的相关性。
在分子分析组之外,4 名患者在奥希替尼/奥希替尼耐药后发生 SCLC 转换。据报道,从第一代EGFR-TKI进展到第三代,SCLC转化是3-14%患者获得性耐药的机制。确认小细胞肺癌转化后,推荐铂类依托泊苷方案。
我们的研究有几个局限性。首先,该研究仅限于单中心、回顾性设计和小样本量。其次,收集组织和血浆样本(以可获得者为准)的分子数据进行分子分析,这可能会影响分子修饰的结果。未来,需要基于组织的分析来充分了解奥希替尼耐药的潜在机制。
简而言之,失败后奥希替尼/奥希替尼的分子再分析对于指导个性化的后续治疗选择具有重要的临床效用。需要进一步研究新疗法或联合疗法以克服对奥希替尼的耐药性。扫描下方微信二维码了解更多:
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话