欢迎光临吉康旅!
其中,获国家药监局批准的肿瘤创新药有7个,国内首批3个,扩大新适应症4个。
3 国内首批
豪森药业第三代EGFR-TKI阿米替尼
甲磺酸阿美替尼片(商品名:®)是国内首个用于治疗局部晚期或转移性非小细胞肺癌()患者的第三代EGFR-TKI制剂。
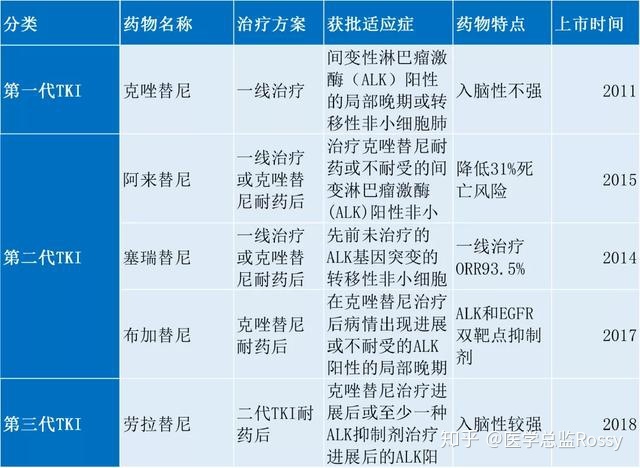
在我国的肺癌患者中,通常1-2年后,患者会对第一代靶向药物产生耐药性。如果肿瘤进展迅速,需要立即更换药物。目前EGFR-TKI已经发展到第三代,国内上市情况如下:
优势显着的第三代靶向药物备受关注。目前已有3家药企在部署第三代EGFR-TKI。详情如下:
据美国专利局称,阿斯利康奥希替尼的化合物专利将于2032年7月25日到期;豪森药业的奥美替尼和浙江埃森阿维替尼均拥有全球化合物专利,可用于奥希替尼在专利到期前抢占市场。
罗氏 PD-L1 mAb
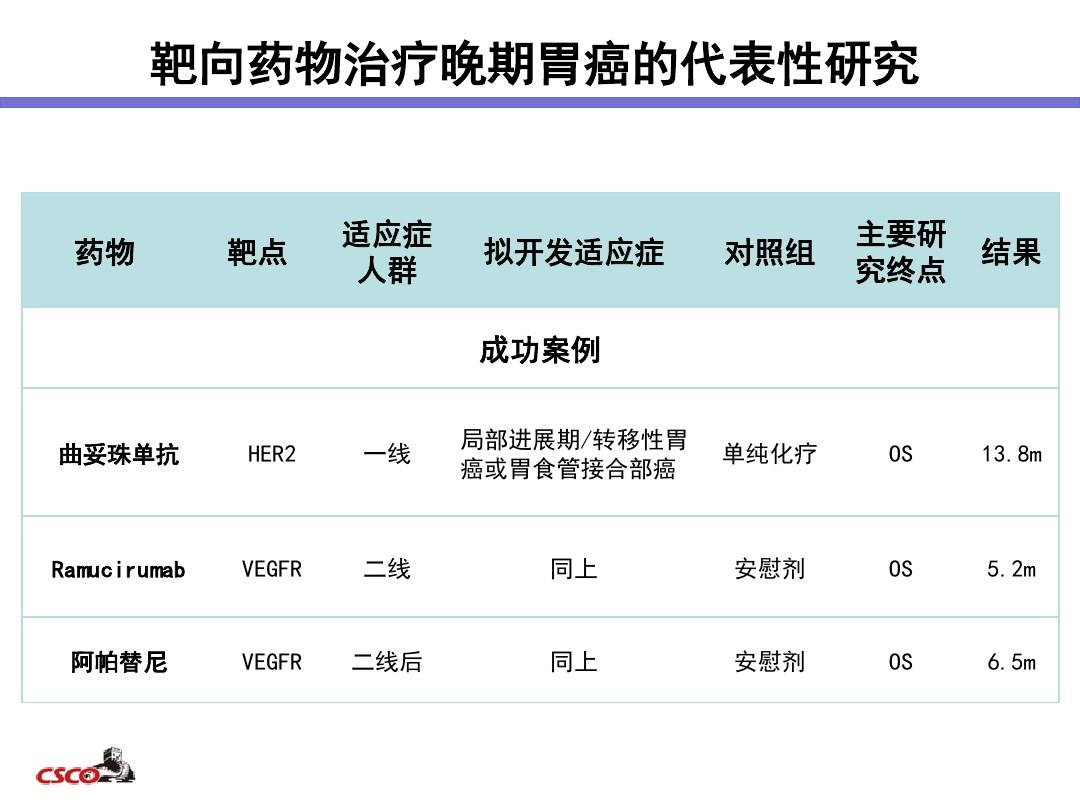
(商品名:太生奇®)是全球首个也是目前唯一在中国获批一线治疗广泛期小细胞肺癌的肿瘤免疫疗法。
目前,罗氏正在同步开展太生奇®的9项大规模全球III期临床试验,评估其在一些急需或无有效疗效的肿瘤领域的临床应用,如肝细胞癌、三阴性乳腺癌等领域.
日前,基于全球多中心III期临床试验结果,NMPA优先给予“T+A”(阿特珠单抗联合贝伐单抗)免疫联合疗法作为晚期不可切除肝细胞癌的一线治疗方案。有望成为全球首个获批治疗晚期不可切除肝细胞癌的一线免疫联合疗法!
罗氏的 ADC 药物恩美曲单抗(乳腺癌)
曲妥珠单抗(商品名:®),全球首个获批的实体瘤单药抗体-药物偶联物(ADC,-Drug),中国首个HER2靶向药物ADC产品。
在HER2阳性乳腺癌治疗领域,罗氏研发的药物建立了从初始新辅助治疗、术后辅助治疗、晚期一线治疗的抗HER2治疗体系。
曲妥珠单抗在中国获批后不久,乳腺癌领域又添新药:2月25日,美国FDA批准联合卡培他滨用于接受过两种或两种以上抗HER2方案的成人患者。晚期或转移性 HER2 阳性乳腺癌患者。
大部分业内人士认为,抗肿瘤药物适应症的数量决定了其在市场竞争中的地位,因此企业也在大力拓展获批的靶向药物和免疫治疗药物的新适应症。
此次获批新适应症的创新药有两个是PD-1药物。得益于新适应症的拓展,胃癌和肝癌也进入了免疫治疗时代。
4个新的扩展适应症
用于 BMS 的 PD-1 抑制剂纳武单抗(O 药物)
在中国获批的3个适应症:非小细胞肺癌、头颈部鳞状细胞癌、胃癌。
此外,美国 FDA 已批准 与 CTLA-4 抑制剂 联合用于治疗既往接受过索拉非尼治疗的肝细胞癌(HCC)患者。该小组的第一个也是唯一的双重免疫疗法。
恒瑞医药PD-1抑制剂
中国已批准两种适应症:霍奇金淋巴瘤和肝癌。
据药智数据查询,恒瑞的卡瑞利珠单抗临床试验目前处于III期临床试验阶段。期待更多适应症的批准。
诺华双靶点联合疗法达拉非尼/曲美替尼
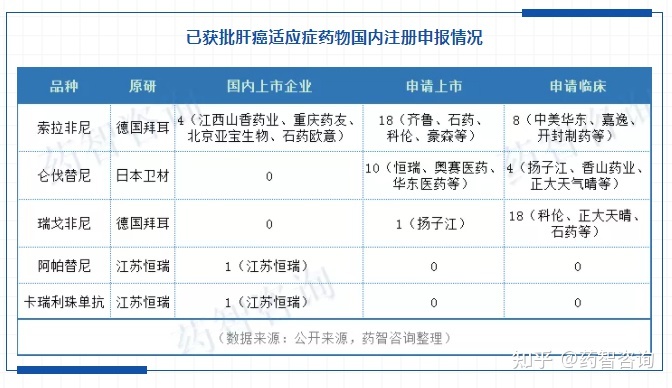
中国批准的2个适应症:
目前 FDA 批准的适应症是:BRAF 突变的黑色素瘤和甲状腺未分化癌。
默克西妥昔单抗
2个适应症在中国获批:
新获批适应症打破了中国复发或转移性头颈部鳞癌患者30年来铂类化疗疗效不佳的困境,填补了头颈部鳞状细胞癌靶向治疗领域的空白癌。
其他
“药王”修美乐进军眼科领域,2020年第一季度获得2个适应症,在中国共获批6个适应症。
近年来,国家各项利好政策的加快实施,为医药企业提供了良好的市场竞争环境。国内基因和细胞治疗企业也不断进行技术创新,陆续开启产业化进程。例如,新药研发领军企业恒瑞医药、肺癌领军企业贝达药业、专注car-t的复星医药等都迅速跟进。随着国内制药企业的发展,中国的肿瘤药物市场将蓬勃发展。
对于患者来说,一方面不用担心没有药吃。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话