欢迎光临吉康旅!
(奥希替尼)一线治疗EGFR突变晚期非小细胞肺癌,与目前标准靶向治疗相比,可延长疾病无进展生存期8.7个月(18.@ >9 个月与 10.2 个月)。
阿斯利康今日宣布,美国食品药品监督管理局(FDA)正式批准(中文商品名:,药品名称:)用于EGFR突变(表皮生长因子受体突变,包括外显子19缺失或外显子21)的一线治疗突变)转移性非小细胞肺癌患者()。突变测试需要 FDA 批准的测试套件。
该批准基于 III 期试验的结果,该试验在 2017 年欧洲医学肿瘤学大会 (ESMO) 上公布并发表在《新英格兰医学杂志》上。
阿斯利康肿瘤业务部执行副总裁戴夫说:“今天 FDA 批准()肺癌的一线治疗方案对患者和我们公司来说是一个激动人心的里程碑。在所有预先指定的患者亚组中,中位数的数据前所未有无进展生存期(包括有和没有中枢神经系统转移的患者)可以延长生命并更好地控制肿瘤的生长和转移。”
“奥希替尼一线方案的批准是治疗EGFR突变患者的一大进步,也是治疗规范的重大改变,”埃默里试验的首席研究员SS博士说亚特兰大大学癌症研究所。与 EGFR 抑制剂相比,奥希替尼显示出无进展生存期显着改善,并且没有意外的安全问题。”
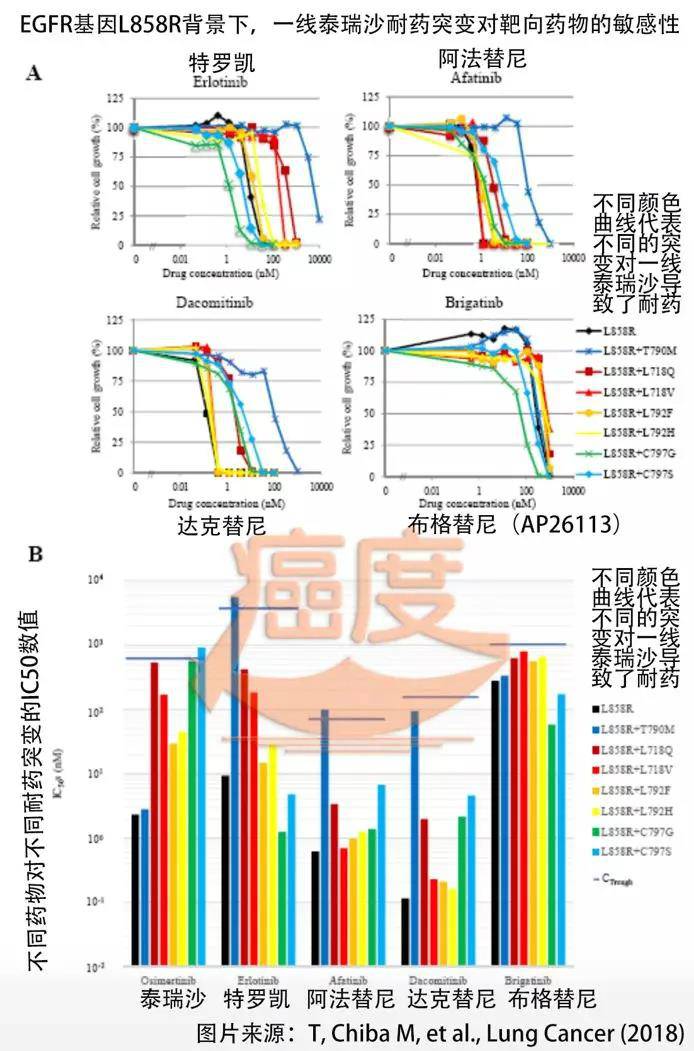
研究内容
在这项研究 () 中,将奥希替尼与当前一线护理标准 EGFR 酪氨酸激酶抑制剂 (EGFR-TKI)——厄洛替尼或吉非替尼——用于治疗新诊断的局部晚期或转移性 EGFR 突变 ()非小细胞肺癌。
奥希替尼达到了无进展生存期(PFS)的主要终点(见下表)。奥希替尼的 PFS 结果在所有预先指定的患者亚组中是一致的,包括那些有或没有中枢神经系统 (CNS) 转移的患者。在最终 PFS 分析时,总体生存数据不成熟。
试验研究者评估疗效结果
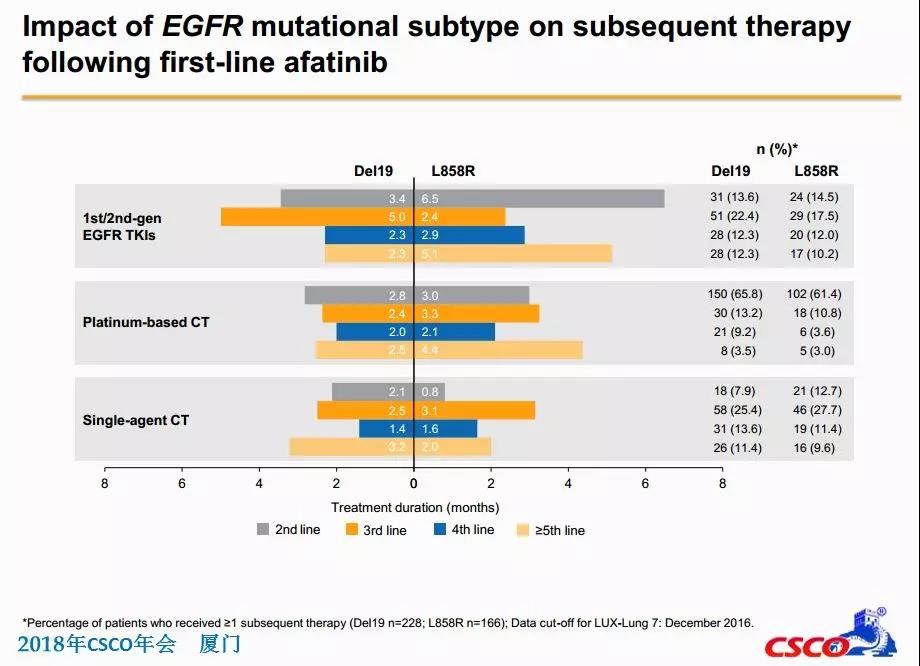
试验中奥希替尼的安全性数据与之前临床试验中观察到的数据一致。奥希替尼总体耐受性良好,34% 的服用奥希替尼的患者和 45% 的对照组患者发生 3 级或更高级别的不良事件 (AE)。接受奥希替尼治疗的患者最常见的不良反应(≥20%)是腹泻(58%)、皮疹(58%)、皮肤干燥(36%)、指甲毒性(35%)、口腔炎(29%)、疲劳( 21%)和食欲下降(20%)。
在美国和中国,特瑞沙(奥希替尼)已被批准用于一线 EGFR-TKI 治疗期间或之后疾病进展的 EGFR 突变转移性 患者的二线治疗,以及存在继发耐药突变的患者经测试证实。
2017年,特瑞莎(奥希替尼)一线方案获得美国FDA突破性治疗和优先审评资格。(奥希替尼)正在欧盟和日本进行监管审查,旨在申请一线治疗方案,并可能在2018年下半年获得最终上市批准。
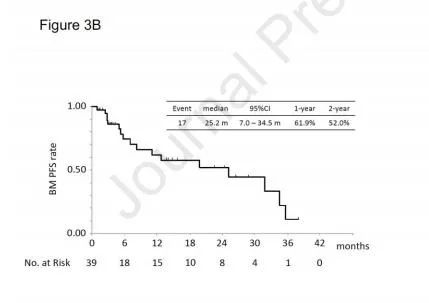
在巴西,根据数据,特瑞沙(奥希替尼)于 2018 年 4 月 16 日获批,用于一线治疗 EGFR 突变转移性非小细胞肺癌患者。
参考来源
1. 阿斯利康官网:美国FDA作为EGFR-非细胞肺一线治疗
2. 在 EGFR-非细胞肺中。N Engl J Med 2018;378:113-125
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话
塞来替尼塞来替尼联合那武利优治疗ALK重排非小细胞肺癌的效果如何?
2022-09-22克唑替尼(Crizotinib,Xalkori)是一款值得重点关注的好药、重点药。作为一款从开始研究到上市时间最短的“传奇药物”,克唑替尼在抑制M...
在EML4–ALK重排的非小细胞肺癌(NSCLC)模型中已经发现了致癌通路相关的PD-L1表达,因此在这类患者中使用PD-1抑制剂纳武利尤单抗(Nivo...
原发性肝癌为全球第6位常见肿瘤,居癌症相关死亡原因的第4位,其中肝细胞肝癌(HCC)约占75%~85%。我国是HCC高发国家,乙肝(HBV)相关...
接受达拉非尼联合曲美替尼治疗的不可切除或转移性BRAF V600突变肢端/皮肤黑色素瘤患者的总生存期:一项多中心、单臂IIa期试验的长期随...
据悉,肺动脉高压是一种慢性、危及生命的疾病,由于各种心肺疾病或系统性疾病引起肺动脉压力升高,进一步导致右心衰竭,该病的致死率、...








