欢迎光临吉康旅!
索拉非尼对肝癌患者不良反应严重程度及其与预后的关系(青岛大学医学院附属医院,山东青岛)的影响。方法回顾性分析索拉非尼治疗72例肝癌患者的药物不良反应及随访结果。索拉非尼不良反应的严重程度是根据是否需要减少剂量或短时间停药来判断的。分析了肿瘤进展时间 (TTP) 和总生存期 (OS),并使用 Cox 回归风险模型进行了多变量分析。结果本组72例患者中位OS为12。不同程度腹泻60例;轻中度不良反应59例,重度不良反应13例;与肝癌患者的 TTP OS 无关(P5))。结论 索拉非尼在肝癌患者中的严重不良反应少见,未发现不良反应严重程度与预后相关。关键词:肝肿瘤;肝癌 ; 索拉非尼;药物不良反应; 肝癌预后 doi: 10. 3969 issn. 1002-266X。2013. 43. 031 CLC 编号:R735。7; R979。文号:B 文章编号:1002-266X(2013)43-0080-02 基金项目:青岛市公共部门科技支撑计划项目(10-3-3-3-8-nsh)。与肝癌患者的 TTP OS 无关(P5))。结论 索拉非尼在肝癌患者中的严重不良反应少见,未发现不良反应严重程度与预后相关。关键词:肝肿瘤;肝癌 ; 索拉非尼;药物不良反应; 肝癌预后 doi: 10. 3969 issn. 1002-266X。2013. 43. 031 CLC 编号:R735。7; R979。文号:B 文章编号:1002-266X(2013)43-0080-02 基金项目:青岛市公共部门科技支撑计划项目(10-3-3-3-8-nsh)。肝癌预后 doi: 10. 3969 issn. 1002-266X。2013. 43. 031 CLC 编号:R735。7; R979。文号:B 文章编号:1002-266X(2013)43-0080-02 基金项目:青岛市公共部门科技支撑计划项目(10-3-3-3-8-nsh)。肝癌预后 doi: 10. 3969 issn. 1002-266X。2013. 43. 031 CLC 编号:R735。7; R979。文号:B 文章编号:1002-266X(2013)43-0080-02 基金项目:青岛市公共部门科技支撑计划项目(10-3-3-3-8-nsh)。
通讯作者:吴立群 手术是原发性肝癌患者长期生存唯一有效的治疗方法,但手术后高复发率影响肝癌患者的长期生存。索拉非尼是一种多靶点酪氨酸激酶抑制剂,是第一种也是唯一一种在肝细胞癌 (HCC) 患者中显示出生存优势的药物。本研究回顾性分析了青岛大学医学院附属医院近5年随访的72例肝癌患者的药物不良反应及随访结果,并评价其不良反应的严重程度。索拉非尼治疗肝癌。及其对预后的影响。临床数据 2008 年 8 月,青岛大学医学院附属医院收治72例HCC患者,其中男性65例,年龄31~74岁。纳入标准:连续使用索拉非尼3个月以上;ECOG体能状态评分为0;肝功能-Pugh 类;通过影像学或组织学检查证实为 HCC。排除标准:心、脑、肾严重器质性疾病患者;服用索拉非尼少于3个月或因严重不良反应停止治疗的患者。72例患者中,70例有乙肝病毒感染背景,血清肝炎病毒学检测阴性,丙肝病毒抗体阳性。肝功能 - Pugh 分类,例如。肝外转移42例,血管瘤栓19例;
TNM分期,分期30例,分期42例。28 例 ECOG 体力状态评分为 0。服用索拉非尼前未接受任何治疗的患者2例,接受手术治疗的患者33例(HCC切除加肝移植的患者24例),接受消融治疗和经导管动脉化疗栓塞(TACE)单次治疗的患者34例未接受其他治疗,直接服用索拉非尼,2例接受手术治疗的患者在肝移植前和肝移植后10例(肝移植后2例,肝切除术后4个月)开始服用索拉非尼。. 索拉非尼服用方法:d.出现3级及以上不良反应时减半服用或暂停服用,不良反应减轻后恢复原剂量。索拉非尼不良反应分级根据常见的腹泻、皮疹和高血压症状分为轻中度组(虽然有反应,但仍可服用常用剂量)和重度组(需减量或间断停药)缓解症状)。随访方法 所有患者每4周随访一次,包括肝肾功能检查、AFP检查和影像学检查。根据mR标准计算生存时间(OS)和肿瘤进展时间(TTP)。随访截止时间为2013年3月31日或患者死亡时,随访3年。
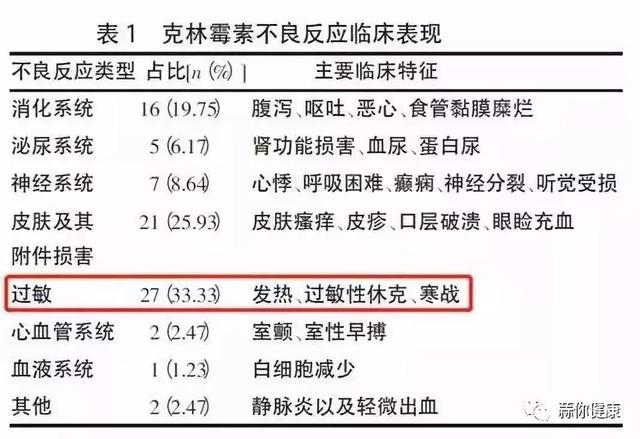
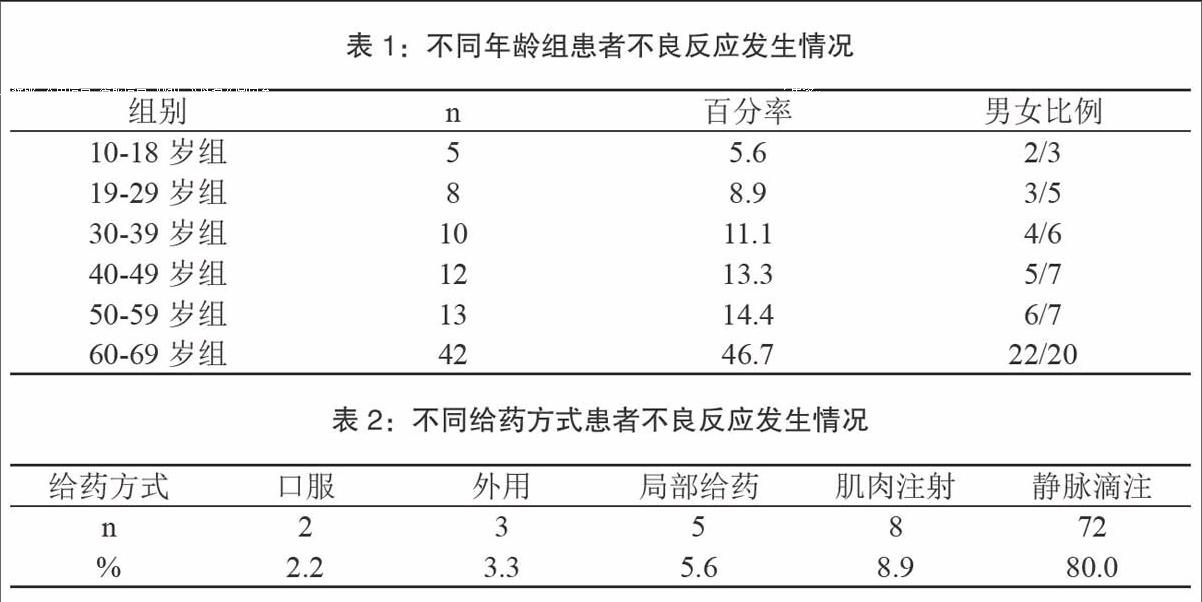
P0。05 表示差异具有统计学意义。生存结果 本组72例患者中位OS为12。索拉非尼不良反应发生率 本组72例患者中,61例(84. 7%)患者在服用索拉非尼后出现皮肤毒性,7例需减量药物剂量;60例患者(83. 3%)出现不同程度的不良反应。腹泻,其中 5.9% 的患者需要减少药物剂量)发展为高血压,且未发生剂量减少;3例因肝功能不全停药,1例在服药1个月时因门脉胃病出血停药半个月。本组发生轻中度不良反应59例(其中无不良反应2例,均为肝移植患者)、严重不良反应 13 索拉非尼不良反应严重程度与ECOG评分的关系。59例患者中,ECOG评分23例,严重不良反应13例。ECOG 评分 2 索拉非尼不良反应严重程度与肝癌患者预后的关系 轻度至中度不良反应 59 例,重度不良反应 13 例 中位 OS 为 13. 个月,中位 TTP 为 7。讨论 HCC 对传统的细胞毒性化疗药物不敏感。研究证实,索拉非尼可有效抑制人肝癌细胞中Raf激酶的表达,从而抑制细胞的生长。索拉非尼通过靶向多种途径抑制索拉非尼的发展,包括 Raf-1 B-Raf 激酶、血管内皮生长因子受体-2-3) 和血小板衍生生长因子受体β (-β) 酪氨酸激酶。它是第一种通过破坏肿瘤细胞增殖和血管生成来显着延长晚期 HCC 患者 OS 的药物。
TACE 通过中断肿瘤的血液供应导致缺氧性坏死,但组织缺氧也会刺激血管生成生长因子的释放,例如 VEGF 水平升高 [8,9]。理论上,TACE联合索拉非尼治疗HCC是相辅相成的,应该有显着的疗效。大多数患者服用索拉非尼后的主要不良反应是腹泻、恶心、乏力、高血压和皮肤毒性。皮肤毒性包括脱发、口腔内膜炎、红斑和手足皮肤反应 (HFSR)。HFSR 的严重程度取决于索拉非尼给药的时间、剂量和药物参与程度。HFSR 不是对药物的过敏反应,索拉非尼单独或与 VEGF 受体、血小板衍生生长因子受体、c-KIT 激酶和 Fms 样酪氨酸激酶 3 [10]。多数患者服用索拉非尼后出现轻至中度腹泻,其机制尚不明确,可能与胰腺外分泌功能下降有关[11],部分研究[12]认为2个HCC患者的OS较好。[10] 等人发现,无皮肤毒性患者的中位 TTP 月数明显长于有皮肤毒性的患者,因此索拉非尼治疗的 HCC 患者的早期皮肤毒性被认为具有潜在的疗效。标识。本研究未发现降低索拉非尼剂量与预后相关,也未发现HFSR和腹泻的严重程度与服用索拉非尼的患者预后相关,可能与肿瘤负荷程度和治疗方式有关该组中的 HCC 患者(例如,9)。肝移植患者免疫抑制剂的应用与移植肝内无肿瘤有关。
服用索拉非尼的HCC患者不良反应严重程度与预后的关系需要多中心大样本研究。参考文献: 原发性肝细胞癌肝切除术后短期复发的危险因素[J].中华外科杂志,2011,49(9):784-788. [2] JM, S, V, et al . - [J]. Med, 2008, 359 (4): 378- 390. [3] AL, Kang YK, Chen Z, et al. sor-Asia--: a,-,-bo- [ J]., 2009, 10 (1): 25-34. 索拉口服非尼布联合放疗治疗肝癌疗效观察[J]. 山东医药, 2011, 51(50)) @>: 44-45. [5] EA, P, J, et al. New eval-: R (, 2009, 45 (2): 228-247. [6] A, C, R, et al. che- (TACE) in (HCC): 角色 [J]. Am, 2008, 103 (4): 914-921. [7] AL, Guan ZZ, Chen AD, et al. sor- ar:亚洲-[J]. Eur原发性肝癌TACE前后血清HIF-1α、VEGF和CT灌注成像。相关性分析[J].中华医学杂志, 2013, 93 (19): 1472-1475. [9] 林萍萍, 刘艳丽, 高东奇, 等. 索拉非尼对人肝癌细胞凋亡及其对Raf激酶表达的影响[J]. 山东医药, 2011, 51(46): 64-65. [10] B, D, A, et al. skin oma pa-[J]., 2010, 15(1): 85-92. [11] R, D, C, et al. ar [J]. , 2013, 84 (1) : 6-13.[12] Mir O, R, -RP , et al. - - [J]. 安, 2012, 23 (1): 280-281. (收稿日期: 2013-08-29)山东医药2013, Vol. 53, No. 43 1472-1475。[9] 林萍萍,刘艳丽,高东奇,等.索拉非尼对人肝癌细胞凋亡及其对Raf激酶表达的影响[J]. 山东医药, 2011, 51 (46): 64-65. [10] B, D, A, et al. skin oma pa-[J]., 2010, 15 (1): 85-92. [11] R, D, C, et al. ar [J]. , 2013, 84 (1) : 6-13.[12] Mir O, R, -RP, et al. - - [J]. 安, 2012, 23 (1): 280-281. (收稿日期: 2013-08-29)山东医药2013, Vol. 53, No. 43) 1472-1475。[9] 林萍萍,刘艳丽,高东奇,等.索拉非尼对人肝癌细胞凋亡及其对Raf激酶表达的影响[J]. 山东医药, 2011, 51 (46): 64-65. [10] B, D, A, et al. skin oma pa-[J]., 2010, 15 (1): 85-92. [11] R, D, C, et al. ar [J]. , 2013, 84 (1) : 6-13.[12] Mir O, R, -RP, et al. - - [J]. 安, 2012, 23 (1): 280-281. (收稿日期: 2013-08-29)山东医药2013, Vol. 53, No. 43) @1) : 6-13.[12] Mir O, R, -RP, et al. ——[J].安, 2012, 23 (1): 280-281. (收稿日期: 2013-08-29) 山东医药2013, Vol. 53, No. 43) @1) : 6-13.[12] Mir O, R, -RP, et al. ——[J].安, 2012, 23 (1): 280-281. (收稿日期: 2013-08-29) 山东医药2013, Vol. 53, No. 43)
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话