欢迎光临吉康旅!
2018年心血管系统接受最多的药物为仿制药,接受数为89个,较2017年的30个增加196.67%。本文还将重点分析仿制药的接受情况。今年心脑血管药:新三类下首批申报的国防品种有哪些即将上市?在新4类申报的仿制药品种中,哪些是首批上市的不同剂型的仿制品?哪些会在上市后直接通过一致性评价,占据市场优势?看一看。
2018年仿制药爆发,受理数同比增长196.67%
从图1可以看出,近10年心血管系统药物总体接受趋势在2013年达到申请高峰,为966件(按接受数,下同),2016年急剧下降。 2017、2018年小幅回升。从药品申报曲线类型来看(仅仿制药、进口、新药申报、进口再注册、补充申请、审评等)暂时考虑),2016年之前,心血管系统药物大部分为新药和仿制药申报;2016年后 2018年新药申请量大幅下降。2018年新药申请只有1个,在经历了2016年仿制药下滑后,2018年反弹至89个,比2017年增长196.67%。
值得一提的是,在进口的12个受理号中,有1个受理号是申报为化学药品5.的波生坦分散片,这是第一个获得FDA批准的药品。3 岁及以上患有特发性或先天性肺动脉高压 (PAH) 的儿科患者的药物治疗。目前已被认定为特优品种,审评速度加快,上市迫在眉睫。
4首仿制,恒瑞1品种引领市场
89个仿制药受理号均为报告制作,新3类申请下的仿制药受理号为11个,为在境外上市但在国内未上市的仿制药,包括替米沙坦片、氨氯地平片等。、瑞格森注射液、酒石酸美托洛尔片、布洛芬注射液、氨氯地平阿托伐他汀钙片、安立生坦、阿齐沙坦片7个品种。截至目前,其中5个尚未在中国上市(详情如图2).
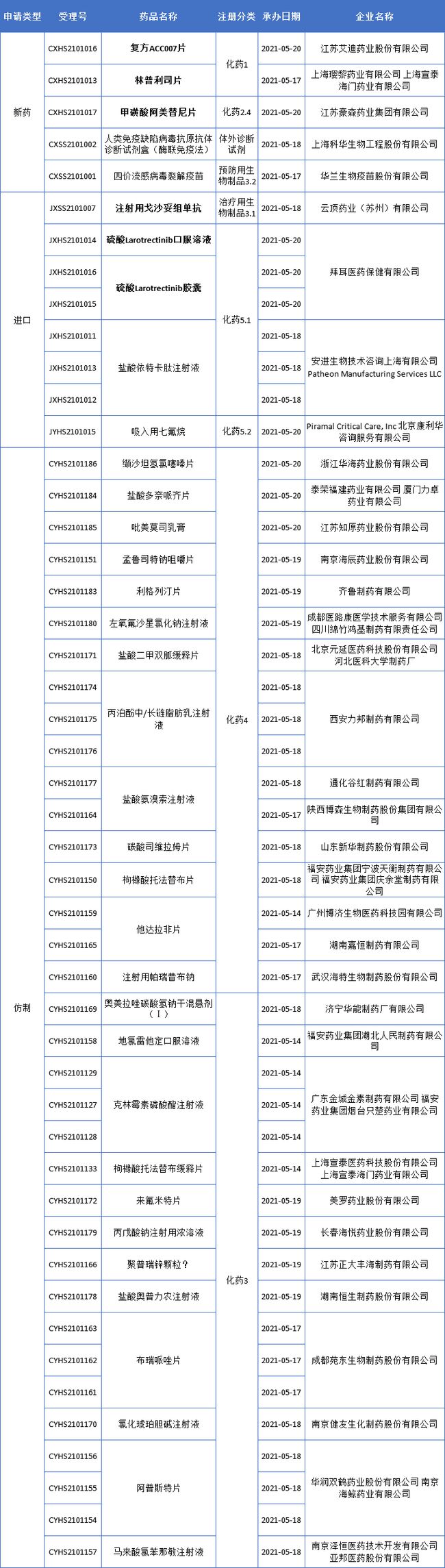
5个品种中,阿齐沙坦片和瑞加松注射液均未在我国原研进口。其中,阿齐沙坦片是国内企业申报的热门品种,共有109个受理号,其中105个为新药。3.1 类临床申请,104 项临床批准。今年的2个受理号是北京生物医药申报的第三类化学药品,尚未开始审评。不过,同样申报生产第三类化学药品的恒瑞医药在2017年被受理并纳入优先审评。目前已经启动审核,暂时提前,上线在即。
其他3个品种均为国内原研进口,但从进口品种的市场表现来看,替米沙坦、氨氯地平片和安立生坦在国内均无中标信息。氨氯地平阿托伐他汀钙片 进口品种氨氯地平表现良好。目前,该药已在31个地区中标,近几年中标地区数不俗。今年氨氯地平5mg:阿托伐他汀10mg*7是10个产品在各地区中标,平均中标价为59.21元。今年该品种有2个受理号,均由北京嘉林药业申报。但是,除了第 3 类下的 1 份申请外,还有第 4 类下的 1 份申请。目前,
4种不同剂型首次仿制报产,市场前景看好
新增4类共申报77个受理号,其中26个品种(北京嘉林药业申报的4类受理号1个除外),10个受理号是国内上市品种不同剂型的首仿。包括非诺贝特片(Ⅲ)、琥珀酸美托洛尔缓释片、缬沙坦氨氯地平片(Ⅰ)和沙库巴曲缬沙坦钠片四个品种。公司已获准上市,但均为进口,其中2家已纳入医保B类(详情见图3).
4个琥珀酸美托洛尔缓释片的受理号均由南通联亚药业申报为4类,其他年份14个申报为6类,均获批临床使用。该药由阿斯利康进口。在中国,只有阿斯利康在32个地区中标。获奖地区47.5mg*7规格较多。2018年在12个地区中标。中标的平均价格为 15.41。而且该药已纳入国家乙类医保,市场前景看好。
此外,康贝申报非诺贝特片(Ⅲ)受理号1个,其他年份仿制药申报受理号2个,分别由贝塞罗药业和康贝申报6个类别,并获临床批准。非诺贝特片(Ⅲ)仅从雅培进口并上市。目前,23个地区有中标信息。0.16g*10规格今年在4个地区中标,均价38.57元。不过,该品种已于2017年被纳入国家医保B类,预计在很长一段时间内会增加销量。
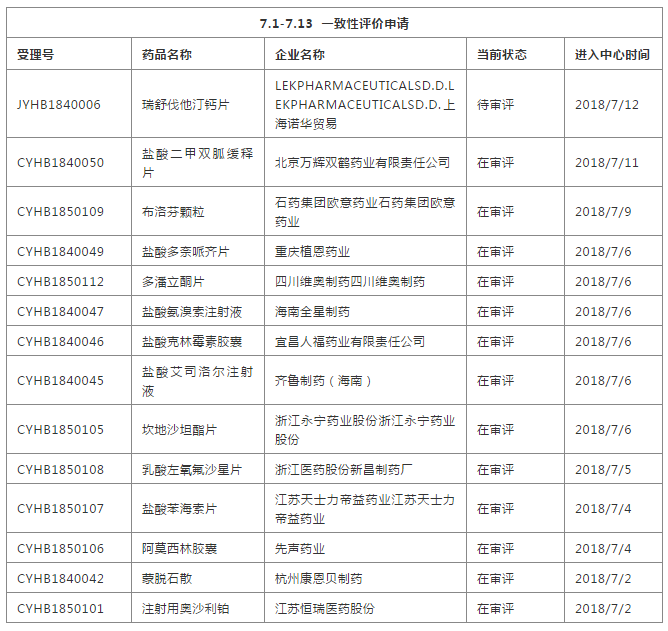
另外两个在各地中标较多的进口品种是缬沙坦和氨氯地平片(Ⅰ)。今年,该品种的两个受理号分别是北京生物制药和江苏恒瑞药业。最新状态为已完成审评,恒瑞领先,于2018年11月7日完成。其他年份共上报6大类35个仿制药,其中1个申报临床并获得批准;报告生产34个;15个被批准用于临床。缬沙坦氨氯地平片(Ⅰ)仅由诺华公司进口,已在24个地区中标。中标地区数量呈上升趋势。2018年缬沙坦80mg:氨氯地平5mg*7在10个地区中标,中标。均价52.08元。
8款与原研药效相同的仿制药即将上市,匹伐他汀钙片、硝苯地平缓释片或成为首发
其余67个仿制药受理号中,有22个品种,均已在中国境内一家或多家企业获批生产。其中,8个具有相关受理号的品种上市申请被纳入优先审评审批(详见4),纳入原因有二:1、自愿撤回,变更为标准与原研药质量和疗效一致,改进后重新申报仿制药注册; 2.同一生产线生产,已在美国上市,该类药上市后,视为通过一致性评价。
第一种情况包括3个品种(图5红色品种):北京万生药业申报的阿托伐他汀钙片,共2个受理号;合肥英泰药片申报的瑞舒伐他汀钙,共1个受理号;南京长奥药业匹伐他汀钙片的申请,共1个受理号。
其中,阿托伐他汀钙片已通过浙江新东港药业有限公司和北京嘉林药业有限公司的审评,北京万生药业成功上市后,可能成为第三家审评公司。瑞舒伐他汀钙片已经过4家企业复审,常州制药厂也出具了复审。因此,即使合肥瀛泰上市,也将面临激烈的竞争。匹伐他汀钙片尚未经过任何公司的审查。华润双和药业、江苏万邦生化医药集团也在开展BE试验,尚未启动申报。如果南京长奥药业成功上市,很有可能成为第一家上市公司。企业。
第二种情况,共纳入5个品种(图5中未标红的品种):华海药业申报的奥美沙坦酯和替米沙坦片,各有3个受理号;海正辉瑞宣布厄瓜多尔贝沙坦和氢氯噻嗪片有2个接受号;南通联亚药业申报的硝苯地平缓释片受理号3个;广东阳光药业第1号苯磺酸氨氯地平片受理号。此外,常州制药厂申报的瑞舒伐他汀钙片也属于此类情况。共有4个接受号,目前显示。对这个品种的高估上面已经提到过,这里不再赘述。.

目前,奥美沙坦酯和替米沙坦片均未通过一致性评价。目前只有一家公司获批生产奥美沙坦酯和替米沙坦片,一致性评价尚未启动。国内有39家厂家,但目前只有上海信义天平药业和浙江金利源药业在进行BE试验,进展缓慢。因此,华海药业最有可能成为第一家通过两个品种评审的企业。
厄贝沙坦和氢氯噻嗪片通过了华海药业和正大天晴的一致性评价,而浙江爱诺药业只进行了BE,海正辉瑞可能成为第三家通过评价的公司,形成三管齐下的对抗。没有企业通过硝苯地平缓释片的一致性评价,国内也没有经批准的企业开展一致性评价备案。南通联亚药业很有希望成为第一家通过评审的企业。苯磺酸氨氯地平片 扬子江药业集团、浙江晶鑫药业等5家企业已通过审核,多家企业也被受理,所以广东东光药业是否会成为第六家审评公司还有待观察。不确定性大,竞争激烈。
除优先审评品种外,其余23个受理号的14个品种中,只有1家企业通过了安立生坦片的一致性评价,其他企业均未通过一致性评价。快,先把清单弄明白。
仿制药
药智网
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话