欢迎光临吉康旅!
第二届“35·35”CSCO-梁以辉2018杰出青年肿瘤医师大赛”注册筛选阶段正式结束!在众多参与注册筛选的医生中,100位优秀青年医生脱颖而出!他们将在近期将举行三轮PK,展现年轻医生风采!第一轮为最新ASCO摘要解读,考生可自由选择口头报告,对主办方指定的口头报告题目进行点评(如:背景、结果评价、临床评价 100位年轻医生在规定时间内提交了解读,解读非常精彩,现展示给大家阅读!欢迎转发,让更多医生看到青春的力量!欢迎评论,发表意见,与年轻医生同台讨论!
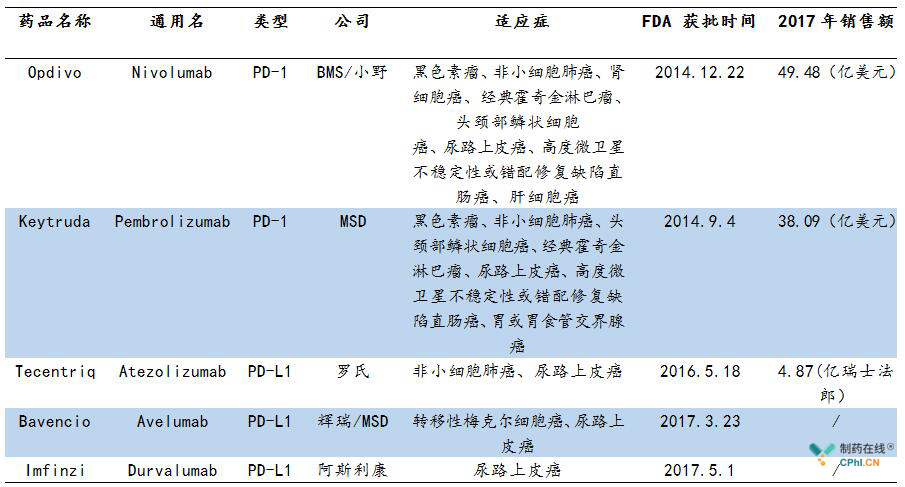
3504:一项关于伊立替康和西妥昔单抗 (IC) 与伊立替康、西妥昔单抗和雷莫芦单抗 (ICR) 作为晚期结直肠癌 (mCRC) 的二线治疗的随机试验(在探索二线治疗失败后的 - 和 -基于一线治疗):结果。
背景:尽管抗 VEGF(R) 和 EGFR 抗体在 RAS 野生型 mCRC 中均具有活性,但两者的联合治疗对未经选择的 mCRC 患者无益。我们进行了这项研究,以确定添加抗雷莫芦单抗是否可以改善伊立替康和西妥昔单抗作为 KRAS 野生型 CRC 患者的二线治疗。患者之前曾接受贝伐单抗联合治疗或治疗,并在一线治疗中取得进展。
方法:患者接受氟尿嘧啶、奥沙利铂联合贝伐单抗一线治疗。CT评估进展后,随机分为IC组(伊立替康和西妥昔单抗,分别为180 mg/m2和500 mg)。/m2) 或 ICR 组(伊立替康、西妥昔单抗和雷莫芦单抗 8 mg/kg)每 2 周一次。中期分析显示 35 名患者随机分组后的 ICR 组毒性超过 3-5 级。因此,建立了改良的 ICR 方案(150 mg/m2、400 mg/m2 和 6 mg/kg)。对患者进行 PS 评分(0 vs 1),奥沙利铂与否)对治疗后进展(是 vs 否)和最后一次治疗后 6 个月内的进展(或更长)进行分层。α=0.15 或 p
结果:从 2014 年 6 月到 2017 年 7 月,对 102 名患者进行了随机分组和评估。65% 的患者为男性,9% 为黑人,8% 为西班牙裔,平均年龄为 60 岁。PS 0 占52%,24%在奥沙利铂治疗期间进展,15%在一线治疗结束后6个月以上进展。IC 和 mICR 组的 3-4 项总体毒性分别为 47% 和 54%,腹泻 10% 对 15%,皮疹 13% 对 8%,中性粒细胞减少 9% 对 10%。排除的原因是:60% 的进展、18% 的不良事件和 10% 的患者意愿。分层对数秩分析显示,mICR 与 IC 组的 PFS HR = 0.65(mPFS = 5.8 个月;p = 0.068),满足 p
结论:在 KRAS 野生型 CRC 患者中,以奥沙利铂为基础的一线治疗联合贝伐单抗进展后,二线抗体治疗联合 EGFR 抗体和伊立替康可延长 PFS。这种效果类似于其他二线抗 VEGF 治疗试验中报道的 PFS 改善。研究结果支持针对 EGFR 和 VEGF(R) 靶点的抗体组合,以便在适当的靶标人群中获得额外的好处。
注释:
这项由美国ECOG- 进行的II期临床试验,旨在回答奥沙利铂和贝伐单抗在一线进展后二线应该如何治疗:1.雷莫芦单抗是否应该用于连续抗-血管生成疗法;2.在 KRAS 野生型患者中联合抗 EGFR 和 VEGF(R) 治疗是否会使患者受益。在随机分配到 IC 和 ICR 组的 102 名患者中,近三分之二为男性,中位年龄为 60 岁,约四分之一在一线奥沙利铂治疗期间出现疾病进展。该研究的主要终点是 PFS。添加雷莫芦单抗可缩短肿瘤生长和进展时间(HR=0.65), 并且接受抗EGFR和抗双靶点联合治疗的患者疾病进展风险降低了35%,这与其他二线抗VEGF临床试验的PFS报道相似。经过近 6 个月的随访,三药联合组的总体 3/4 级毒性略高(54% vs 47%)。针对这两个靶点的抗体可以在靶 mCRC 人群中联合使用,给患者带来额外的好处 [1]。
一、抗EGFR和抗VEGF(R)双靶点联合治疗临床研究的曲折历程
抗EGFR和抗VEGF(R)疗法能否联合治疗mCRC一直是研究人员关注的问题。早在12年前,BOND和BOND-2二期临床研究就取得了积极成果,带来了双靶点联合治疗的曙光[2];同时,多项基础/临床前研究也表明,EGFR激活可以上调VEGF的表达。两种药物的表达,同时阻断两种药物可以发挥协同抑癌作用,为两种药物的联合用药提供了理论依据。然而,2012年的后续III期临床试验结果,打破了西妥昔单抗和贝伐单抗联合化疗治疗一线mCRC的美好愿望。无论是 PFS、ORR 还是 OS,双靶点治疗并不比单靶点治疗好。靶向治疗甚至会带来更多的不良反应[3]。然而,应用抗EGFR和抗VEGF双靶点治疗的尝试并没有结束。2018年,II期试验告诉我们,抗EGFR和抗VEGF(R)双靶点治疗二线治疗可能在部分mCRC目标人群中受益。
二、抗EGFR和抗VEGF(R)双靶点联合治疗在目标人群二线治疗上实现概念性突破
此次美国ECOG- 开展的临床试验的设计出发点基于两点考虑:1.以往联合双靶点治疗的研究没有考虑到RAS,并没有筛选目标人群。在该试验中,研究人员针对KRAS野生型患者,也是首次在目标人群中进行抗EGFR和抗VEGF(R)双靶点治疗的临床试验;2.由于之前的双靶点联合治疗mCRC一线治疗III期临床试验失败,考虑到一线治疗进展后肿瘤细胞可能会出现一些信号通路重构,研究人员更关心的是双靶点疗法能否用于二线治疗。尽管取得了积极成果,但这项 II 期临床试验的结果不足以改变当前的临床治疗决策。我们期待后续III期临床试验的跟进,指导我们是否可以在一线抗血管生成进展后,双靶点治疗用于RAS野生型患者的二线治疗。治疗。
三、一线抗VEGF治疗进展后继续二线抗血管生成治疗可能成为最佳解决方案
TML 和其他研究证实,贝伐单抗仍然可以使 mCRC 跨线治疗的患者受益 [4, 5]。该研究为跨线使用抗血管生成疗法提供了新的证据。一线贝伐单抗失败后,二线使用抗雷莫芦单抗改善了 PFS(HR=0.65),疾病进展风险降低 35%,研究者口头报告)并且在采访中也多次强调,这个数据与其他二线抗VEGF试验的PFS报告相似。结合今年在大肠癌领域备受关注的另一项研究[6],在贝伐单抗一线治疗失败后,瑞格非尼继以西妥昔单抗的抗血管生成效果优于西妥昔单抗继以瑞戈非尼,越来越多的证据指向患者进行跨线抗血管生成治疗的可能性。在一线抗 VEGF 治疗取得进展后,二线抗血管生成治疗策略仍有可能继续使用或成为 mCRC 患者的最佳治疗方案。
四、双/多靶点联合治疗已成为靶向治疗领域临床研究的趋势
阻断单一信号通路很容易导致肿瘤细胞获得性耐药,通过激活其他替代信号通路可以获得生长信号补偿。因此,多靶点/信号通路阻断目前正成为靶向治疗领域临床研究的热点。和趋势。在大肠癌靶向治疗领域,对于BRAF突变,单一的BRAF抑制剂无效,但必须联合BRAF抑制剂和EGFR单克隆抗体治疗[7],甚至同时抑制BRAF、EGFR和MEK[8];在扩大的难治性 mCRC 中,两种靶向药物曲妥珠单抗和拉帕替尼的组合显示出益处 [9];针对西妥昔单抗的获得性耐药,我们团队提出了Wnt通路抑制剂和EGFR单克隆抗体联合治疗策略[10]。在肿瘤免疫治疗领域,PD1抗体和抗体联合治疗已成为研究热点,研究成果令人鼓舞[11, 12]。相信会有越来越多的联合靶向治疗临床研究陆续问世,为肿瘤患者提供更多的治疗选择和临床获益。
【温馨提示】:如果您觉得陆远远博士的解读不错,请在下方点赞,把文章分享给更多的同事!当然,您也可以在下方留下您的个人意见!
参考
1. HS、PJ、O' PJ 等人。和 (IC) 和 (ICR) 作为 (CRC) 和 : 的第二行。临床杂志 2018, 36():3504-3504.
2. LB、Lenz HJ、HL 等人。II of , , and with and in - : BOND-2。临床杂志 2007, 25(29):4557-4561.
3. L、S、S 等人。III of , , 和 5-/ vs. - in 。临床 2012, 11(2):101-111.
4. J、J、D 等人。in (): a 3. 2013, 14(1):29-37.
5. Masi G、L、Boni L 等人。or of to -line in : 的。安 2015, 26(4):724-730.
6. K、T、T 等人。: II of by for with , , and . 临床杂志 2018, 36():557-557.
7. S、SL、VK 等。属于 BRAF-(SWOG 1406).J Clin 2017, 35():520-520.
8. RB、T、CE 等。BRAF、EGFR 和 MEK 在 BRAF()- 中。2018, 8(4):428-443.
9. - A、L、C 等人。Dual- with and in-, KRAS 12/13 野生型, HER2- (): a -of-, , open-, 2. 2016, 17(6):738-746.
10. Lu Y, Fan D, R et al. - 通过 Wnt/β-的 miR-100 和 miR-125b。Nat Med 2017, 23(11):1331-1341.@ >
11. Hodi FS、J、AC 等人。和 : 2 年 a , , , 2 。2016, 17(11):1558-1568.
12. RJ、NM、DF 等。加上 -Cell 。N Engl J Med 2018, 378(14):1277-1290.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话