欢迎光临吉康旅!
复星医药昨日宣布,其控股子公司贝伐单抗生物类似药已完成转移性结直肠癌Ⅰ期临床试验,并启动Ⅲ期临床试验。
贝伐单抗是重磅产品,2016年全球市场规模为67.83亿瑞士法郎;2017年国内市场规模约9.3亿元。2017年贝伐单抗通过国家议价纳入医保,仅限于晚期转移性结直肠癌或晚期非鳞状非小细胞肺癌,以及渗透率有望迅速提高。目前,齐鲁药业、信达生物制药和贝达药业在中国处于III期临床试验阶段,适应症均为非小细胞肺癌。恒瑞医药品种将于近期启动III期临床试验。公司对大肠癌适应症的选择将有助于加快临床试验的进展,
贝伐单抗生物仿制药与公司的抗 PD-1/PD-L1 具有高度协同作用。
1、抗PD-L1单抗联合抗VEGF单抗一线治疗非小细胞肺癌可显着延长患者的无进展生存期。抗PD-L1单抗联合抗VEGF单抗(贝伐单抗)一线治疗非小细胞肺癌达到主要临床终点(无进展生存期),总生存期数据有望取得优异成绩。“化疗+”组中位无进展生存期8.3个月,客观缓解率为64%,明显优于“化疗+”对照组(中位进展) - 无生存期6.8个月,客观缓解率48%);
2、抗PD-1单克隆抗体联合抗VEGF单克隆抗体在肾细胞癌一线治疗中具有极好的潜力。根据美国MD安德森癌症中心I期临床研究,抗PD-1单克隆抗体联合抗VEGF单克隆抗体阿瓦斯汀(贝伐单抗)一线治疗具有卓越疗效的潜力肾细胞癌。可显着提高患者的客观缓解率(ORR):联合/阿瓦斯汀组患者客观缓解率为53%,而单药组仅为42%,/联合组仅为38%。
复星医药30日宣布,控股子公司复宏汉霖研发的利妥昔单抗注射液(重组人鼠嵌合抗CD20单克隆抗体注射液,HLX-01) for non-)用于治疗黄金淋巴瘤的上市申请获国家食品药品监督管理总局药品注册审评受理。
汉柳斯
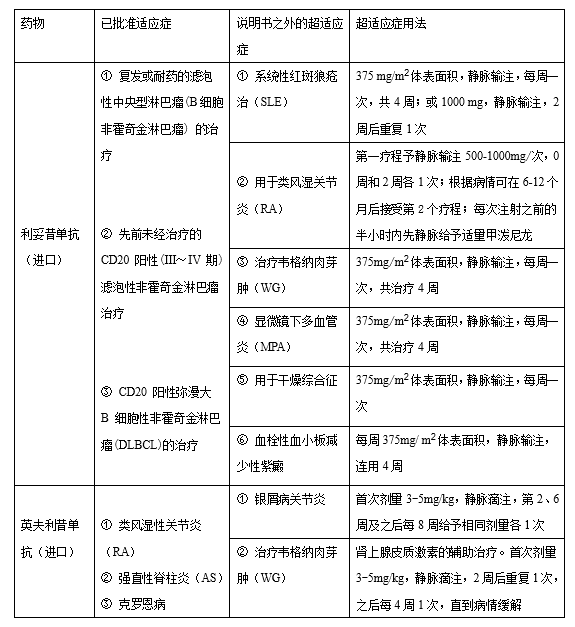
作为复星医药大分子生物药物的研发平台,复宏汉霖生物科技有限公司(简称“复宏汉霖”)致力于多个单克隆抗体药物的研发,其中首个单克隆抗体药物是对妥昔单抗有益的同类药物.
复宏汉霖单抗研发进展
公司单克隆抗体研究管线极为深厚,抗Her-2单克隆抗体正在进行III期临床试验,预计明年三季度左右完成,预计2019年上市;上市年份。也有多个创新单抗正在研发中,如抗EGFR单抗在台湾进行I期临床试验、抗单抗获得美国临床批文、PD-1单抗正在申请临床试验等。无论研发进度和在研管线的深度和广度,公司都是国内单克隆抗体领域的绝对领先者。
复兴研发
公司研发投入达到6.26亿元,占总收入的7.49%,在国内药企中仅次于恒瑞!
研发投入比恒瑞(亿元)
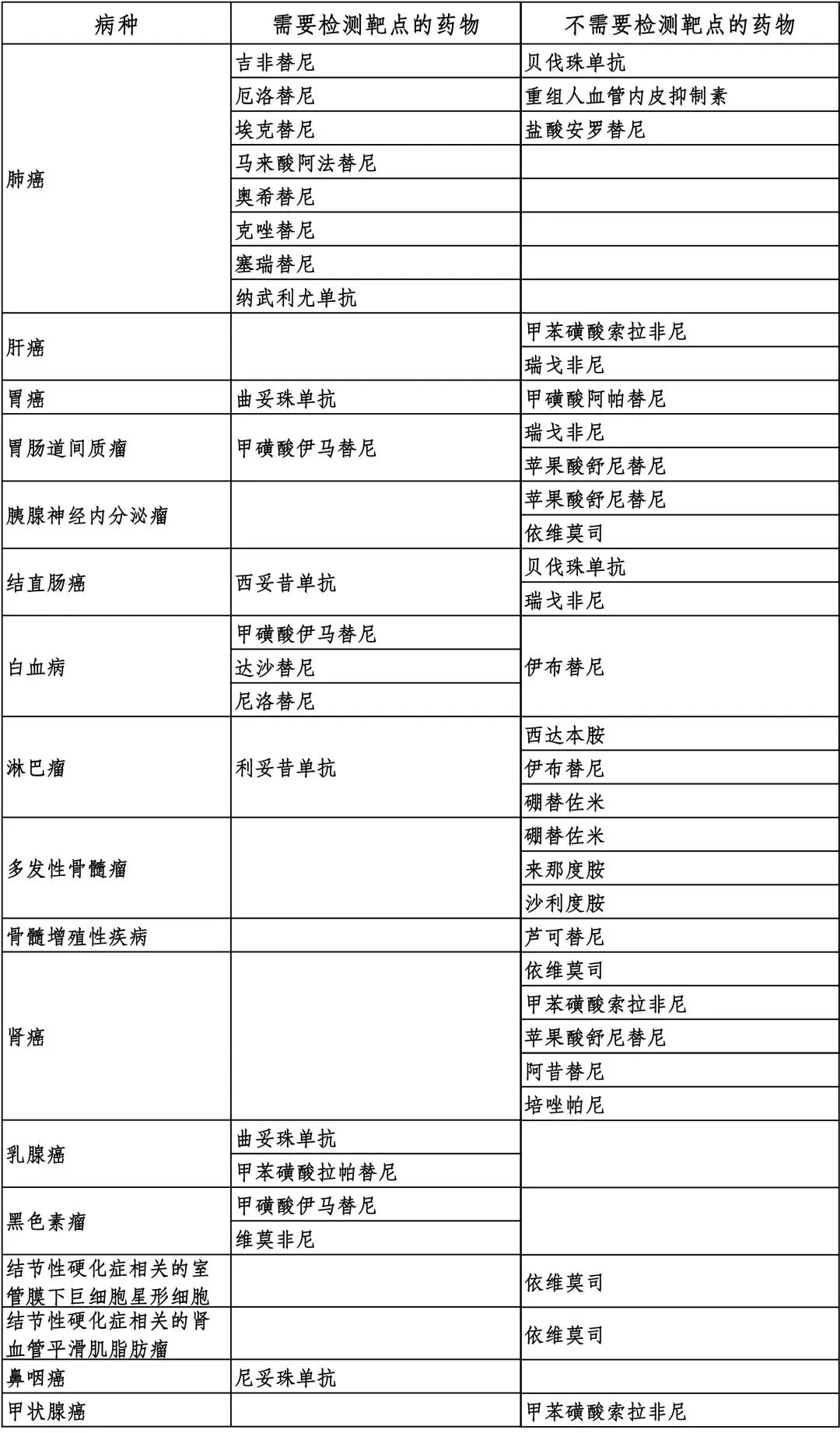
其中,多款单克隆抗体产品、第三代胰岛素、CAR-T、肺癌诊疗机器人等有望在未来5年内陆续推出,为未来业绩的高增长打下坚实基础数年。
公司产品上市预测
投资+并购
2017年1月,复星医药与KITE成立合资公司,公司与Kite各持有合资公司50%的股权。对于高风险高回报并存的CAR-T产业,复星将携手国际巨头开拓中国市场,并享有最大的盈利风险比,直接确立国内CAR-T产业的领先地位. 2017年10月,KITE的CAR-T产品成功上市。
KITE的股票在过去一年飙升
它是印度第一家获得美国FDA批准的注射剂制造商。目前拥有31个ANDA批准,产品在全球近90个国家上市。
2013年,复星医药收购禅城医院,禅城医院近年来保持高速增长,成为年轻化医疗服务领域的佼佼者。
禅城医院
研发进入收获期,从生物仿制药到创新单克隆抗体。复星医药三个生物类似药有望成为国内首个:利妥昔单抗已提交上市申请,预计2018年获批上市,成为中国首个生物类似药;曲妥珠单抗、阿达木单抗处于III期临床阶段,预计2018年提交上市申请,2019年获批上市。公司共有8个临床获批产品,包括5个生物类似药和3个创新生物药,是少数同时拥有抗 PD-1 mAb 和抗 PD-L1 mAb 的公司之一。公司同时开拓国内和欧洲市场,丰富的产品组合具有很强的协同性。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话