欢迎光临吉康旅!
9506-口服-的加号用于 EGFR-。
分析
背景和更新结果:
III期研究旨在评估贝伐单抗联合厄洛替尼对EGFR敏感患者的疗效。既往结果显示,联合用药组的无进展生存期(PFS)明显优于单药组。次要研究总生存期(OS)的结果在这次 ASCO 会议上公布。结果显示,每组112例患者,中位随访39.2个月,联合组和单药组的中位OS为50.7个月和46.2个月(HR=1.007,P=0.973),外显子19缺失亚组的中位OS为41. 9 个月未达到。外显子 21 突变亚组的中位 OS 为 50.7 个月和 38.18 个月,
两组分别有25.9%和23.2%的患者接受二线奥希替尼治疗,中位PFS2分别为28.6个月和28.@ >,分别。24.3 个月(HR=0.773, P=0.205)。在两个治疗组中,接受二线奥希替尼的患者中位 OS 优于二线化疗组分别为50.7个月和40.1个月(HR=0.645).
结论:表明贝伐单抗联合厄洛替尼可显着提高PFS,但对OS无明显益处。与结果一致,该联合方案诱导的耐药突变发生率与第一代EGFR TKI相似。
9507-oral-plus 用于 EGFR-非细胞肺线 ()。
双靶向EGFR TKI治疗:奥希替尼+吉非替尼
背景和方法:EGFR TKI 是 EGFR 敏感突变的标准治疗方法。当奥希替尼用于一线治疗时,约7%~25%的患者会出现EGFR突变,而吉非替尼可以克服这种耐药突变。当吉非替尼作为一线治疗时,约50%的患者会发生突变,而奥希替尼可以克服这种耐药突变。临床前研究表明,奥希替尼加吉非替尼可能会延缓耐药突变的出现。
我们进行了一项 I/II 期临床研究,涉及 EGFR 敏感突变的初治转移患者。该研究的主要终点是最大耐受剂量(MTD)和剂量递增和扩展阶段的可行性。次要终点是 3-5 级治疗相关不良事件、总体缓解率 (ORR)、PFS 和 OS。
结果:截止分析时,MTD 为每日奥希替尼 80mg + 吉非替尼。可行性分析中,81.5%的患者完成6个周期及以上联合治疗,客观缓解率(ORR)88.9%,疾病控制率(DCR)100% ,良好的反应:88.9%的患者达到部分反应,11.1%的患者达到疾病稳定。
在基线时,65% 的患者(26 名患者)可检测到,在治疗 2 周时,88% 的患者血浆 EGFR 变得无法检测到。
估计的中位 PFS 为 22.5 个月。疾病进展时,7例患者进行了NGS检测,未发现已知的EGFR继发耐药突变,无患者发生组织学转化。
结论:奥希替尼联合吉非替尼用于 EGFR 敏化是可行和可耐受的,并导致快速血浆 EGFR 突变清除。观察到的 ORR 为 89%,与一线奥希替尼的 ORR 相当。
9564--+:加号(pts)和(EGFR)-非细胞肺()。
亚洲人群研究结果公布
背景:III 期研究(B 部分)表明,与安慰剂 + 厄洛替尼相比,雷莫芦单抗 + 厄洛替尼显着延长了转移性 EGFR 突变的初治患者的 PFS,分别为 19.@ >4 个月和 12.4月 (HR=0.59, P
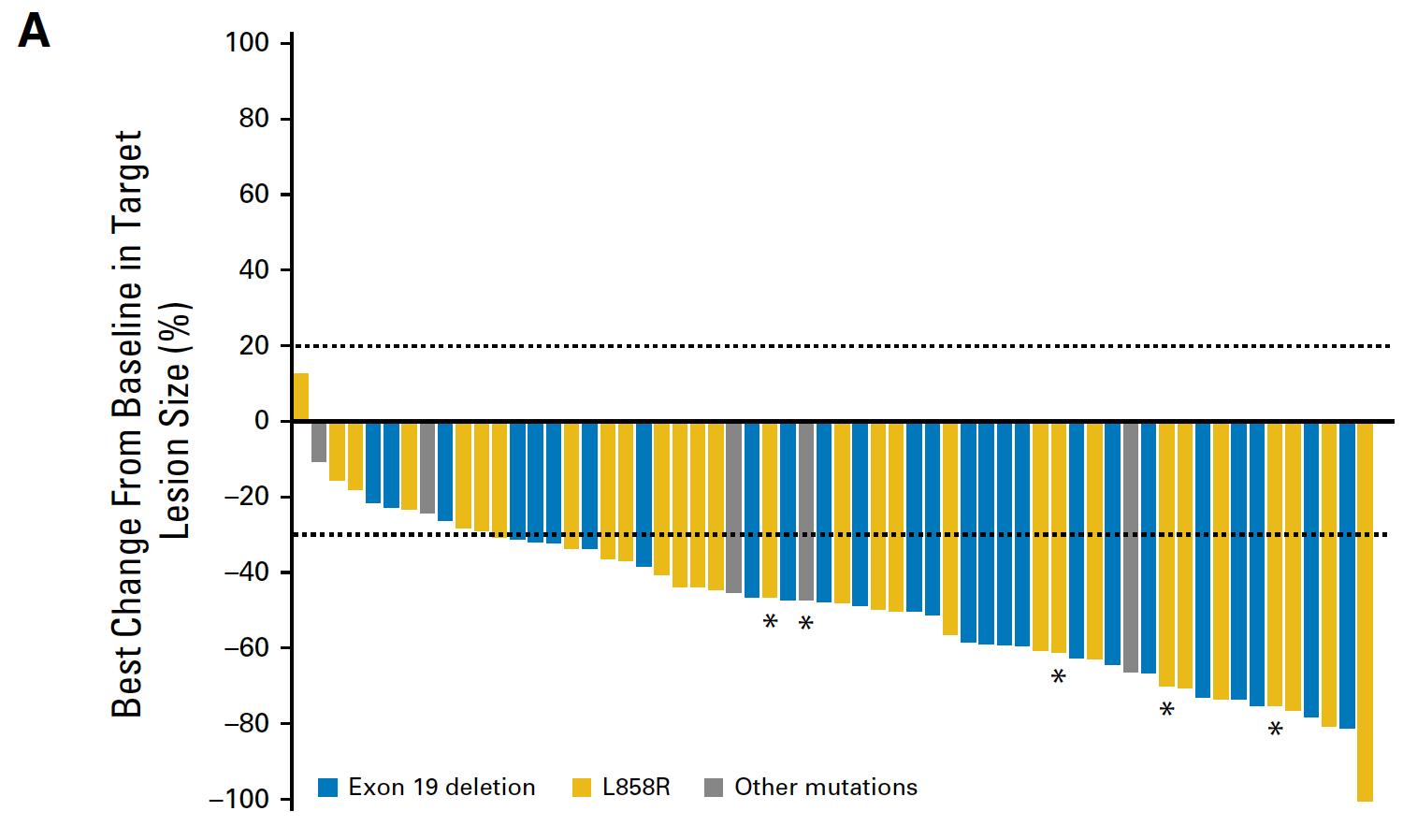
结果:本研究共纳入82例患者,其中日本、台湾、韩国分别有68例、8例和6例。女性患者占65.9%,外显子19缺失患者占43.9%。中位随访 13.8 个月,1 年 PFS 率为 65%。外显子19缺失突变和突变占67.2%(n=36)和63.4%(n=46),ORR为71%),分别,DCR 为 99%,
在 30 天的随访中,通过 NGS 测量,在疾病进展后 78%(7/9.1@> 的患者)中发现了突变。
结论:1年PFS率为65%,+研究达到了研究的主要终点。雷莫芦单抗+吉非替尼的疗效与雷莫芦单抗+厄洛替尼相当,联合治疗的不良事件与单药相当。相似的。
9569——加上作为非细胞肺-EGFR的线。
META 分析:抗血管生成药物 + EGFR TKI 的真实世界效果如何?
背景与方法:厄洛替尼是EGFR敏感突变的标准一线治疗方案之一,厄洛替尼联合VEGF抑制剂治疗EGFR突变患者仍存在争议。我们进行了一项 META 分析,以评估 VEGF 抑制剂加厄洛替尼与单独厄洛替尼在晚期 EGFR 突变患者一线治疗中的疗效。
结果:4项研究评估了贝伐单抗+厄洛替尼(,,,,等),1项研究评估了雷莫芦单抗+厄洛替尼(),5项研究包括1230例19外显子突变654例和568例,非鳞状细胞癌568例患者分别为 63% 为女性,85% 为亚洲人,60% 为非吸烟者。结果显示,VEGF抑制剂+厄洛替尼显着提高患者PFS(HR=0.59,P
结论:与单药厄洛替尼相比,VEGF 抑制剂联合厄洛替尼可显着改善 PFS 和 DOR。
9570——在非细胞肺()中带有 EGFR:A。
奥希替尼在非敏感 EGFR 突变患者中:突变和外显子 19 插入受益匪浅
背景:奥希替尼被批准用于一线治疗晚期EGFR敏感突变患者(外显子19缺失和突变,占EGFR突变的80%),或第一代EGFR TKI治疗进展后突变阳性患者。然而,奥希替尼对罕见的 EGFR 突变,包括突变、突变、突变和外显子 20 插入的疗效尚不确定。
结果:从 6 个美国数据库中确定了 51 名 EGFR 突变患者,患者特征为:72.5% 为女性,中位年龄为 65 岁,82.3% ECOG PS 0-1分,43.1% 的患者从不吸烟,100% 的患者为腺癌,25.5% 的患者为亚洲人,常见突变为(35. 3%,n =18), (27.5%, n=14) 和外显子 20 插入突变 (15.7%, n=8).3 9.2%(n=20)患者接受奥希替尼作为一线治疗,所有队列的中位生存时间为7.1个月,中位生存时间为8.一线和后线治疗分别为 9 个月和 5.9 个月。
每个队列的中位生存时间如下表所示↓
奥希替尼一线治疗突变和突变患者的中位生存时间分别为5.8个月和19.3个月(P=0.008) .
结论:结果与 2019 年在韩国进行的一项 II 期研究相似,突变和外显子 19 插入似乎从奥希替尼治疗中获益更多。
9571--抗与谁 EGFR TKI :来自 I/II 的数据。
新型第三代EGFR TKI颅内疾病控制率90.6%
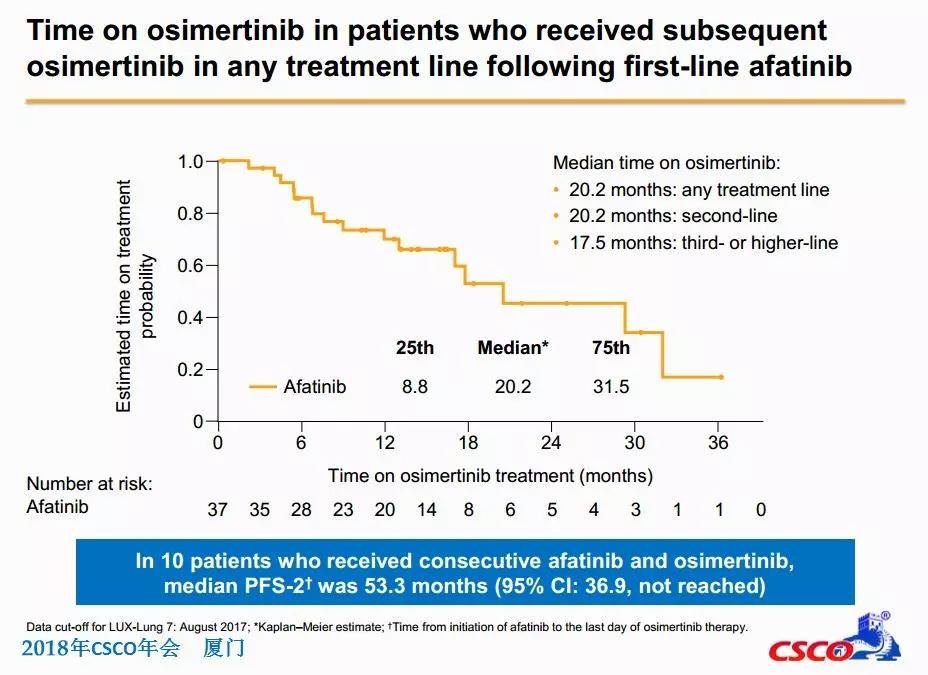
背景与方法:是一种高选择性、不可逆的第三代EGFR TKI,可靶向EGFR敏感突变和突变。临床前研究表明,它具有高血脑屏障渗透性。颅内治疗的疗效结果。这是一项 I/II 期剂量递增、剂量扩展研究,针对在先前 EGFR TKI 治疗后出现进展的晚期患者。主要终点是独立审查委员会评估(IRC)颅内客观缓解率(IORR)和颅内无进展生存(IPFS)。
结果:截至 2019 年 9 月 30 日,共有 181 名患者接受了至少 1 剂(20、7 剂量水平)。脑转移分析人群纳入64例患者,颅内疾病控制率(IDCR)为90.6%,中位IPFS未达到。在可评估的脑转移人群中,共有 22 名患者,OIRR 和 IDCR 分别为 54.5% 和 90.9%。在 7.2%(13/181) 患者中,大脑是第一个现有或新的疾病进展部位。
结论:与临床前研究一致,证明了对脑转移具有临床意义的活动。临床试验信息:。
9572 - 和 240 毫克作为 EGFR 的剂量:来自 I/II 的数据。
安全可行
背景和方法: 的 II 期研究的推荐剂量。纳入既往 EGFR TKI 治疗后疾病进展的晚期疾病患者,78 名患者接受治疗,76 名患者确认阳性突变。
结果:截至 2019 年 9 月 30 日,共有 78 名患者接受了至少一剂 (),中位年龄为 62 岁,中位随访时间为 9.6 个月。76例突变阳性患者中,ORR为57.9%,DCR为89.5%,中位PFS为11.0个月,中位DoR为13. 8 个月,2 经研究者评估的 ORR、DCR、中位 PFS 和中位 DoR 分别为 72.4%、94.7%、1< @3.2 个月和 11.8 个月。
结论:240 mg 具有良好的安全性,在阳性患者中显示出良好的抗肿瘤活性。
9573--以非细胞肺()EGFR(-L004).
安罗替尼+埃克替尼对有突变或AKT1突变的患者,ORR为72%
背景与方法:有研究表明,抗血管生成药物+EGFR TKI可显着提高EGFR突变患者的PFS。与贝伐单抗不同,安罗替尼更方便,可抑制更多靶点,与安慰剂相比,安罗替尼三线治疗可显着延长晚期患者的PFS和OS。罗替尼+埃克替尼的疗效和安全性。这是一项针对局部晚期转移性 IIIB/IIIC 或 IV 非鳞状细胞癌患者的前瞻性、单臂、多中心临床研究。允许具有 EGFR 敏感突变的初治患者入组。
结果:2018 年 7 月至 2019 年 12 月,共有 35 名患者入组研究,接受安罗替尼 + 埃克替尼治疗。2020年7月数据截断时,初步结果显示中位随访6.01个月,32例可评价疗效的患者中,ORR为59%,DCR为88%,67%(10/ 15)外显子缺失 19 和 53% (9/1<@)7) 突变患者达到客观缓解。18 例突变或 AKT1 突变和/或肿瘤抑制基因(TP53、RB1 和 PTEN)患者的 ORR ) 为 72%。
结论:安罗替尼+埃克替尼对接受过治疗的晚期EGFR突变患者疗效良好,联合治疗耐受性好,不良事件可控。临床试验信息:。
9574-- () 在与-naïve EGFR- 非细胞肺 (): II 中。
它如何在脑损伤中起作用?
背景和方法:之前的 I/II 期研究表明,EGFR 突变初治的晚期或转移性疾病患者有持久的反应,脑损伤患者的疗效和耐受性更好。ASCO 会议公布了 II 期研究的 OS 结果。该研究包括接受过 EGFR 敏感突变的患者( )。主要终点是总体反应率(ORR),次要终点是 DCR、DOR、PFS 和 OS。
结果:截至 2019 年 11 月,45 名患者被纳入研究,58% (26) 的 ECOG PS 为 1,40% (18) 在基线时有脑转移,56% 有外显子 19 缺失,40% 的患者有突变后,总人群中的 ORR 为 69%,BIRC 评估的中位 PFS 为 18 个月,中位 OS 未达到 33 个月,脑转移和无脑转移亚组的影响如下表所示。
结论:随着随访时间的延长,中位 OS 尚未达到,并且是一种很有前景的第三代 EGFR TKI,它在 EGFR 突变初治的晚期患者(包括脑转移)中显示出疗效。临床试验信息:。
9583--c-MET、AXL 和 -2 的 Ib 以及 EGFR-TKI 与 .
中国之声:+吉非替尼有望克服非耐药突变
背景与方法:它是一种针对 Met、Axl、-2、Mer 和 Flt3 突变的新型 TKI。这项由中山大学肿瘤中心张莉教授进行的Ib期研究评估了安全性并确定了II期研究的推荐剂量(RP2D),并研究了+吉非替尼对阴性患者的疗效和安全性。开发的获得性耐药性进行了探索。该研究包括至少一名 EGFR TKI 和阴性获得性耐药的中国晚期患者。主要终点是安全性和 RP2D,次要终点是药代动力学和抗肿瘤活性。
结果:2016 年 11 月至 2019 年 12 月期间,共有 86 名患者入组和治疗(30 mg,n = 36;40 mg,n = 46;60 mg,n = 4),36% 的患者发生脑转移基线时,有 66%/33%/1% 曾接受过一线/二线/三线 EGFR TKI 治疗。常见的治疗相关不良事件 (TRAE) (≥30%) 是心肌酶升高 (所有等级和 3 -4 等级分别为 74.4% 和 0%),转氨酶升高(73.3%;2.3%),皮疹(60. 5%);3.5%),蛋白尿(44.2%;0%),凝血异常(37.2%;15.1%),腹泻(33.7%;2.3%)和高血压(32.6%;11.6%)。RP2D 为 40 mg,可在 84 名患者中评估 在受影响的患者中,ORR 为 19.1%(其中,16 名达到 PR),DCR为91.7%(其中61人达到SD,7人达到PD)。2020 年 1 月 9 日在每日数据截止时,65 名 (75.6%) 患者出现疾病进展,中位 PFS 为 4.4 个月,72 名 (83.7 %)患者接受C.-Met基因扩增检测,基因拷贝数(GCN)较高的患者反应较好,GCN≥9.08@>GCN≥9.09@>GCN≥3亚组的ORR为3< @6. 4%、25.0% 和 21.6%。
9.13@>
9.14@>
结论:40 mg 的 RP2D 联合治疗在 EGFR TKI 突变患者中显示出有希望的抗肿瘤活性。C-Met GCN 可能是预测效果的潜在生物标志物。临床试验信息:。
9586--EGFR+ 非细胞肺中 CNS 的高剂量 ():A - 。
奥希替尼升级使更多软脑膜转移患者受益
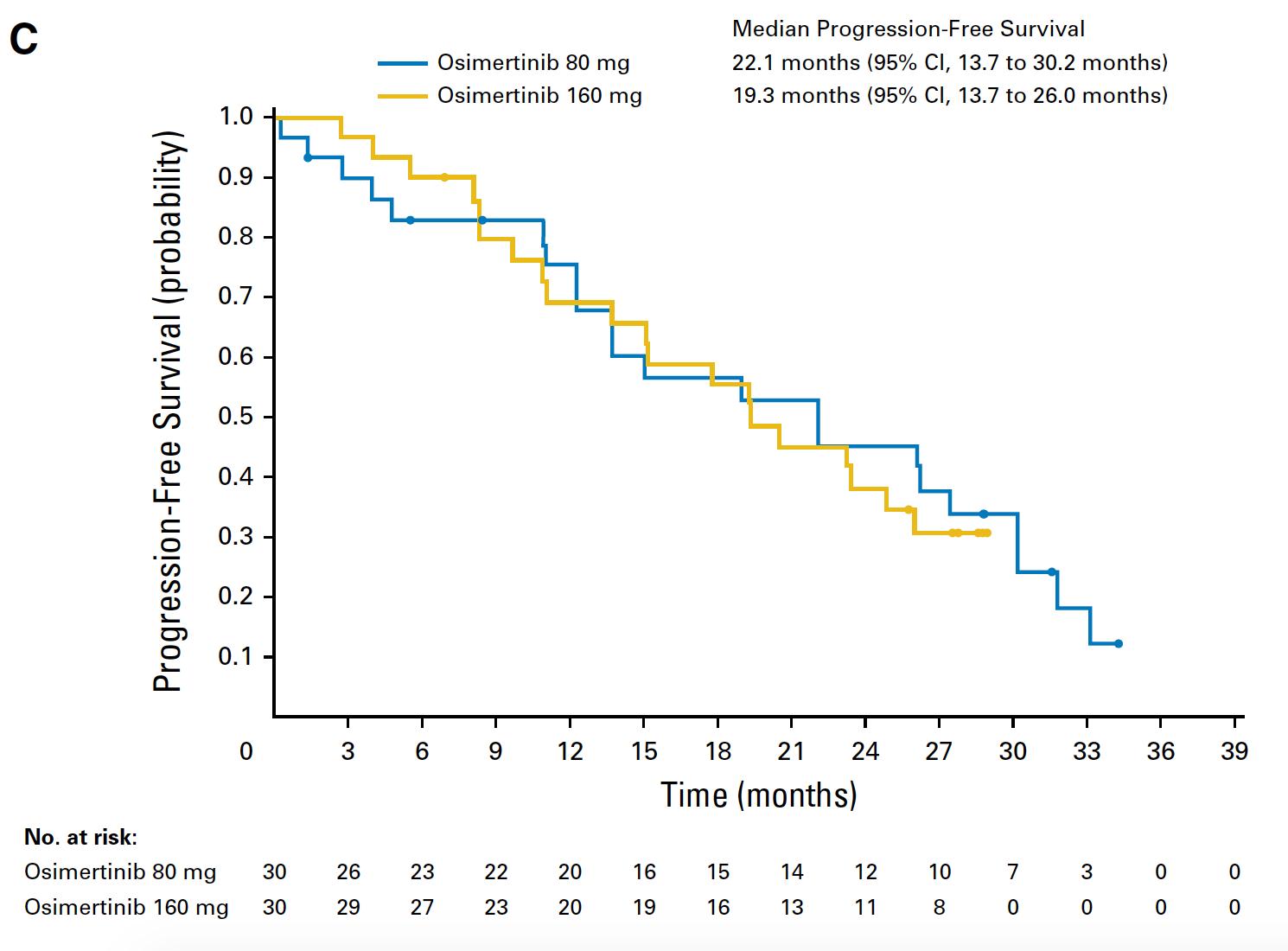
背景与方法:研究表明,大剂量奥希替尼 160 mg QD() 在中枢神经系统 (CNS) 或软脑膜转移 (LMD) 患者中显示出活性,但奥希替尼 80 mg 对 CNS 剂量对疾病进展的影响尚不清楚。该研究回顾性分析了接受奥希替尼治疗的 105 名 EGFR 阳性患者,这些患者在接受 80 毫克至(队列 A,24 名患者)或 80 毫克至同时化疗和/或放疗(队列 B,34 名患者)的中枢神经系统疾病进展患者队列中) 和奥希替尼直接给药(队列 C,11 名患者)。CNS 疾病控制的中位持续时间 ( ) 定义为从服用奥希替尼到 CNS 疾病进展或停止治疗的时间。
结果:在 105 名患者中,69 名 CNS 疾病进展患者在 2013 年 10 月至 2020 年 1 月期间接受了奥希替尼治疗,61 名(90%)患者出现孤立的 CNS/LMD 疾病进展而没有全身疾病进展。队列 A 的中位数为 3.8 个月,在队列 B 中,孤立性 LMD 患者的中位数为 5.8 个月,脑实质转移患者的中位数为 2 个月,联合治疗的中位数为5.1 个月,C 队列的中位数为 4.2 个月。
9.19@>
结论:在 80 mg 奥希替尼治疗中,对奥希替尼的剂量递增对具有 CNS 或 LMD 进展的真实世界 EGFR 阳性患者提供了适度的益处,并且剂量递增模式似乎比奥希替尼初治治疗对 LMD 疾病更有效。在接受治疗的中枢神经系统疾病进展患者中也显示出相当大的益处,尽管该研究受到小样本量和研究设计的限制,但结果表明需要优化这种给药方式以更好地管理中枢神经系统疾病进展患者。
9597--A II 用于非细胞肺 EGFR 的初始 CNS:(1603/WJOG)。
第一项研究:奥希替尼联合放疗治疗突变脑转移患者
背景和方法:大约 15%–30% 接受 EGFR TKI 治疗的患者发生 CNS 进展。本研究旨在评估奥希替尼联合放疗对中枢神经系统转移患者的疗效。这是一项针对未接受放射治疗的 CNS 转移患者的 II 期研究,两个队列是一个队列和一个一线治疗队列。主要终点是脑转移患者的标准评估反应率(BMRR),该队列的结果发表在本研究中。
结果:在 2016 年 10 月至 2019 年 7 月期间,该队列包括 40 名患者,BMRR(标准)为 66.7%,BMRR(标准)为 70.0%,中位 PFS 为7.1 个月,ORR(标准)为 40.5%。
结论:这是第一项评估奥希替尼联合放疗在脑转移和 EGFR 突变的初治患者中的应用的研究。该研究达到了主要终点。结果表明,突变脑转移患者应在放疗前尝试接受奥希替尼治疗。倪治疗。
9602-- and of () in with - : A IIb-arm 。
中国好声音:新型第三代EGFR TKI
背景与方法:( )是第三代EGFR TKI。石元凯教授团队的这项研究是一项IIb期多中心单臂研究,旨在评估突变患者的疗效和安全性。该研究纳入第一/二代EGFR TKI治疗后局部晚期或转移性疾病进展或初治突变的患者,接受(80 mg,每天两次),主要终点为ORR,次要终点包括DCR、PFS、和操作系统。
结果:2018年6月至2018年12月共纳入220例患者,212例患者为IV期,截至2019年4月12日,ORR为73.6%,估计6周和12周DCR率为87.3% 和 82.3%,中位 PFS 为 7.6 个月,中位 OS 和 DoR 未达到。
结论:在 EGFR 突变患者中显示出有希望的疗效和安全性。
厚朴方舟成立于2012年,总部位于北京。成立了由全球权威医学专家组成的美日名医集团。是日本政府正式颁发的第一家具有海外医疗资格的公司。如需境外就医,请拨打免费热线咨询!
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话