欢迎光临吉康旅!
AACR 会议如火如荼。4月16日上午,肺癌免疫进展专场上,晚期一线治疗+贝伐单抗+化疗的研究公布了不同PD-L1表达水平患者和EGFR+/ALK+患者的PFS数据,以及邀请哈佛大学麻省总医院F.教授现场点评。以下是现场评论的精彩内容。
F. 教授现场点评
贝伐单抗是一种抗血管生成单克隆抗体,铂类化疗联合贝伐单抗已被批准用于晚期非鳞状细胞癌一线治疗。它是一种抗PD-L1单克隆抗体,与多西他赛相比,在晚期二线及以上治疗中可显着延长患者的OS。贝伐单抗联合用药具有协同作用。贝伐单抗除了具有抗血管生成作用外,还可以通过抑制VEGF来达到免疫调节作用,主要通过以下三种机制:1.诱导树突状细胞成熟,从而促进T细胞的活化;2.使肿瘤血管正常化,从而增加T细胞进入肿瘤;3. 通过下调 MDSC 和 Treg 细胞,它建立了一个“热” 肿瘤微生物组。环境。因此,贝伐单抗可以通过逆转 VEGF 介导的免疫抑制作用来增加活化 T 细胞的肿瘤杀伤作用。
审稿人 F. Prof.
这是一项多中心、随机、对照的 III 期临床研究,评估化疗联合化疗(卡铂和紫杉醇)联合或不联合贝伐单抗治疗初始 IV 期非鳞状细胞癌患者的疗效和安全性。分配到3个治疗组:+卡铂+紫杉醇(A组,n=402),或+贝伐单抗+卡铂+紫杉醇(B组,n=400),或贝伐单抗+卡铂+紫杉醇( C组,对照组,n=400)。本研究入组患者均进行治疗标本活检,可进一步进行生物标志物分析。根据患者是否携带获得性驱动基因分为ITT-WT(87% 的随机患者)和 EGFR/ALK 阳性患者(13%)。ITT-WT患者根据免疫相关基因表达谱进一步分为Teff-High WT组和Teff-low WT组(Teff基因表达谱包括PD-L1和IFNγ三个基因的mRNA表达水平)。该研究旨在分析不同PD-L1表达水平(通过IHC方法检测)患者的疗效。数据。
本次报道的数据中,ITT-WT患者中,不同PD-L1表达水平的患者(根据抗体检测,分为高表达、低表达和无表达三组),B组的PFS明显好于. 在 C 组中,即使是 PD-L1 表达阴性的患者(TC0 和 IC0).
图 1. 150 个不同亚组患者的 PFS 比较
蓝图方案中,22C3、28-8和这三种试剂在PD-L1在肿瘤细胞中的染色比较一致,而染色阳性的肿瘤细胞少于其他三种试剂。因此,研究人员设想,如果150研究中的患者被另一种PD-L1抗体染色,结果会受到影响吗?研究人员进一步使用抗体对患者的肿瘤组织进行染色。结果表明,使用两种抗体,PD-L1均不表达,低表达和高表达的患者比例相等。并且不同抗体检测平台的结果是一致的。在无 PD-L1 表达的患者中,B 组的 PFS 也明显优于 C 组。
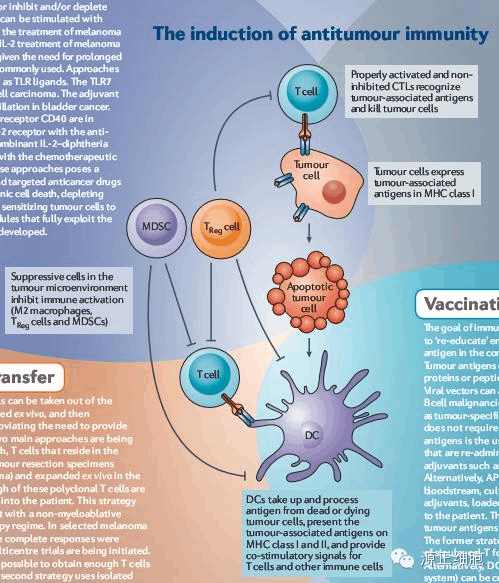
图2.使用不同的PD-L1抗体检测平台,150项研究结果一致
为什么是这样?
本研究最大的特点是部分EGFR+/ALK+患者同时入组。这些患者能从免疫治疗中受益吗?研究人员进一步分析了这些患者的疗效(n=108),结果显示在EGFR+/ALK+患者中,B组的PFS也明显优于C组,mPFS为9.@ > 7 个月和 6.1 个月(HR=0.59;95%CI:0.37-0.94)。值得注意的是,在 108 个 EGFR+ /ALK+患者,6例出现EGFR/ALK双突变,ALK+患者中,18%出现EGFR突变,双突变发生率高于以往研究报道,阳性的可能性值得关注。
图3. 150 项研究招募了 108 名 EGFR+/ALK+ 患者
下一步是什么?
F.教授还回顾了目前免疫组合在高级一线治疗中的临床研究。大多数研究排除了 EGFR+/ALK+ 患者。总结如图4所示。因此,在研究中,EGFR+/ALK+患者的疗效分析是本研究的一大特色。未来需要更多的研究来探索EGFR+/ALK+患者是否适合一线免疫治疗。
图4.免疫联合在晚期一线治疗中的临床研究
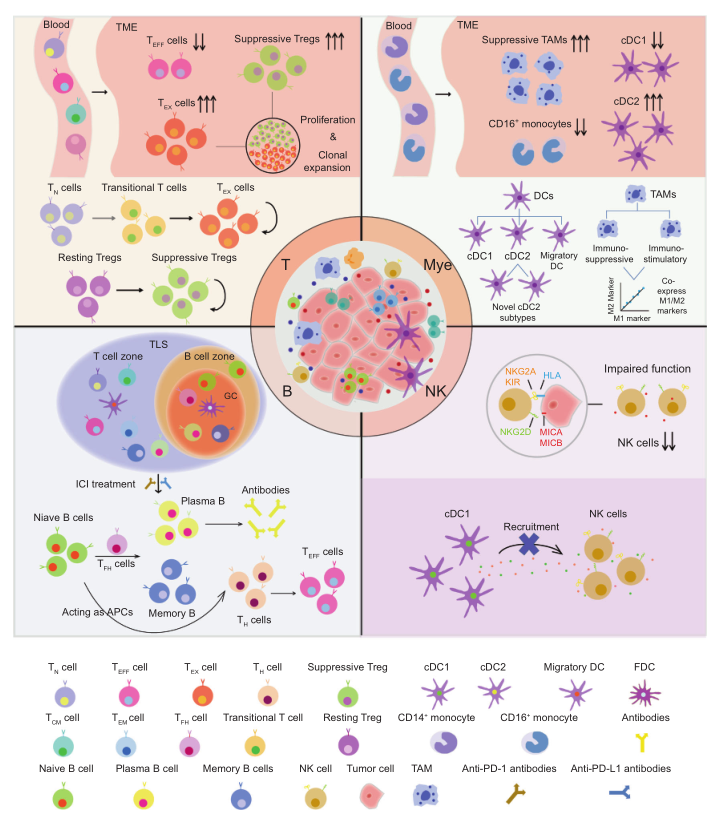
本次会议还报道了化疗联合化疗的III期研究。F. 对这两项研究进行了比较。虽然两项研究均取得了积极成果,但值得注意的是,在入选人群的选择上存在差异。一定的区别。
图 5. 与 189 项研究的比较
最后,F.教授对研究进行了总结。这是一项具有更好研究设计的大规模III期临床研究。结果表明,紫杉醇卡铂+贝伐单抗联合用药可显着延长患者的PFS。,无论其 PD-L1 表达状态如何。此外,该研究也是第一个观察到免疫治疗对 EGFR+/AK+ 患者有显着益处的随机临床研究。期待研究进一步随访后OS数据的报告,以及A组和C组患者的疗效对比。值得注意的是,随着晚期一线治疗的转变模式,我们应该站在一个新的起点,重新审视这项研究的实际临床意义。
-150 个总结
背景
在一项随机对照的 3 期临床试验研究中,非鳞状细胞癌患者的一线治疗,无论 PD-L1 表达水平如何,(抗 PD-L1)+bev+化疗与bev+化疗. 该分析旨在进一步了解 +bev + 化疗在关键亚组中的疗效:由 IHC 和 EGFR/ALK 改变定义的 PD-L1 表达亚组以及基线时有肝转移的患者。
方法
患者接受 1200 mg + bev 15 mg/kg + 卡铂 (C) AUC 6 + 紫杉醇 (P) 200 mg/m2(B 组)或 bev + C + P(C 组)q3w。共同主要终点是 ITT-WT(EGFR 或 ALK 野生型患者)人群的 PFS,次要终点由肿瘤细胞 (TC) 和肿瘤浸润免疫细胞 (IC) 上的 PD-L1 表达定义对于亚组的 PFS,预先指定了探索性回顾性分析。
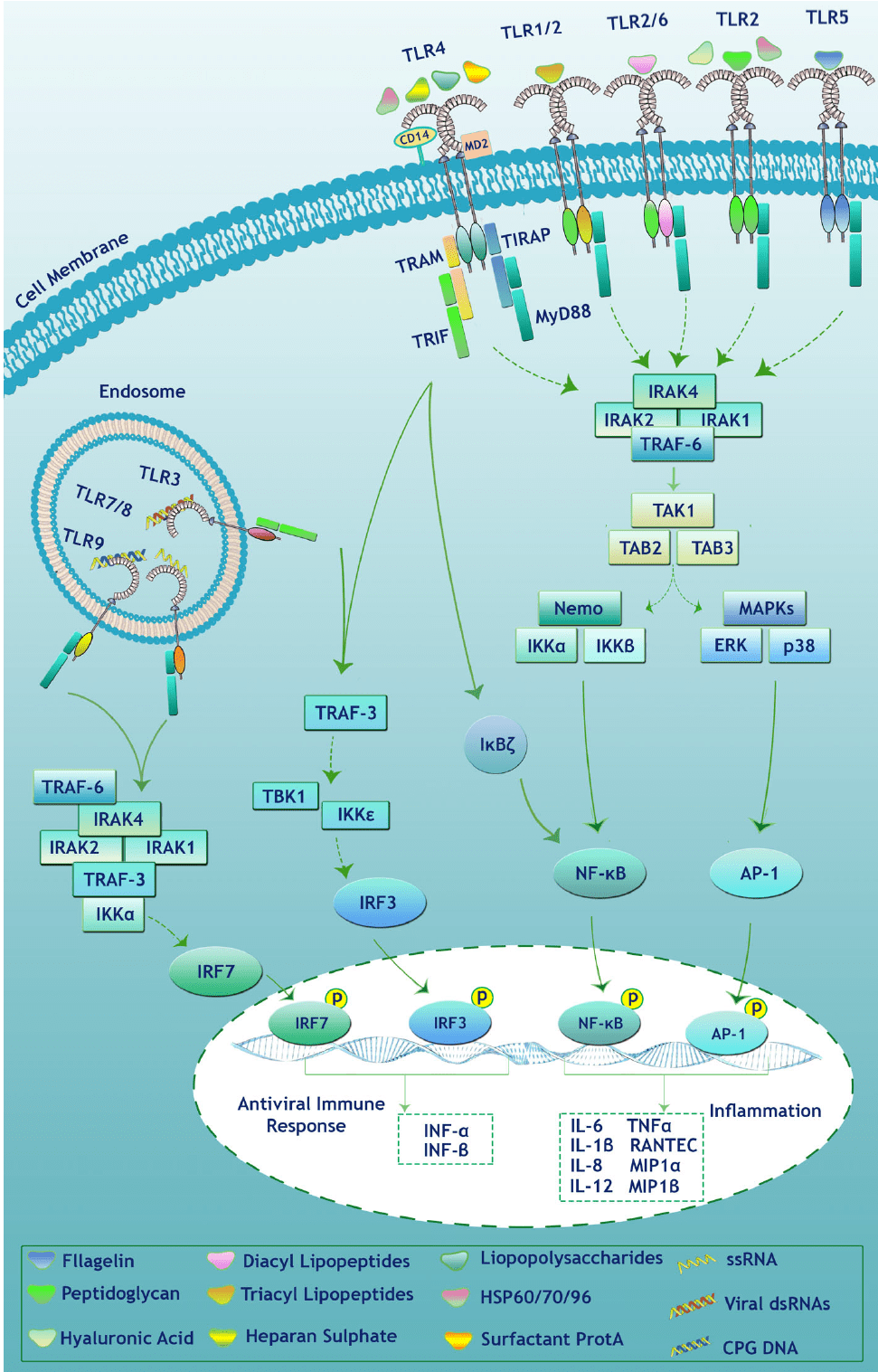
结果
在 ITT-WT 的 B 组和 C 组 (n=692)) 中,503 名患者的肿瘤切片可用于检测 (BEP)。ITT-WT 和 BEP 的患者特征相似。在这两项测试中,在该方法定义的所有 PD-L1 表达亚组(包括 PD-L1 阴性和 PD-L1 低表达的患者)中,B 组与 C 组观察到了相似的 PFS 益处。在 EGFR 或 ALK 基因组改变的患者中也观察到了 B 组与 C 组相似的 PFS 益处,包括具有可操作 EGFR 突变的患者和基线时有肝转移的患者。
综上所述
在所有 PD-L1 亚组中均观察到 +bev + 化疗的益处,无论使用何种 IHC 测定。此外,在具有 EGFR/ALK 基因组改变的患者和具有这种基因组改变的肝转移患者中也观察到了具有临床意义的 PFS 益处。
表 1:生物标志物亚组与研究中其他亚组的 PFS 分析
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话