欢迎光临吉康旅!
卵巢癌的标准治疗是基于手术的综合治疗(综合分期手术或细胞减灭术)。除少数FIGOⅠ期患者外,大部分患者术后需化疗联合紫杉烷和铂类,80%的患者一线治疗可达到完全缓解。然而,超过 70% 的患者在 5 年内仍会复发。复发后的各种治疗方案,包括各种二线化疗药物,效果非常有限,大多数患者最终在多次复发期间对化疗药物产生耐药性。在精准治疗的指导下,靶向药物治疗成为现阶段肿瘤治疗研究最多的热点。目前,复发性卵巢癌的分子靶向药物治疗研究较多,存在诸多问题和争议。临床上应综合考虑,掌握适应证,单独选择药物。中国人民解放军总医院第一医学中心妇产科 颜红
1. 复发性卵巢癌靶向药物治疗的临床研究与共识
1.1 抗血管生成药物
以贝伐单抗为代表的抗血管生成药物是治疗复发性卵巢癌研究最多的靶向药物。贝伐单抗是一种针对血管内皮生长因子 (VEGF) 受体的人源化单克隆抗体。贝伐单抗联合化疗治疗复发性卵巢癌的Ⅲ期临床研究有3项,分别是,和。该研究针对对铂敏感的复发性卵巢癌患者。入组一线治疗6个月以上复发的卵巢癌、输卵管癌和原发性腹膜癌患者484例。随机分组后,分别给予他们GC(吉西他滨+卡铂)。)+安慰剂和GC+贝伐单抗治疗。
帕唑帕尼 ( ) 是一种酪氨酸激酶抑制剂,可阻断由 PDG-FR 和 c-kit 等多种受体介导的血管生成、细胞增殖和肿瘤转移的信号通路。其中,是帕唑帕尼的主要靶点。AGO——是一项随机、双盲、III 期研究,招募了 940 名在一线治疗结束时没有进展的晚期卵巢癌患者。随机分组后,他们分别接受了帕唑帕尼和安慰剂的维持治疗。结果表明,与安慰剂相比,帕唑帕尼可显着改善 PFS(17.9 个月 vs 12.3 个月,P=0.0021)。研究未显示亚洲女性的 PFS 获益(18.1 个月 vs 18.1 个月)。
() 是一种口服酪氨酸激酶抑制剂,治疗靶点为-1, 2, 3。在II期临床研究中,西地尼布单药治疗已显示其治疗复发性卵巢癌的有效性。该试验是一项随机、双盲、安慰剂对照的西地尼布联合化疗和维持治疗铂敏感复发性卵巢癌的III期临床试验,共有456名患者入组。中期分析结果显示,与单纯化疗组相比,西地尼布维持组的PFS延长2.0个月(11.4个月vs9.4个月, HR0.68,P=0.0022),主要副作用为腹泻、中性粒细胞减少和过敏反应。
此外,血管生成素抑制剂曲巴尼 (, ) 是一种血管生成素抗体肽,目前正处于 III 期临床试验-1 和-2 的药物联合化疗药物治疗复发性卵巢癌,-1 研究显示联合治疗组的 PFS 优势(12.5 月 vs 10.9 月,P=0.024),但只有基线时腹水的患者有 OS 获益。来自 the-2 研究的当前数据显示,联合组的客观缓解率 (ORR) 和 DOR 具有优势,但尚无生存数据。
1.2 靶向DNA修复酶的药物
PARP(poly ADP-ri-bose)是一种多功能蛋白质翻译后修饰酶,存在于大多数真核细胞中,在DNA损伤修复和细胞凋亡中发挥重要作用。在以往的I期和II期临床试验中,口服PARP抑制剂奥拉帕尼()对复发性/2突变卵巢癌患者可取得良好的疗效,副作用轻微。该研究是奥拉帕尼联合化疗治疗铂敏感复发性BRCA突变卵巢癌的III期临床试验。入组295例患者,随机分为化疗组和化疗联合奥拉帕尼和奥拉帕尼。镍钛诺维持治疗组。结果显示,BRCA突变患者接受奥拉帕尼可显着延长PFS(5.
-OV16/NOVA 是 (-rib) 用于维持治疗化疗后铂敏感复发性卵巢癌的 III 期临床试验。共纳入 553 名患者,其中 350 名患者没有 BRCA 基因突变。以 2:1 的比例随机分为尼拉帕尼治疗组和安慰剂组。结果表明,无论基因突变患者还是非突变患者,尼拉帕利维持治疗均能显着延长PFS(突变组:21.6个月vs5.5个月,HR0.27;无突变但HRD阳性组12.9月vs3.8月,HR0.38),研究中最常见的严重不良反应为血液学毒性,剂量调整是可控的。
这也是 () 治疗铂敏感复发性卵巢癌的 II 期临床研究。共纳入 206 名患者,根据基因状态分为 3 个亚组:BRCA 突变(n=40)、同源重组缺陷 LOH-high(n=82) 和 LOH-low) n=70),12例为BRCA野生型,但由于标本中肿瘤组织不足,同源重组分类。结果显示BRCA突变组的中位PFS为12.@ >8月,LOH高组5.7月,LOH低组5.2月。BRCA突变或BRCA野生型但LOH水平高的患者使用可以有更好的PFS获益,最常见的严重副作用是贫血。
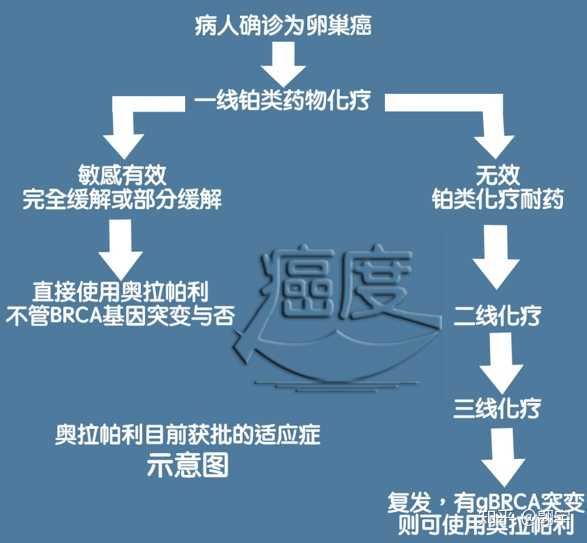
基于上述研究,在国际妇产科联合会(FIGO)和美国国家综合癌症网络(NCCN)指南中,贝伐单抗和培唑帕尼联合二线化疗已被推荐用于治疗复发性卵巢癌。癌症。并推荐贝伐单抗、奥拉帕尼和勒卡帕尼单药治疗复发性卵巢癌。最近,美国食品药品监督管理局(FDA)扩大了奥拉帕尼的适应症,批准了一种新的奥拉帕尼剂型(片剂)用于所有对铂敏感的复发患者,无论是否存在 BRCA 突变。
2. 探索具有有效靶点的分子标志物,筛选靶向药物治疗的最佳受益人群
根据靶点分子标志物的检测结果,选择相应的治疗药物是最理想的靶向药物治疗模式。例如,表皮生长因子受体家族成员EGFR在非小细胞肺癌中检测到,一线使用EGFR-TKI药物对EGFR敏感突变患者可取得良好效果。在转移性结直肠癌中,KRAS野生型患者是一线化疗联合西妥昔单抗的主要受益者。
在卵巢癌中,抗血管生成药物贝伐单抗是目前研究最多的靶向药物。然而,仍然缺乏可靠的分子靶点来分类和筛选可能受益于贝伐单抗使用的患者群体。对于其他肿瘤研究较多的EGFR-TKI药物,虽然在基础研究中确实存在EGFR蛋白在卵巢癌中的过度表达,但遗憾的是,在少数研究中并没有发现EGFR蛋白。基因突变和蛋白表达与EGFR-TKI药物疗效的相关性。
临床研究表明,具有/2突变的卵巢癌患者可能受益于PARP抑制剂治疗,可以延缓肿瘤复发,将复发风险降低70%。此外,研究还发现,PARP抑制剂的治疗对BRCA突变阴性卵巢癌患者也有效。这些患者使用 PARP 抑制剂的靶点是什么?是在同源重组途径上还是有其他位点还需要进一步深入研究。要努力寻找准确的分子靶点指导临床用药,使靶向治疗真正做到精准有效。
3. 复发性卵巢癌靶向药物的时机
卵巢癌的复发和耐药性一直是妇科肿瘤领域的难题。对于复发性卵巢癌患者,应该有一个长期的终生管理计划。从治疗开始,就应根据患者的经济能力和病情选择针对性治疗。和维持药物,减少不良反应,提高生活质量。事实上,靶向药物的最佳应用时机和方法,无论是一线还是二线,与标准化疗同时和序贯应用,还是化疗后的维持治疗,都需要高水平的循证支持。医学证据。合理的用药选择和用药顺序可以减少治疗的毒副作用,
尽管上述部分RCT研究证实,使用贝伐单抗、奥拉帕尼等靶向药物治疗复发性卵巢癌可提高患者的PFS,但大多数研究未能观察到对OS患者的益处。此外,使用贝伐单抗等抗血管生成药物毒副作用较大,显着影响患者的生活质量,无进展生存期获益不是很显着。PARP抑制剂的研究数据清楚地表明了其高效、低毒的优势。其他治疗卵巢癌的靶向药物并没有显示出如此显着延长患者的PFS,并且耐受性良好,部分患者已经治疗6年以上。. 这表明PARP抑制剂可能在未来复发性卵巢癌的临床治疗中发挥重要作用。然而,其昂贵的药价是临床应用的障碍。
因此,在靶向药物治疗的临床应用中,不能不经意间权衡利弊,应综合考虑药物方案的成本效益和成本效益。
4. 讨论合理和最优的细胞毒药物

临床上,大多数靶向药物与传统的细胞毒药物联合使用。如何选择与靶向药物联合使用的细胞毒药物值得探索。从理论上讲,与靶向药物相适应的化疗方案应具有适当的强度,不应叠加毒性,使靶向药物发挥最大的作用。如果化疗方案过强,会增加患者出现毒副作用的风险,或者靶向治疗药物的疗效受到化疗天花板效应的影响。例如,在晚期结直肠癌中,多项 Meta 分析表明,与以伊立替康为基础的化疗相比,贝伐单抗联合氟尿嘧啶单药治疗或以奥沙利铂为基础的化疗并未显着改善患者的 OS。
在卵巢癌的治疗中,常规的一线或二线化疗方案主要配合靶向药物,如紫杉醇+卡铂、吉西他滨+卡铂、脂质体阿霉素单药、紫杉醇单药每周一次等,这些化疗方案耐受性较好. 目前,尚无同一靶向药物联合不同化疗方案的研究,以及比较其疗效的报道。因此,在探索更有效的化疗方案联合靶向药物方面仍有很大的空间。设计和开展新的临床试验以寻找靶向药物的最佳化疗方案是未来研究的另一个方向。
5. 多种靶向药物联合
肿瘤的发生和发展涉及大量的信号转导通路,它们相互影响、相互关联。当前的单一目标封锁只针对其中一个环节。一旦代偿机制完成,肿瘤细胞就可以绕过被抑制的信号通路,继续通过其他通路生长。理论上,联合靶向抑制不同的信号通路可以更有效地杀死肿瘤。研究人员已经开始在这一领域进行探索。在非小细胞肺癌和HER-2阳性转移性乳腺癌的研究中,两种靶向药物的联合用药比单一药物更有效。然而,多种靶向药物的组合并不能全部提高疗效。在转移性结直肠癌和两项临床研究中,
2005年,美国NCI启动了贝伐单抗联合厄洛替尼治疗复发性卵巢癌的II期临床研究。2007年又有一项索拉非尼联合贝伐单抗治疗复发性卵巢癌的研究,但研究结果尚未发表。2010年,NCI开展I/II期临床研究,比较西地尼布联合奥拉帕尼和奥拉帕尼单药治疗复发性卵巢/原发性腹膜/输卵管癌的疗效。研究的部分结果在 2014 年 ASCO 会议上公布,两种靶向药物联合用药显着延长 PFS(9.0 个月 vs 17.7 个月,HR0.42, P =0.002.7@>,提高了客观反应率(48% vs 80%,P=0.002)。分层分析发现,两种药物联合治疗对无 BRCA 的患者没有影响。基因突变患者的疗效提高更为明显。操作系统数据还不成熟。在多靶点个体化治疗方面值得继续探索。
随着对卵巢癌病因的深入探索,基因突变与卵巢癌发病机制和异质性的关系越来越受到重视。此外,同一患者的原发肿瘤和每个转移肿瘤之间也存在异质性。这些异质性是否会导致患者靶向药物疗效的不一致,值得进一步研究。因此,利用高通量测序技术和功能基因手段开展肿瘤基因组学研究,寻找越来越精准的治疗靶点,建立卵巢癌分子分型,指导个体化化疗治疗策略,是重要的一环。复发性卵巢癌。诊治方向之一。
此外,研究疗效显着不同的患者组肿瘤基因组差异,探索多基因多分子组合预测靶向治疗疗效。预计正在进行的基础和转化研究将发现更多有价值的靶向药物,为战胜复发性卵巢癌这一难治性妇科恶性肿瘤提供有力武器。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话