欢迎光临吉康旅!
恶性肿瘤免疫治疗现在正以强势的姿态颠覆以往的肿瘤诊疗规范,紧随其后的是比免疫治疗更成熟的靶向治疗。目前肺癌的靶向治疗已经相当成熟,吉非替尼、奥希替尼、克唑替尼等靶向药物已经给EGFR和ALK突变的非小细胞肺癌患者带来了福音。在转移性结直肠癌(mCRC)领域,靶向治疗仍有待突破,但也取得了许多令人振奋的进展。本文主要讨论目前mCRC患者的预测生物标志物及其相关的靶向治疗药物。
RAS/RAF 野生型和抗 EGFR mAb
表皮生长因子受体(EGFR)是一种参与细胞信号转导的酪氨酸激酶受体,在许多实体瘤中高表达或异常表达。抗 EGFR mAbs 通过与 EGFR 蛋白的细胞内或细胞外结构域结合来抑制信号转导,从而阻止细胞增殖并导致细胞凋亡。RAS基因位于EGFR下游,KRAS和NRAS突变提示CRC患者不能从抗EGFR单克隆抗体的使用中获益。
西妥昔单抗是一种抗 EGFR 单克隆抗体,可显着改善具有野生型 RAS 和 BRAF 的 mCRC 患者的生存率。近年来,许多回顾性研究表明,西妥昔单抗的疗效与部位显着相关。左侧结直肠癌化疗联合西妥昔单抗在客观缓解率(ORR)和总缓解率方面优于化疗联合贝伐单抗。生存(OS)有一定的优势。对于右侧结直肠癌,化疗联合西妥昔单抗在 ORR 上可能有一定优势,但在 OS 上不如贝伐单抗。在一项 3 期研究中,另一种抗 EGFR mAb 与西妥昔单抗的头对头比较显示不劣于西妥昔单抗 [1]。
BRAF 突变和 BRAF 抑制剂
BRAF是重要的原癌基因之一,是RAS-RAF-MEK-ERK信号通路(MAPK/ERK通路)的一部分。绝大多数突变为BRAF突变,导致下游MEK-ERK信号通路持续激活,促进肿瘤增殖和侵袭。BRAF突变见于约8-10%的,临床病理特征更倾向于高龄、女性、右侧、低分化粘液腺癌、常见腹膜及远处淋巴结转移、预后不良[2 ]。
BRAF抑制剂威罗非尼对突变型恶性黑色素瘤疗效显着,值得推荐,但单药威罗非尼在mCRC患者中的效果并不理想,联合治疗逐渐兴起。SWOG 随机研究评估了西妥昔单抗联合伊立替康 ± 威罗非尼在 BRAF 突变 mCRC 中的益处,结果显示,加用威罗非尼改善了无进展生存期 (PFS) 的主要终点(风险比 [HR] =0.50, P=0.001)[3].基于这项研究,CSCO指南推荐西妥昔单抗+伊立替康±威罗非尼用于基因型/BRAF突变的mCRC患者的野生型RAS二线及以上治疗.
基于研究 - 一项旨在评估西妥昔单抗与 BRAF 抑制剂卡纳替尼 () 与或不与 MEK 抑制剂比美替尼 () 与常规二线或三线化疗相比的疗效和安全性的研究 根据研究数据 [4], 2021 CSCO指南推荐BRAF抑制剂+西妥昔单抗±MEK抑制剂用于RAS野生/BRAF突变的mCRC患者的二线或以上治疗。此外,基于小样本研究,BRAF抑制剂达拉非尼+西妥昔单抗+MEK抑制剂曲美替尼也被推荐用于BRAF突变mCRC患者的后线治疗。
RAS突变和靶向RAS突变的药物
大约 50% 的 mCRC 有 KRAS/NRAS 突变,这些肿瘤预后不良,从西妥昔单抗等药物中获益甚少,使其治疗更具挑战性。AMG-510是全球首个KRAS靶向药物,特异性靶向KRAS G12C突变亚型,具有高选择性。在第一项在 KRAS G12C 突变的 mCRC 患者中评估 AMG 510 的临床研究(研究)中,ORR 为 7.1%(3/42),疾病控制率(DCR)为 76.@ >2% (32/42)。这款药物的问世打破了KRAS突变肿瘤无药可用的尴尬局面,但还有很长的路要走。
MSI 和免疫检查点抑制剂
免疫检查抑制剂 (ICIs) 疗法已在 dMMR(错配修复蛋白缺陷)/MSI-H(高度微卫星不稳定性)mCRC 患者中得到很好的证实,是预测其疗效的主要生物标志物之一。NCCN 和 CSCO 指南建议对所有 II 期 CRC 进行 MMR 和 MSI 检测,而 dMMR 或 MSI-H 的 II 期患者可能有更好的预后,并且不能从单药氟尿嘧啶的辅助化疗中获益。
-142研究旨在评估单独使用纳武单抗或纳武单抗联合易普利姆玛治疗dMMR/MSI-H mCRC患者的疗效。纳武利尤单抗单药治疗组中位随访 21 个月的数据显示,ORR 为 34%,DCR 为 62%,12 个月时 PFS 为 44%,12 个月时 OS 为 72%。双免疫组中位随访 25.4 个月的结果显示,ORR 为 58%,DCR 高达 81%,12 个月 PFS 为 71%, 12 个月的 OS 为 85% [5]。根据本研究结果,纳武利尤单抗单药和联合方案获得 FDA 批准用于 MSI-H/dMMR mCRC 的二线治疗。
-177 是一项 III 期临床研究,旨在评估派姆单抗单药治疗与标准化疗在 MSI-H/dMMR mCRC 一线治疗中的比较。结果显示,一线派姆单抗单药治疗的中位 PFS 是化疗组的 2 倍(16.@>5 个月 vs 8.2 个月;HR=0.60 ;95%CI :0.45~0.80;P=0.0002),ORR增加10.7%[6]。基于结果在这项研究中,CSCO 指南推荐将派姆单抗用于 dMMR/MSI-H mCRC 患者的一线治疗。
HER2和抗HER2靶向药物
常规推荐 HER2 检测并与晚期胃癌的预后相关,但在 mCRC 中仍存在争议。越来越多的证据支持 HER2 扩增或过表达作为抗 EGFR 靶向治疗耐药的预测因子。提供了曲妥珠单抗联合拉帕替尼、曲妥珠单抗联合帕妥珠单抗和曲妥珠单抗联合在 A 期和 II 期临床研究中的数据,用于 mCRC 证据中的抗 HER2 治疗。基于以上数据,目前正在进行一项比较曲妥珠单抗联合帕妥珠单抗和伊立替康联合西妥昔单抗治疗HER2扩增的mCRC患者的随机II期临床试验,我们将拭目以待。
NTRK 融合和 NTRK 抑制剂
NTRK基因融合是近年来的热门明星靶点。对于NTRK阳性实体瘤患者,NTRK抑制剂治疗的总体ORR为75%,其中完全缓解(CR)率达到22%;处理率为 57.4%。脑转移患者颅内ORR为54.5%。NTRK 融合在结直肠癌中很少见,发生率 0.35%。NTRK 抑制剂为标准治疗失败的患者提供了额外的治疗机会。中的疗效数据有待进一步探索。
参考:
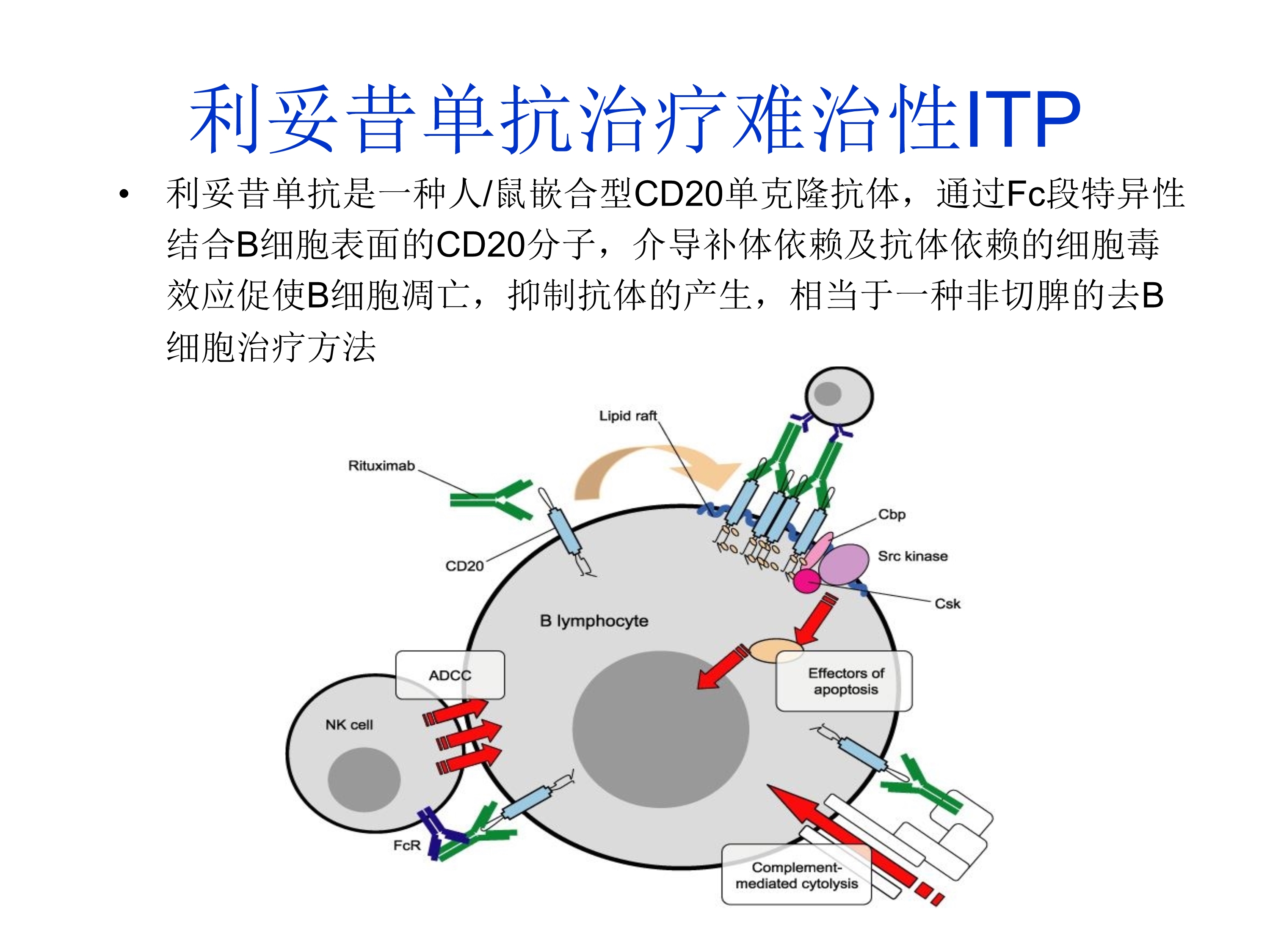
1. el K、SJ、DE、M、H:它在 和 中的作用。细胞科学杂志 2011, 124(Pt 13):2175-2186.@>
2. R, T, JF, R, T:代表 . 2020, 12(9).
3. S、KA、VK、Lenz HJ、AM、Maru D、Yan Y、R、G、Hong DS 等人:BRAF- (SWOG) 的和 With or in。临床杂志 2021, 39(4):285-294.
4. F、S、C、Kasi PM: 和 () 用于 BRAF - 。(巴克) 2019, 55(11):683-693.
5. MJ, R, JL, S, Lenz HJ, MA, J, Hill A, M, Moss RA 等人:在 DNA 中 - 或 -high ( 142): 一个开-, , 2. 2017, 18(9):1182-1191.
6.@> T、Shiu KK、Kim TW、BV、LH、Punt C、D、-R、M、P 等人:在 --High 中。N Engl J Med 2020, 383(23) :2207-2218.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话