欢迎光临吉康旅!
中华肿瘤外科杂志,2014年12月,卷。 6, No. 6 Chin J Surg Onco,。 2014, Vo1.6, No. 6.345. .贝伐单抗联合一线化疗治疗晚期转移性结直肠癌的临床观察。高文,刘令祥,朱伟友,徐静,舒永干 基金项目:国家自然科学基金(N0,);江苏省六大人才高峰(No.WSN-032)作者单位:江苏省南京市南京医科大学第一附属医院肿瘤科第一作者:高文,女,博士,主治医师、讲师,研究方向:肿瘤个体化诊疗,E-mail:@126.corn 通讯作者:舒永干,男,博士,主任医师,教授,博士生导师,研究方向:肿瘤个体化诊疗, E-mail:@ 【摘要】 目的观察贝伐单抗联合一线化疗治疗晚期结直肠癌( , mCRC)的疗效和副作用。贝伐单抗与一线化疗。与化疗药物联合治疗。
贝伐单抗的给药剂量为每 2 周 5 mg/kg,或每 3 周 7.5 mg/kg。一线化疗方案:18例联合基于L-OHP的方案(方案或方案),12例联合CPT。 11是主程序()。评价疗效和不良反应,并随访生存信息。结果 30例无CR患者中,PR 15例(50.0%),SD 10例(33.3%),PD 5例(16.7%);客观缓解率为50.0%,疾病控制率为83. .3%;中位无进展生存时间为10.809个月(95%CI:4.079-15.921)。与贝伐单抗相关的主要不良反应为高血压3例,鼻出血1例,蛋白尿1例。其他2例出现血液学毒性,考虑与化疗有关;接受CPT-11方案的患者中,4例出现迟发性腹泻,但上述副作用较轻,均在对症治疗后治疗. 可缓解,不影响治疗。 【关键词】 转移性结直肠癌;贝伐单抗;一线化疗 05 wjth chem for the -line on wjth al GAO Wen, LIU, ZHU, XU ring, SHU .(— 肉, The A f i o, ,) by th e 的 (No. 81);六—试试(号.WSN-032):SHU,E-mail:@:to the e f and of plus for the—line on with (mCRC). 30 pa—with mCRC L-0HP on ( or )( =18) or CPT-1 1 on ()(a=12)plus.was with 5 rag/kg 2 , or 7.5 mg/kg 3. of 是 , 和 tox- 同时是 . 的时间也是 . 数据是 - . 15 of 30 had and 10 got and 5 pa- got . 比率是 50% 和比率是 83.3% .中位数自由 sur (PFS) 为 10.809 (95%CI: 4.079~15.921)。to 分别为 3、1、1 .2 suf-from 和 4.·346·中文 of , 2014, 6, 6, Cbin J Su Li 0nc0. 2014 Vo1. 6. No. 6 with is and the is well to, be used as the —line for with mCRC. : ; ; — line 结直肠癌是世界上常见的恶性肿瘤,近年来在我国发病率逐渐上升。
约25%的新诊断结直肠癌患者为转移性结直肠癌(mCRC),约30%的早期结直肠癌患者术后可能出现复发和转移。以化疗为主的综合治疗是目前转移性结直肠癌的主要治疗方法。其中,一线化疗方案主要是氟尿嘧啶(f)联合奥沙利铂(,L-OHP)或伊立替康(.,CPT-11))。喜昔单抗或贝伐单抗联合一线化疗对mCRC的疗效有益,贝伐单抗是一种针对血管内皮生长因子(VEGF)的重组人源化单克隆抗体,已经进行了多项重大研究,临床样本研究证实了其明确的疗效。对包括晚期结直肠癌在内的多种实体瘤的疗效,因此美国国家综合癌症网络(NCCN)指南推荐贝伐单抗联合治疗作为转移性结直肠癌的一线治疗方案¨。本研究回顾性分析了贝伐单抗联合一线化疗30例mCRC患者,在验证疗效的基础上进一步探索其可能的靶点和安全性,作为研究方向的下一步。

1 资料与方法 1.1 病例选择 2012年1月至2013年12月在我科接受初步治疗的30例mCRC患者符合以下标准:(1)组织病理学证实的mCRC(TNM分期为IV),包括新诊断mCRC和术后复发转移的患者;(2)有可测量的病灶,可以通过CT或MRI等影像学客观评估;(3)患者的生活质量PS评分(ECOG)为0至2分表示可以耐受全身化疗。(4)预计生存时间>3个月,肝肾功能及血常规基本正常;(5)排除术后接受贝伐单抗联合一线化疗)以下情况:①4周内接受过手术或预计接受手术的患者;②有脑转移;③有血栓形成或出血性疾病;④正在服用抗凝或抗血小板聚集药物⑤联合使用完全或不完全性肠梗阻、活动性肠炎或炎症性肠病。患者具体情况见表1。 1.2 治疗方法贝伐单抗(商品名:, ,规格100 mg/4 ml)联合一线化疗。贝伐单抗的剂量为 NCCN 指南推荐的 5 mg/kg,每 2 周重复一次,或 7.5 mg/kg,每 3 周重复一次。联合化疗方案:18例联合L-OHP方案(方案或30例mCRC患者一般情况见表1),12例联合CPT-11方案(RI方案)。
详情如下:(1):奥沙利铂85mg/m静脉滴注d1+亚叶酸/m静脉滴注+5.fu /m静脉推注,连续泵送5.fu 600r ag/m,22 h dl~2,每2周一次。(2):奥沙利铂130 mg/m,静脉滴注d1 10 卡培他滨1 000 mg/m,口服,每天2次,共14天,21天(3)方案:伊立替康(CVF-11)180 mg/m 静脉输注 d1+CF 200 mg/in 静脉输注 d1 ~2+5-Fu 400 mg/m 静脉推注)注射,连续泵 5-Fu 600 mg/m 22 h dl~2,每 2 周一次。一线方案根据指南选择,结合患者一般情况、基础疾病、潜在耐受性或毒副作用预测制定疗效、预期疗效、依从性、社会经济状况。所有化疗均常规治疗,防止呕吐。常规、生化、心电图等,上述指标在治疗期间定期复查。他期。 30例患者共接受249个周期的治疗,平均每例患者8.3个周期。对于2周方案的患者,至少4个周期的治疗进行疗效评价(只有1例患者在2个周期后出现明显的进展症状。经影像学证实后,改变处方。中华肿瘤外科杂志,第 6 卷第 6 期,2014 年 12 月,Chin J Surg Onco,.2014,Vo1.6,No.6 Case ),对于 3 周方案,将使用至少 2 个周期的治疗来评估疗效。
1.3 观察指标疗效按照实体瘤疗效评价标准()进行评价。完全缓解(CR):所有靶病灶消失;部分缓解(PR):基线时病灶长度和直径总和减少≥30%; PD;疾病进展(PD):基线病灶长径总和增加>20%或出现新病灶。治疗过程中详细记录病灶的变化。客观缓解率(ORR)为CR+PR(%),疾病控制率(DCR)为CR+PR+SD(%)。无进展生存期 (PFS):从开始治疗到观察到疾病进展或任何原因导致的死亡之间的时期,随访至 2014 年 10 月 1 日。毒性和副作用根据美国国家癌症研究所的 毒性时间(NCI-CTC 3.0版),分为0-IV度,每个周期评估毒副作用。 1.4 统计处理采用SPSS 17.0统计软件对数据进行统计分析。组间采样率比较临床观察指标(ORR和DCR)的比较采用双边卡方检验,P<0.05认为有统计学意义。
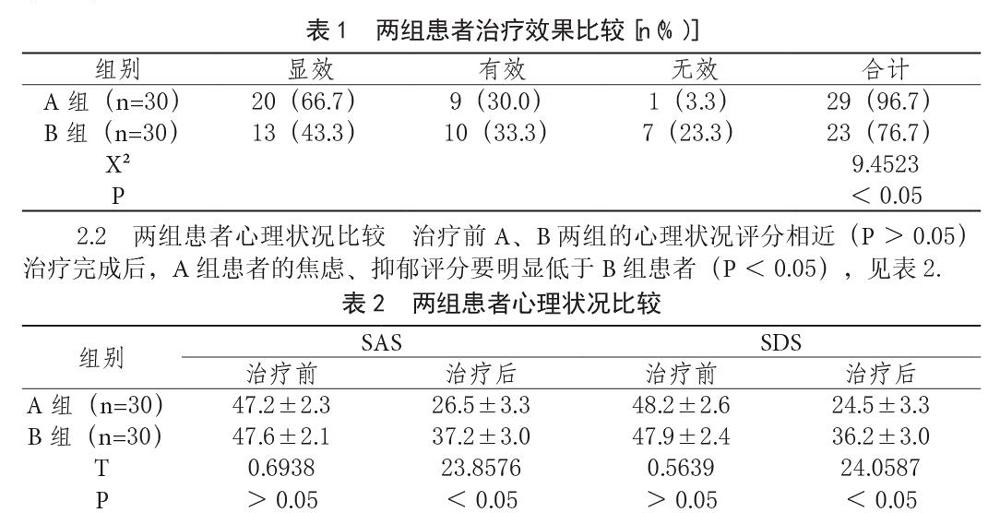
PFS采用-法计算并绘制生存曲线,中位PFS由生命表求得。 2 结果 2.1 疗效评价 所有患者均得到完全随访,死亡2例,死因为肿瘤进展,与药物副作用无关,其余28例存活至今。 30例患者均至少接受2个周期的治疗,最多接受14个周期的治疗,可评价临床疗效。 30例无CR患者中,PR 15例(50.0%),SD 10例(33.3%),PD 5例(16.7%),ORR为50.0%,DCR为83.3%。具体疗效见表2。经卡方检验,贝伐单抗联合3种不同化疗方案的ORR和DCR差异无统计学意义(P>0.05)。患者基本临床参数(包括性别、年龄、病理)ORR与DCR的相关性无显着差异(P>0.05)。PFS为10.809个月(95%CI:4.079-15.92<@)。1)(图1). 表 2 贝伐单抗联合化疗治疗晚期结直肠癌的近期疗效 · 347 · PFS 10.809 个月 图 1 30 例 mCRC 患者的无进展生存期(—曲线) 2.2 安全性观察 总体患者,观察到的副作用较轻,主要包括胃肠道反应和血液学副作用。
胃肠道反应主要是恶心和呕吐。 4例患者联合CPT-1 1方案出现迟发性腹泻,多为Ⅰ~Ⅱ级,经对症治疗后好转;观察2例I-II级肝功能损害。 ,经过保肝治疗,转氨酶恢复正常;骨髓抑制主要表现为粒细胞和(或)血小板减少,多为Ⅰ~Ⅱ级,其中Ⅳ级骨髓抑制仅2例。恢复正常,未因粒细胞缺乏而死亡。贝伐单抗相关不良反应主要为:3例血压升高,其中1例血压一度达到210/100 mmHg,经降压等对症治疗后恢复正常; 1 例患者出现蛋白尿,1 例患者出现鼻出血。未观察到动静脉血栓形成、胃肠道穿孔和严重出血事件(致死性脑出血、肺出血和胃肠道出血),也没有因对治疗不耐受而终止贝伐单抗治疗的事件。 3 讨论 全身化疗是mCRC患者综合治疗的主要手段。一线标准治疗主要包括5-Fu及其衍生物、第三代铂类和拓扑异构酶I抑制剂。传统化疗方案以5 Fu为基础,其治疗的中位生存期为12个月左右; L. OHP 或 CPT-11 为基础的联合化疗比传统的 5. Fu 治疗显着提高了短期有效率,延长了疾病进展时间,并将 mCRC 患者的中位生存时间从 12 个月提高到 18 个月-21 个月。
随着基于分子靶向的个体化治疗的出现,新型分子靶向治疗药物的临床应用为mCRC患者带来了更多光明。目前一线治疗引入的靶向药物主要有贝伐单抗和西妥昔单抗。肿瘤血管生成是肿瘤发生、发展的基础,而VEGF是促进肿瘤血管生成的重要因素。近年来,抗血管生成的基础和临床研究已成为肿瘤个体化诊疗的新领域。目前的研究表明,VEGF在多种大肠癌细胞中高表达,临床研究也发现VEGF存在于50%~80%的大肠癌组织中。苏兹昂科,。 2014, Vol 6, No. 6 VEGF高表达预示预后不良。体外和体内实验表明,VEGF的高表达与肿瘤细胞的侵袭和转移有关。因此,VEGF已成为结直肠癌抗血管生成治疗的重要靶点。贝伐单抗是一种重组人源化、人鼠嵌合抗 VEGF 单克隆抗体,可识别和抑制人源化 VEGF 的所有主要同种型。作用机制是阻断VEGF,阻断其与血管内皮细胞表面受体(如FLT-1和KDR等)的结合,从而阻止肿瘤血管生成,抑制肿瘤生长和延长转移。
目前的研究表明,化疗的局限性也与肿瘤血管结构的缺陷有关,导致肿瘤血管通透性增加,间质压力升高,从而降低细胞毒药物在肿瘤中的作用,但贝伐单抗可以改善肿瘤微血管结构,降低血管密度,提高血管通透性,使肿瘤血管正常化,通过与VEGF的特异性结合,增加肿瘤细胞对化疗药物的摄取,从而提高化疗疗效。 J.基于贝伐单抗的第一个III期临床研究结果,贝伐单抗是FDA批准用于治疗mCRC的第一个肿瘤血管生成抑制剂。本研究表明贝伐单抗联合IFL方案可显着提高治疗有效率(44.8% vs. 34.8%),延长TFP(10.4个月vs.7.1个月)、PFS(10、6个月vs. 6.2个月) ),中位生存期延长了 4.7 个月(20.3 个月对 15.6 个月)。贝伐单抗组还将死亡风险降低了 34%”。后续研究继续分析贝伐单抗联合奥沙利铂为主的方案,1 401例mCRC患者随机接受一线贝伐单抗单克隆抗体或安慰剂联合X...
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话