欢迎光临吉康旅!
肝癌靶向药,肝癌靶向治疗,肝癌靶向药,又一晚期肝癌靶向药获批!
中国肝癌概况
我国是肝癌大国,严重危害人民群众身体健康。据中国癌症统计(延迟3~4年),估计2015年肝癌新发病例46.60,000例,肝癌死亡42.20,000例。我的国家。第三大死因。世界上近一半的肝癌患者在中国,因此有人称肝癌为“中国癌症”。
近年来,肝癌治疗领域取得了许多突破,特别是在靶向治疗和免疫治疗方面。许多新药为无数癌症患者带来了“新生命”,显着提高了他们的生存率。.
晚期肝癌靶向药物获批
2019年5月10日,美国食品药品监督管理局批准(雷莫芦单抗)用于既往接受过索拉非尼(多吉美)(HCC)单药治疗的甲胎蛋白(AFP)≥/ML的肝细胞癌患者。
因此,雷莫芦单抗成为第一个在生物标志物选择的 HCC 人群中具有临床益处的药物。
该批准基于一项国际双盲、安慰剂对照、多中心 III-2 期试验的结果,该试验由美国马萨诸塞州总医院著名肝癌专家朱秀轩教授领导,作为该研究对晚期肝癌患者的影响意义重大,此前发表在重量级杂志《柳叶刀》上。( . 网络版 2019 年 1 月 18 日)
首先,该试验招募了所有在索拉非尼治疗后出现晚期或不耐受的晚期患者。可以说,这个阶段的患者几乎没有好的治疗选择。
-2 研究达到了其主要终点,显示在先前接受索拉非尼治疗的甲胎蛋白 (AFP) 浓度至少为 400 ng/ml 的 HCC 患者中,与安慰剂相比, 使用 mAb 改善了总体生存期。 耐受性良好,安全性可控。雷莫芦单抗治疗所有亚组的无进展生存期结局更好。-2是第一个在选择生物标志物的肝细胞癌患者群体中进行的阳性 III 期试验。
甲胎蛋白浓度升高的晚期肝细胞癌患者预后较差。在之前的一项研究中,与安慰剂相比,雷莫芦单抗在接受索拉非尼一线治疗的晚期肝细胞癌患者中并未改善意向治疗人群的总生存期,但在基线 AFP ≥ 400 ng/ ml 亚组患者。-2 研究包括 AFP ≥ 400 ng/ml 的晚期肝细胞癌患者,这些患者之前仅接受过拉非尼单线治疗,以评估雷莫芦单抗在此类患者中的疗效和安全性。研究在 20 个国家的 92 家医院、诊所和医疗中心进行。
从 2015 年 7 月 26 日至 2017 年 8 月 30 日,共有 292 名患者被随机分组,其中雷莫芦单抗组 197 人,安慰剂组 95 人。在中位随访 7.6 个月时, 组的中位 OS 显着长于安慰剂组,分别为 8.5 个月和 7.3 个月;亚组分析显示,除女性患者组(雷莫芦单抗组 43 人,安慰剂组 16 人)外,雷莫芦单抗组所有其他亚组的总体生存结果均更好。 组的无进展生存期也明显优于安慰剂组,分别为 2.8 个月和 1.6 个月。
雷莫芦单抗简介
【英文名】
【适应症】胃癌、肺癌、大肠癌、食道癌、肝癌等。
【目标】
【研发公司】礼来(美国)
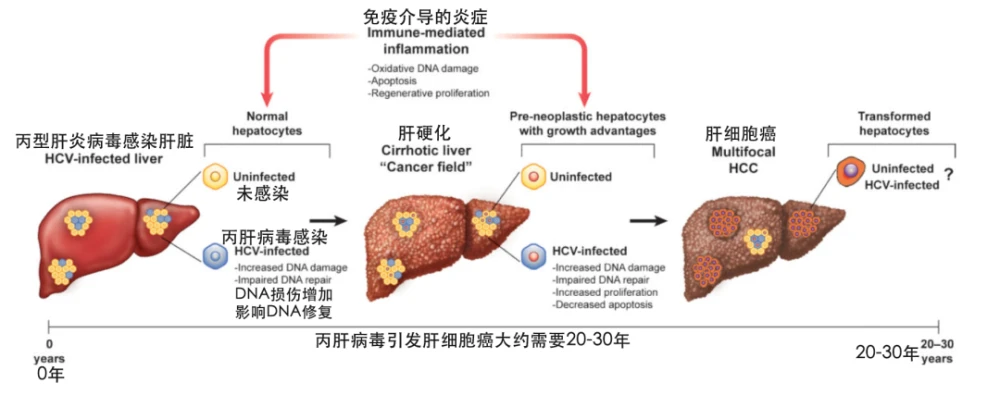
雷莫芦单抗是一种靶向血管内皮生长因子受体2()的单克隆抗体,于2014年4月21日获得FDA批准,与化疗药物联合用于治疗胃癌或胃食管结合部腺癌、转移性非小细胞肺癌和结直肠癌,2015 年销售额为 3.84 亿美元。
肝癌治疗进入新时代!
几年前,索拉非尼是唯一获得 FDA 批准的可用于晚期肝癌患者一线治疗的药物。在其他药物多次试验失败后,乐伐替尼终于在2018年来到一线治疗,并在III期试验中显示出比索拉非尼更好的临床效果。
过去肝癌的二线治疗没有标准的治疗方案,现在FDA已经批准了两种酪氨酸激酶抑制剂瑞戈非尼([])和最近批准的卡博替尼[],以及两个免疫检测点抑制剂。获批的还有纳武利尤单抗( , )和派姆单抗( , )。此外,期待已久的雷莫芦单抗( )终于被正式批准为二线治疗药物。
全球肿瘤学家网提醒患者,国内细胞免疫治疗技术,包括cart细胞、树突状细胞疫苗、NK细胞、TILs细胞、TCR t细胞疗法、癌症疫苗等,均处于临床试验阶段,尚未获批在中国正式使用。医院。国内患者可参加正规临床试验,并在医生监督下使用。全球肿瘤学家网络不建议患者贸然尝试任何医疗机构和研发机构进行有偿治疗。
本网站的新闻、文章、研究数据、治疗案例均来自国内外医学论文。涉及的新药、新技术可能仍处于临床研究阶段,不能以患者作为治疗疾病的依据。目前癌症治疗尚无治愈方法,患者需要在医院接受正规治疗或在医生指导下参与新药新技术的临床试验。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话