欢迎光临吉康旅!
神经肿瘤学周刊
神外边疆
神外前沿-协和神经肿瘤学周报,胶质母细胞瘤(GBM)是成人最常见的原发性恶性脑肿瘤,恶性程度高,5年生存率不到10%。尽管目前的治疗标准包括最大手术切除、放疗和替莫唑胺化疗,但大多数患者会出现肿瘤复发。同时,目前没有证据表明存在延长复发性胶质母细胞瘤患者生存期的疗法。虽然贝伐单抗作用于 VEGF 并抑制肿瘤血管生成,已被 FDA 批准用于治疗复发性胶质母细胞瘤,但对延长生存期没有明显作用。
近期,同样针对纳武利尤单抗的III期临床试验( 143 III)结果于2020年5月发表在JAMA上。第一作者和通讯作者均为达纳癌症研究所教授。本试验比较了纳武利尤单抗与贝伐单抗在复发性 GBM 患者中的生存获益和安全性。
在本次临床试验中,主要终点为总生存期(OS),次要终点包括12个月生存期(OS-12)、总缓解率(ORR)、无进展生存期(PFS)。遗憾的是,这项III期临床试验没有达到其主要终点,两组的中位生存期(mOS)无统计学差异。与2017年试验结果相比,本次发表的新亚组分析部分增加了官方结果显示,MGMT 启动子甲基化阳性的患者和未使用糖皮质激素的患者最有可能从免疫检查点抑制剂治疗中获益。亚组分析假设可能有一些特定的患者可能会从免疫治疗中获益。
编译器
胶质母细胞瘤恶性程度高,复发率较高,因此,复发性胶质母细胞瘤的治疗相关研究意义重大,已成为当前的研究热点。目前临床研究较多,对其他肿瘤有效的免疫检查点抑制剂治疗也适用于复发性胶质母细胞瘤。热量很高。这项 PD-1 抑制剂的 III 期临床研究是在 I 期临床试验成功后启动的,但在主要和次要终点分析中均未产生有利于实验药物的结果。本研究还进行了亚组分析,提示未接受糖皮质激素治疗的患者和MGMT启动子甲基化阳性患者可能受益于免疫检查点抑制剂治疗。
虽然143个III期临床试验虽然没有取得令人满意的结果,但这项研究对神经肿瘤领域免疫治疗的进一步发展具有重要意义,同时也提示我们治疗的时机、顺序或组合药物可能会影响免疫检查点抑制剂的疗效。研究表明,新辅助 PD-1 抑制剂和主动免疫联合免疫检查点抑制剂可能会产生令人鼓舞的结果。 2019年发表的研究表明,新辅助PD-1抑制剂可能为复发性GBM患者提供生存益处,同时临床前模型表明PD-1抑制剂在诱导的T细胞活化状态下可以达到更好的治疗效果。以上两种方法都是为了刺激整个肿瘤的免疫反应,使胶水免疫活性低,属于“冷肿瘤”。浆母细胞瘤转化为“热肿瘤”,从而使免疫治疗变得更好。免疫治疗在胶质母细胞瘤中的作用仍有待进一步研究。
方法
本研究是一项随机、开放标签、多中心的 III 期临床研究。患者纳入标准包括年龄≥18岁、KPS大于70、经组织学证实的WHO IV级复发性GBM或胶质肉瘤(RANO),标准判断为一线治疗为放疗和替莫唑胺化疗),最后一次手术超过28天,最后一次放疗超过12周。多于1次复发的GBM患者和继发性GBM患者可能需要不断增加糖皮质激素的剂量以控制脑水肿患者无法入组。入组患者以 1:1 的比例随机分配 在纳武单抗治疗组和贝伐单抗治疗组中,纳武单抗治疗组中的 184 名患者每 2 周接受 3 mg/kg 纳武单抗静脉注射,贝伐单抗治疗组中有 185 名患者接受静脉注射。治疗组每 2 周接受一次纳武单抗治疗。周接受贝伐单抗 10 mg/kg 静脉注射,通过常规增强 MRI 检查确定肿瘤反应和进展(图 1)。
图1 临床试验流程图
从统计学上讲,使用双边对数秩检验来比较治疗组之间的 OS。各组患者生存情况采用-法评估,风险比HR采用Cox比例风险模型估计。使用SAS统计软件(9.2版)进行统计分析。
结果
共入组369例患者,其中纳武单抗组184例,贝伐单抗组185例,纳武单抗+贝伐单抗抗治疗组中位随访时间为9.8个月和9.4 个月。纳武利尤单抗治疗组mOS为9.8个月,贝伐单抗治疗组为10.0个月,两组的中位生存期差异无统计学意义。次要终点方面,纳武利尤单抗治疗组的PFS显着低于贝伐单抗治疗组,分别1.5个月和3.5个月,ORR高于纳武利尤单抗贝伐单抗组和贝伐单抗组分别为 7.8% 和 23.1%(图 2)。
图 2 PFS,OS 曲线。
A:总生存期(OS); B:无进展生存期(PFS)
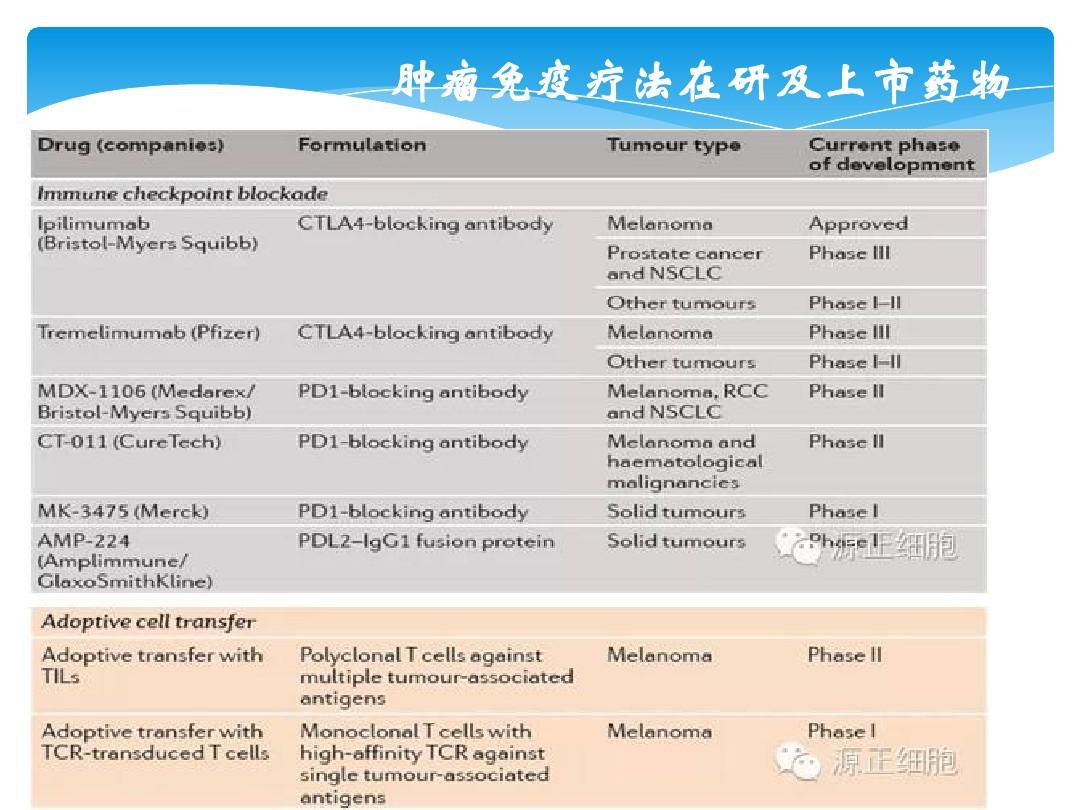
在亚组分析方面,研究主要分析了MGMT启动子甲基化和糖皮质激素使用对生存的影响。关于糖皮质激素的使用,在 组中,没有使用糖皮质激素与较长的 mOS 相关,而在 组中,在 组中,使用糖皮质激素对患者的预后没有显着影响。这种现象可能是由于糖皮质激素对T细胞功能的直接作用,可能会抑制免疫系统的激活,从而导致免疫治疗效果不佳。 , 需要糖皮质激素治疗的患者往往病情进展迅速,可能没有足够的时间从免疫治疗中受益。
在MGMT启动子甲基化方面,两组MGMT启动子甲基化阳性的患者mOS均较长。总之,在接受纳武利尤单抗治疗的患者中,MGMT 启动子甲基化阳性且未应用糖皮质激素的患者预后较好(图 3)。
图 3 亚组分析 PFS、OS 曲线。
A:纳武利尤单抗治疗组; B:贝伐单抗治疗组 反应发生率和严重程度与贝伐单抗治疗组无显着差异。
总结
143 III 期临床试验是第一个研究免疫检查点抑制剂对原发性脑肿瘤疗效的随机 III 期临床试验。该研究未达到预设的 OS 主要终点,纳武单抗和贝伐单抗治疗组的 OS 差异无统计学意义,贝伐单抗组患者的 PFS 和 ORR 优于纳武单抗组。同时,亚组分析表明,未使用糖皮质激素和MGMT启动子甲基化阳性是接受纳武利尤单抗患者的预后因素,具有这些特征的患者更有可能从免疫检查点抑制剂治疗中获益。
该临床试验有一定的局限性。首先,亚组分析的患者样本量相对较小。其次,复发性GBM与相应的原发性GBM在分子病理学上存在一定差异,本研究将初诊时采集的组织用于生物标志物的分子病理学测定,未进行二次活检。同时,本试验的主要终点是OS,患者的肿瘤切除程度和进展后不同后续治疗方案的选择可能会影响OS结果的准确性。由于本研究是第一个研究免疫检查点抑制剂对复发性GBM疗效的III期临床研究,而且开展的时间相对较早,因此使用RANO标准而非影像学评估标准也可能导致纳武单抗的测量抗耐药组患者的PFS值低于真实值,而贝伐单抗组患者实测PFS值在一定程度上高于真实值,对准确度有一定影响评估。
总之,本研究未能证明 PD-1 抑制剂对复发性 GBM 的疗效,并提示未使用糖皮质激素的患者和 MGMT 启动子甲基化阳性患者可能会接受免疫检查点抑制。受益于治疗。然而,最近发表的研究表明,新辅助PD-1抑制剂和主动免疫联合免疫检查点抑制剂可能会取得令人兴奋的结果,免疫疗法在胶质母细胞瘤中刺激肿瘤免疫进而杀死肿瘤的作用仍然存在。值得继续研究。
本期作者
陈文林,北京协和医院神经外科2014级博士生,北京协和医院临床医学8年制
本期主编
王宇副教授,北京协和医院神经外科副主任医师,医学博士,美国博士后
联系我们
北京协和医院神经外科恶性肿瘤专科就诊时间:
马文斌主任医师周四上午特诊。
王宇副主任医师周四下午特需门诊。
(建议想咨询治疗方案或参加临床试验咨询的患者选择以上门诊时间进行面诊。)
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话