欢迎光临吉康旅!
电影《我不是药神》中有老太太和警察的对话,“我不想死,我想活”。这句话表达了癌症患者对生命的渴望。正是这种无奈和苦涩,才把靶向药物当成了唯一的救命稻草。
的确,靶向药物的出现给癌症患者带来了新的希望。此类药物针对癌细胞的特定目标,例如某些独特的基因突变。
这种疗法针对病变细胞。与传统的放化疗相比,它可以区分“敌我”,高效选择性杀伤肿瘤细胞,减少对正常组织的损伤。毒性较小。如果把“杀敌千人,自毁八百”的化疗方式比作“地毯式轰炸”,那么靶向治疗就是精准制导的“远程导弹”!
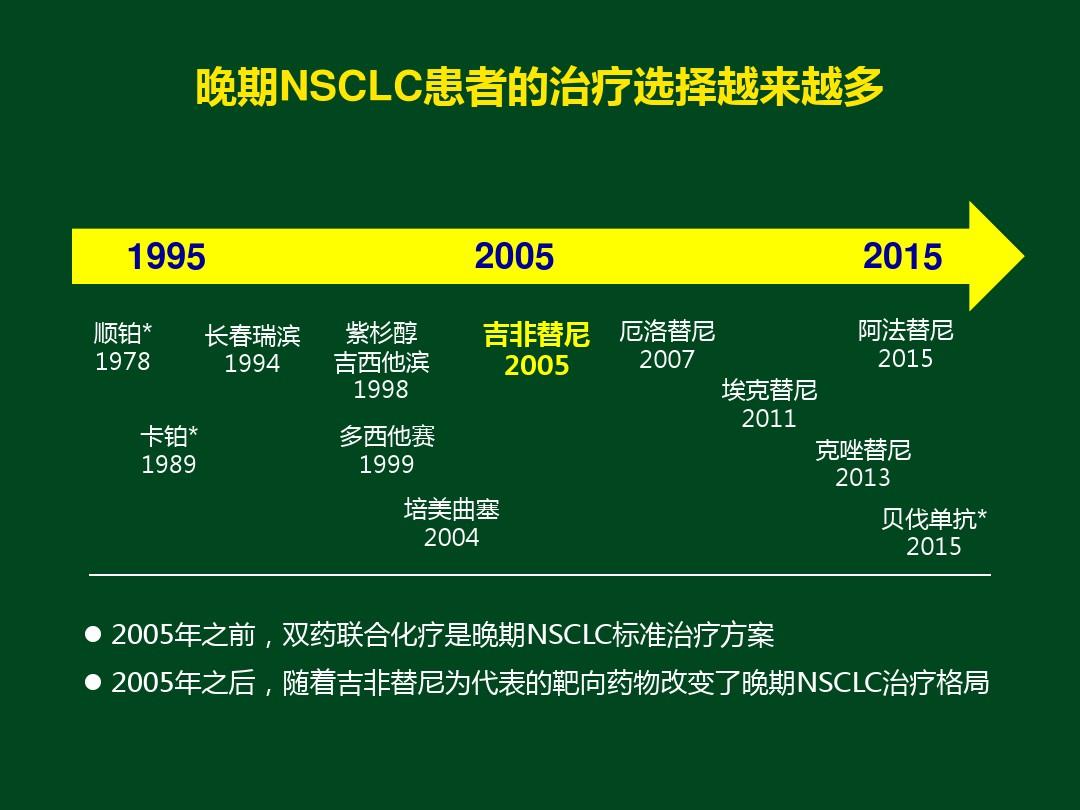
2005年是靶向药物进入中国的元年。自易瑞沙(吉非替尼)进入中国市场以来,中国晚期肺癌患者的中位生存时间在过去十年显着增加。 2.4 次,从之前的 14.1 个月到 33.5 个月,5 年生存率从 8% 提高到 18%,也是翻倍.
更大的进步是靶向药物的副作用远小于化疗,疗效远优于化疗。在提高患者生存期的同时,也可以维持生活质量。通俗的讲,化疗是低效高毒的,而靶向药物是高效低毒的。
近来,癌症靶向治疗进展非常迅速,许多高效靶向药物已在国内外获批上市或投入使用。 2021年肺癌、胆管癌等实体瘤的靶向治疗将迎来新一轮关注,包括钻石靶点NTRK、热门靶点EGFR、MET、RET、ROS1、ALK、罕见靶点KRAS、FGFR等.,众多备受癌友关注的靶向药物如雨后春笋般涌现,重新点燃了无数癌友的生命希望。那么,今天来自无癌之家的小编就来盘点一下这些靶点的最新研究。
“钻石”目标 - NTRK
NTRK之所以被称为“钻石”基因,首先是因为它非常罕见。在直肠癌中,只有 1% 到 5% 的患者有这种突变,而一些罕见的癌症,如婴儿纤维肉瘤和分泌性乳腺癌,NTRK 融合的频率高达 90% 到 100%。其次,针对NTRK融合突变的上市药物和在研药物具有显着的临床效果。接受治疗的患者通常起效快。许多晚期患者在使用NTRK抑制剂后获得了重生,NTRK抑制剂如同钻石一样稀有珍贵。
FDA 批准的 NTRK 靶向药物:、
目前全球市场上有两种治疗NTRK融合基因实体瘤的药物。它们是拜耳/LOXO 的 (2018 年 11 月 FDA 批准)和罗氏的 (2019 年 8 月 FDA 批准)。这两种药物代表了癌症治疗从“基于体内癌症的起源”到“基于肿瘤的遗传特征”演进的重要里程碑。
01
拉罗替尼
两年多来,拉罗替尼在多个国家落地开花,今年终于传来喜讯,即将进入中国。
今年5月20日,CDE官网显示,拜耳提交硫酸胶囊在中国上市申请并被受理(受理号:)。这意味着,全球首个不区分肿瘤来源的泛癌靶向药物有望在中国获批。相信在不久的将来,国内的癌症患者将迎来这种“可治愈”的抗癌药。
02
恩曲替尼
2019年8月,FDA加快批准全球第三种广谱“可治愈”抗癌药(恩曲替尼,RXDX-101)上市,用于治疗神经营养性原肌球蛋白受体的成人和儿童患者)激酶 (NTRK) 融合阳性、局部晚期或转移性实体瘤,初始治疗后有进展或未进展的实体瘤患者(跨越 10 种不同的肿瘤类型)接受标准治疗方案,以及 ROS1 阳性非小细胞肺癌患者。非小细胞肺癌)。
03
第二代新药:瑞博替尼
在2019年6月召开的美国临床肿瘤学会(ASCO)年会上,一款横扫ALK/ROS1/NTRK三个靶点(,TPX-000)的靶向新药(,TPX-000) 5) 的数据太棒了。
是美国公司研发的新一代口服多靶点靶向药物,对ALK、ROS1和NTRK有抑制作用,并能克服对其他TKI的多种作用。抗性基因突变可杀死 ROS1、NTRK 和 ALK 阳性实体瘤。
在 2019 年 ASCO 大会上,研究人员发表了其他 ROS1 抑制剂 (TKI) 的最新数据,这些药物在治疗 ROS1 阳性非小细胞肺癌患者中的疗效。
11 例可评价的 ROS1 阳性患者的总体反应率为 82%,颅内反应率为 100%,临床受益率为 100%,超过目前所有靶向药物。有望成为超越市场的明星产品(拉罗替尼,LOXO-101),(,RXDX-101))新一代广谱抗癌明星。
2021年,新一代广谱抗癌药TPX-0005(瑞博替尼)最新数据在世界肺癌大会上亮相,引起巨大轰动,在癌症圈刷屏!在-1的I/II期研究中,针对特定突变的ROS1阳性患者,客观缓解率达到93%,创下新纪录,超越“可治愈系统”。 “抗癌药恩曲替尼或成为下一个抗癌“传奇”!
目前已获得四项FDA特殊审批通道认证。我们期待该药物早日获得更多优秀的临床试验数据并早日上市。
对于中国患者来说,这些美国抗癌“特效药”不再遥远。
04
创新药物:
(DS-,国内代码AB-106)是日本第一三共株式会社研发的创新药。元生物在中国引进创新药并开始II期临床试验。在I期临床试验中在美国和日本中心中,AB-106已显示出良好的潜力。
2021年9月25日,同济大学附属上海肺科医院周才存教授分享了最新的(AB-106)研究,新一代强效二期研究初步结果) (研究)ROS1/NTRK抑制剂治疗ROS1阳性非小细胞肺癌,优秀的数据让在场的所有专家都兴奋不已,期待该药早日上市,给患者带来新的选择和希望。
1.未接受ROS1 TKI治疗组疗效:客观缓解率高达90.5%!
2.克唑替尼治疗失败组疗效:客观缓解率为43.8%!
3.入脑效果强!客观缓解率高达83.3%!
除上述药物外,全球NTRK药物研发如火如荼,为更多患者带来新希望!抗癌之家特意为癌症朋友整理了目前正在招募的NTRK抑制剂信息。希望能给急于求医的患者提供更多的治疗选择!
热门靶点——EGFR
EGFR( ErbB-1 或 HER1)表皮生长因子受体 主要存在于肺腺癌、亚洲人、不吸烟和女性患者中,大约 15% 的白种人和 30-50% 的亚洲人有 EGFR 基因突变。无吸烟史的人群比例高达50%~60%,常见突变位点为19、21外显子,占90%,称为经典突变,其余10%为18、20外显子突变。 .

64% 的患者受益! “双抗体”JNJ-6372突破奥希替尼耐药
根据 2020 年 ESMO 大会的报告,1 期试验显示,在未经治疗且对奥希替尼耐药的 EGFR 突变晚期非小细胞肺癌患者中,联合用药(拉泽替尼)显示出高效和良好的耐受性。
【结果】
在奥希替尼耐药患者中,客观缓解率为36%,临床受益率(CBR)为64%(包括1例完全缓解和15例部分缓解)。
在可评估的 20 名初治患者中,客观缓解率和临床受益率均为 100%。
无癌之家的专家解释说,无论患者是在一线还是二线接受奥希替尼,还是之前接受过治疗,都可以观察到疗效。
2021 年 5 月 22 日,FDA 宣布批准 -vmjw(, JNJ-6372)上市,作为首个获批治疗 EGFR 外显子 20 插入突变成人或成人非小细胞肺癌的治疗方案 ( )。
FDA 还批准了由 Inc. 开发的 CDx 测试作为伴随诊断选项。
疾病控制率100%,我国自主研发的广谱新药JMT-101来了!
2019年,我国自主研发的专门针对EGFR患者的新药JMT-101获批临床试验!并且在2020年ASCO线上会议上,首次公布了该药在晚期大肠癌患者中的试验结果,疾病控制率达到100%,引起轰动。
好消息是,JMT-101治疗多种实体瘤的I期临床试验已陆续启动。其中,一项治疗非小细胞肺癌的Ib期临床试验正在招募患者。
除了以上介绍的新药外,目前正在招募多款国内外明星新药,这意味着国内患者也有机会免费获得这些抗癌药。
01
药物名称:
目标: 和
研发公司:润欣生物
药物介绍:(又名CK-101)是第三代EGFR-TKI,是一种口服不可逆激酶抑制剂,可特异性抑制包括“看门人”突变在内的多种突变亚型,同时具有良好的脑穿透性,对脑转移患者也有很好的治疗效果。
适应症:EGFR突变阳性肺癌的一线或二线治疗
招聘信息(部分):
1、年龄≥18岁,男女不限;
2、ECOG评分0~1,预期寿命≥3个月;
3、EGFR突变阳性(外显子19缺失或合并其他EGFR突变),或既往EGFR-TKI患者显示临床获益(部分缓解或完全缓解,或病情稳定6个月以上) ),不适合手术或放疗的局部晚期或转移性非小细胞肺癌。
02 麦法替尼
药物名称:麦法替尼
目标:,
开发公司:杭州中煤华东
药物介绍:麦法替尼是第二代不可逆EGFR/HER2高效双重抑制剂,具有高活性、高水溶性,对第一代EGFR TKI的耐药性有很好的治疗效果。
适应症:一线(初始治疗)局部晚期或转移性非鳞状非小细胞肺癌
招聘信息(部分):
非鳞状非小细胞肺癌IIIB或IV期复发或初始治疗,无全身治疗
03 V 美替尼
药物名称:福美替尼()
目标:EGFR
开发公司:艾利斯
p>
药物介绍:第三代EGFR抑制剂。 2021年3月获准在中国上市,用于治疗EGFR突变的非小细胞肺癌。中国自主研发的第三代EGFR抑制剂上市!新适应症的临床试验开放!
适应症:EGFR突变阳性肺癌的二线治疗
招聘信息(部分):
ⅢB或Ⅳ期非小细胞肺癌,不适合根治性手术或放疗,已证实有EGFR外显子20插入突变(包括重复突变),一线治疗失败(TAK-788和除外)的患者JMT-101 抗性)。
04马舒特替尼乐美特胶囊
药品名称:马来酸舒替尼胶囊
目标:罕见的 EGFR 突变(和/或)
p>
研发公司:江苏苏中药业股份有限公司
药物介绍:舒特替尼是国内针对罕见EGFR基因突变的靶向药物,与阿法替尼类似。由周才存教授牵头的马来酸舒特替尼胶囊治疗局部晚期或转移性非小细胞肺癌(仅限于非耐药罕见EGFR突变,和/或)的探索性临床研究是目前正在进行中。未公布的试验数据。
适应症:EGFR罕见突变肺癌一线治疗
招聘信息(部分):
有一个或多个突变, , 并且没有突变, 外显子19缺失突变, 外显子20插入突变, 突变。入组前未接受任何表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)抗肿瘤治疗。
热门目标——MET
近年来,对MET抑制剂的研究层出不穷,其中和是研究数据相对较多的三种药物。
®()是全球首个获批用于治疗非小细胞肺癌的c-MET选择性抑制剂,于2020年3月25日在日本首次获批用于MET外显子14的非小细胞肺癌患者跳过突变。 (相关阅读:重磅!全球首个晚期非小细胞肺癌口服MET抑制剂上市!)
®(卡马替尼)于 2020 年 5 月 6 日获得 FDA 批准用于 MET 的具有外显子 14 跳跃突变的成人非小细胞肺癌患者。 (相关阅读: | FDA 今天批准第一个抑制剂 - 推出)
中国首个MET靶向药物西沃替尼上市!
MET外显子14跳跃突变在1%-3%的非小细胞肺癌()中发生,但在肺肉瘤样癌(PSC)中突变率高达3个1.@ >8%。 MET 外显子 14 跳跃突变对铂类化疗的耐药率较高,因此预后较差。赛沃替尼是我国自主研发的高选择性口服MET抑制剂,有望成为我国首个MET靶向药物。没想到这一天终于来了!
6月22日晚,中国国家药品监督管理局(NMPA)官网显示,和黄医药研发的小分子MET抑制剂(原名)。 Ni)在中国获批,这意味着中国迎来了第一个获批的选择性MET抑制剂,这也是全球第三个获批的MET抑制剂。
被批准用于间充质-上皮转化因子 (MET) 外显子 14 跳跃的局部晚期或转移性非小细胞肺癌。
疾病控制率为 94.4%,布瑞替尼对 MET 非常有希望
贝瑞替尼 (PLB-1001, CBT-101) 是一种强效和高选择性的 c-MET 抑制剂,在体外和体内非小细胞肺癌 ( ) 模型中显示出优异的活性。
2020 AACR大会报告了布瑞替尼治疗c-Met异常晚期非小细胞肺癌的I期临床试验结果。
研究结果显示,8例患者仅检测到c-MET过表达,11例患者仅携带Ex14跳跃突变,8例患者仅检测到MET基因扩增,另外10例患者检测到多于1个MET突变。 一般耐受性良好,没有剂量限制性毒性。在所有可评估疗效的 36 名患者中,布瑞替尼的客观缓解率 (ORR) 为 30.6% (11 /36),疾病控制率 (DCR) 为 94. 4% (34/36).
综上所述,布瑞替尼在治疗 c-Met 异常的晚期非小细胞肺癌中的疗效令人印象深刻且前景广阔。
新型抗体偶联 (ADC) 药物 ABBV-399 潜力巨大
(-v, ABBV-399)是一种新型的c-MET靶向抗体-药物偶联物(ADC),在治疗c-MET过表达的非小细胞肺癌方面具有非常高的潜力患者。潜力巨大。
在2021 AACR年会上,ABBV-399公布了其II期研究结果,显示出治疗c-MET过表达非小细胞肺癌患者的巨大潜力 ABBV-399具有总体缓解率35.1%,中位反应持续时间6.9 个月;其中,c-MET高表达患者的总体缓解率为53.8%,低表达患者的总体缓解率为25.0%。
目前贝瑞替尼、ABBV-399、、卡马替尼等多款MET抑制剂新药临床试验均在招募国内患者。名称和具体数据尚未披露。
热门目标 - RET
RET 激酶的基因组改变,包括融合和点突变,会导致过度活跃的 RET 信号传导和不受控制的细胞生长 RET 融合和突变以不同的频率发生在各种肿瘤类型中。
据统计,约有1%~2%的非小细胞肺癌患者存在RET基因融合。超过60%的甲状腺髓样癌患者有RET基因突变,10%的甲状腺乳头状癌患者有RET基因融合。具体信息可以看下图。所以,做过多次基因检测的大家可以先看看RET基因有没有突变或融合。这个药一旦上市,大家都会有新的希望!如果您还没有测试过,小编建议您选择NGS技术进行全面测试。
两种 FDA 批准的 RET 突变靶向药物
2017年之前,靶向RET突变只能被多激酶抑制的药物(如和)无效。
2020年RET基因突变治疗取得巨大飞跃,两款高效抑制剂获批上市!
(LOXO-292) 有 91% 的颅内反应率!
普瑞替尼 (BLU-667)@) >接近 60%!
临床数据表明,无论是否接受治疗,目标病灶都会消退,疾病控制时间持久!
目前有口服多靶点抑制剂药物-28(EGFR、RET等靶点均有抑制作用),我国自主研发的1类小分子创新药SY-5007(高活性RET抑制剂)正在临床已招募,适应症均为RET融合阳性肺癌患者的二线治疗。
热门目标 - HER2
人类表皮生长因子受体-2(HER2)是1980年代三个研究组独立发现的,是迄今为止研究最深入的乳腺癌基因之一。HER2基因是临床治疗的预后指标监测和肿瘤靶向治疗药物选择的重要靶点。
01复发风险降低72%,DS-8201挑战乳腺癌二线标准治疗
2021 年 10 月 4 日,FDA 授予 DS-8201()突破性疗法认定,用于治疗一名或多名基于抗 HER2 方案的不可切除或转移性 HER2 阳性乳腺癌成人患者的治疗。这是 DS-8201 的第四个突破性疗法认定。
此次获批的数据显示,与TDM1相比,DS-8201可将HER2阳性转移性乳腺癌患者的疾病进展或死亡风险降低高达72%!
02疾病控制率100%! FDA授予HER2+乳腺癌新药快速通道
2021 年 1 月,FDA 授予一种新型抗体药物偶联物的快速通道资格,旨在加速这种先进抗癌疗法的推出,并为患有晚期 HER2 阳性乳腺癌的患者带来更好的治疗选择一线治疗后进展
在本次中国HER2阳性乳腺癌1期临床试验中,客观缓解率高达74%,其中19例患者中有14例缓解,疾病控制率高达100%。
p>
在美国和澳大利亚进行的 HER2 阳性泛肿瘤 1 期试验中,客观缓解率为 67%,3 例患者中有 2 例缓解,疾病控制率为 100%。
目前,全球范围内已经启动了多项临床研究,其中一项正在招募之前曾失败过赫赛汀等一线治疗的 HER2 阳性乳腺癌患者。
“钉子户”目标点——KRAS
KRAS 是实体瘤中最常见的致癌基因之一,KRAS 突变存在于约 30% 的肿瘤中,包括 90% 的胰腺癌、30% 至 40% 的结肠癌和 1 5% 至 20% 的肿瘤肺癌。然而,KRAS靶向药物很少,KRAS曾经是最难的突变,没有药物。
9年磨一剑!疾病控制率80.6%!全球首个KRAS靶向药物AMG-510失焦
2021 年 5 月 28 日,FDA 批准 (, ) 用于治疗已接受至少一名全身治疗的具有 KRAS G12C 突变的非小细胞肺癌 ( ) 患者。这是目前唯一获批的KRAS突变靶向药物,也被称为科学家突破KRAS“不成药”的里程碑!
非小细胞肺癌靶向精准治疗获批,迈出一大步!
KRAS前沿靶向多种实体瘤,疾病控制率高达96%
( ) 是一种针对 KRAS G12C 突变体的优化口服抑制剂。在肺癌、结直肠癌等实体瘤的治疗中显示出良好疗效,有望成为第二个获批上市的KRAS抑制剂。
1)非小细胞肺癌:疾病控制率高达96%!
2)大肠癌:疾病控制率94%!
3)其他实体瘤:疾病控制率100%!
如果我不能使用它怎么办?国药D-1553崛起,国内患者得救!
鉴于刚刚获批上市,国人仍处于药品难求的紧迫阶段,我国药企也纷纷加紧新药研发进程在 KRAS 目标上。
好消息是,国产新药D-1553已正式开始招募各种KRAS g12c突变实体瘤患者!
稀有目标 -
成纤维细胞生长因子受体(FGFR)在肿瘤细胞增殖、存活、迁移和血管生成(新血管的形成)效应中起重要作用。 FGFR基因融合/重排、易位和扩增很可能导致各种癌症的发生。在胆管癌中,目前的研究证实基因融合/重排可以促进肿瘤的发生和发展,靶向治疗对此类突变的胆管癌有明显的治疗作用。
82%疾病控制率!解决胆管癌患者的燃眉之急!
2020年4月17日,FDA加速批准公司()用于治疗既往治疗的局部晚期或转移性成纤维细胞生长因子受体2()融合或重排的胆管癌患者,批准时间为比原定的 5 月 30 日批准日期提前了一个半月。这也是 FDA 批准的第一个胆管癌靶向治疗。
-202临床试验结果显示,融合/重排组客观缓解率为35.5%,其中完全缓解3例(2.8%),35例( 32.7%)患者部分缓解,50例(46.7%)患者病情稳定,疾病控制率为82%。
3 倍的缓解率! FGFR 目标迎来新药!
2020年12月1日,FDA授予治疗/2/3阳性胆管癌患者的优先审评地位,成为该药胆管癌适应症正式获得优先审批的第二个靶点。
本次加速获批的新药涵盖/2/3突变胆管癌,是在首个靶向药物的基础上扩展而来。
其中,二线标准化疗的总有效率为5.4%,而治疗的总有效率为21.6%,增长了3倍。
目前有两种新的融合突变和化疗治疗晚期或转移性胆管癌片剂(至少一种方案含有吉西他滨),HMPL-453酒石酸盐片剂目前正在招募中。
小编有话要说
针对不同的基因突变或不同类型的癌症,有不同的标准化治疗方案。如果及早治疗,可以取得良好的效果。对于晚期患者,也应接受规范、正规的治疗,不仅可以延长生命,还可以达到提高生活质量的目的。此外,
所以确诊为恶性肿瘤后,一定要带上所有的检查结果去肿瘤医院会诊,并请肿瘤科医生给你一个适合你的治疗方案,以免耽误你的病情。最后,祝愿每一位患者早日康复,再次拥抱健康!
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话