欢迎光临吉康旅!
小细胞肺癌,肺癌最恶性的亚型之一。小细胞肺癌最相关的致病因素是吸烟,几乎所有小细胞肺癌患者都是吸烟者;同理,小细胞肺癌治疗特别是靶向治疗的发展也相对困难。
然而,放疗、化疗和免疫治疗是为小细胞肺癌保留的三个“窗口”。这些方案在小细胞肺癌治疗中的疗效仍然可以为患者保留一些希望。
这一次,基因医学交流与大家分享一个非常特殊的案例。本例患者患有广泛期小细胞肺癌,期间多次复发。接受五线治疗后,生存时间达到惊人的10年!
广泛期小细胞肺癌+多次复发+五线治疗=10年以上生存
一位 65 岁的男性患者,与大多数小细胞肺癌患者一样,有很重的吸烟史。 2009年5月,确诊为IVa期小细胞肺癌()。
患者首先接受了伊立替康+顺铂化疗。 6个周期后,疗效非常显着,达到临床完全缓解。
2010 年 11 月,9 个月后,患者首次复发。因复发距离前次治疗6个多月,再次接受伊立替康+卡铂化疗6个周期,达到部分缓解。此外,患者还接受了胸部放疗以及预防性颅脑放疗(以防止脑转移)。
20个月后,2013年2月,患者出现黄疸和瘙痒,肝功能检查异常,腹部增强CT表现,小细胞肺癌已转移至胰头,胆总管被转移。也被屏蔽了。
经支架置入等手术治疗后,患者胆管梗阻症状缓解,再次接受伊立替康+卡铂化疗,同样为6个周期。影像学检查结果提示部分缓解。
已对患者进行随访以跟踪疾病的进展。好在病情稳定,没有出现高胆红素血症复发的迹象。
30个月后,2016年4月,患者出现左下腹非绞痛性疼痛,发现左肾转移灶。这次,患者口服拓扑替康 1 个月,但因胃肠道毒性而停药。在接下来的时间里,患者没有接受任何随访。
直至2018年6月,再次对患者进行随访。患者此时无症状,但影像学研究显示肾周肿块增大。在以往成功的基础上,在五线治疗的基础上,患者仍采用伊立替康+卡铂方案。
4个周期的用药后,患者进行影像学检查,结果显示部分缓解,肾脏转移灶减少。患者随后完成6个周期的治疗并继续随访。
最后一次随访是在 2019 年 8 月 5 日,距患者最初被诊断患有小细胞肺癌整整十年。状态还不错。
在医患双方的共同努力下,这个IV期小细胞肺癌患者已经跨越了10年!
“最毒”肺癌,靶向治疗“荒地”
小细胞肺癌是一种较难治疗的肺癌亚型,约占所有肺癌的15%。即便是目前医学水平上进展如此迅速的新药研发,面对小细胞肺癌也不得不“放慢脚步”。
手术是肺癌最重要的治疗方法之一,但面对小细胞肺癌,即使有机会进行手术,最终的疗效也未必理想。小细胞肺癌具有很强的侵袭性和高度恶性,患者在诊断开始时常发生转移。一些癌细胞在血管中解离,并随着血流在人体的其他部位定植,导致更广泛的转移。即使手术切除后,患者体内仍有可能残留癌细胞和组织,最终导致术后复发。
除了病情危急,小细胞肺癌的治疗也比较困难。综上所述,近两年,人们被视为“新希望”,但最终遭遇了新方案、新药的“滑铁卢”,小细胞肺癌占了很大比例。已经被FDA加速上市的项目也可能因为后期数据没有明显优势而被召回,等待进一步研究争取正式批准的机会(如)。
尽管癌症精准治疗发展如此迅速,但与十几二十年前相比,小细胞肺癌患者的治疗手段却少之又少,堪称“颠覆性”突破。
那么,对于广大小细胞肺癌患者来说,有哪些治疗方案仍然保留着一些希望,能够点燃治疗的“希望之火”呢?
化疗:改写二线治疗标准方案,鲁比卡汀写入NCCN指南!
长期以来,拓扑替康一直被推荐作为小细胞肺癌的二线治疗,并被各大指南推荐并用于临床,但患者的反应率仅为5%-24%左右新药鲁比卡丁(,,)的问世,终于为小细胞肺癌的二线治疗翻开了新的一页。
于 2020 年 6 月获得 FDA 加速批准,并于 2020 年 7 月被纳入 NCCN 指南推荐。这是一种 RNA 聚合酶 II 抑制剂,主要用于阻断细胞的转录过程。经历有丝分裂的细胞会发生畸变和凋亡,因此它们具有抗癌作用。在II期篮子试验( )中,所有患者均在一线铂类化疗后接受了卢比卡汀单药治疗。
结果显示,所有患者的总体缓解率为35.2%,疾病控制率为68.6%。与以往拓扑替康二线治疗的历史数据相比,增长了两倍多!
研究共随访 17.1 个月。中位缓解持续时间为 5.3 个月,中位无进展生存期为 3.5 个月。中位总生存期为 9.3 个月; 6个月生存率为67.1%,12个月生存率为34.2%。
该研究还观察了化疗和复发之间的间隔以及接受新疗法对患者缓解率的影响。对于间隔<90天的患者,总体缓解率为22.2%,疾病控制率为51.1%;对于间隔≥90天的患者,总体缓解率为45%,疾病控制率为81.7%。
这表明,对于那些复发较早的患者,瑞比卡丁二线治疗的疗效不如一线治疗疗效持续时间较长的患者。这一结果也体现了初始治疗效果对整个治疗过程和患者后续生存的重要性。
鲁比卡汀有哪些尚未开发的潜力?听听专家怎么说
在机制上,鲁比卡丁不仅可以影响癌细胞的转录,还可以影响人体正常体细胞的转录过程。例如,肿瘤组织微环境中的巨噬细胞也受此影响。
现有研究数据表明,受 影响的巨噬细胞降低了白细胞介素 (IL)-6 和 IL-8 的表达水平。 IL-6 和 IL-8 是促炎细胞因子。根据现有的临床研究证据[1],它们的表达水平升高会导致人体内自然杀伤细胞(NK细胞)的功能受损。
NK细胞在人体的先天免疫阶段发挥免疫功能。其功能受损,可能导致机体抗癌能力下降。
因此,专家指出,的这种“附加作用”使其成为免疫治疗甚至细胞免疫治疗的潜在“伙伴”。我们期待更多联合项目的成果,这些项目将大力探索鲁比卡汀这一方面的潜力。
免疫治疗一波三折,两个方案脱颖而出!
免疫疗法一直被认为是治疗小细胞肺癌最有前景的方向,已有多个药物“进入”该领域,并分别取得了一些进展。
但小细胞肺癌也是免疫疗法发展最曲折的适应症之一。虽然有几种药物取得了进展,但与现有方案相比,优势远不及其他癌症(如非小细胞肺癌)。
话虽如此,对于靶向治疗选择不多的小细胞肺癌患者,免疫治疗仍可被视为“救命”的手段,为治疗增添了一些希望。
01
:进入前线!长期疗效优势显着
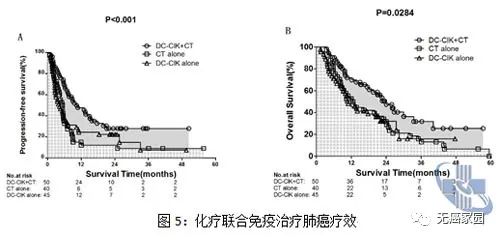
2020年3月27日, + 依托泊苷 + 铂类化疗(卡铂或顺铂)作为小细胞肺癌的新一线疗法。
批准基于 III 期试验的结果。试验结果显示,接受联合化疗的患者中位总生存期为13.0个月,明显超过单纯化疗的10.3名moon患者。
仅看这些数据,差异可能还不够明显。但如果我们延长随访时间线,我们会发现接受度伐单抗+化疗的患者12个月生存率为53.7%,18个月生存率为33.@ >9%,明显超过化疗的 39.8% 和 24.9%。
在无进展生存期方面,两种方案治疗患者的中位无进展生存期相似,但接受度伐单抗+化疗的患者12个月无进展生存期为17. 5%,只有 4.7% 的患者接受化疗。
在缓解率方面, 治疗也显示出优势。接受 加化疗的患者的总体缓解率为 68%,单独接受化疗的患者为 58%。在 12 个月的治疗中,22.7% 的 治疗患者仍然有反应,而仅接受化疗的患者为 6.3%。
免疫+化疗,还是双免疫+化疗?看看这项研究的结果
随着免疫疗法研究的深入和完善,越来越多的研究人员开始将目光转向“双免疫疗法”药物的“威力”联合治疗手段。
也曾尝试过这条路,它的“搭档”是新的CTLA-4抑制剂。继“O+Y”(纳武利尤单抗+易普利姆玛)的脚步之后,德瓦鲁单抗+易普利姆玛的组合也尝试了包括小细胞肺癌在内的多种适应症。

从结果[2]来看,双免疫+化疗的效果不如预期。增加了一种免疫治疗药物,效果与单独化疗相似。
中位总生存期为 10.4 个月,接受双联免疫治疗 + 化疗的患者,10.5 个月的接受化疗的患者,10.5 个月的接受化疗的患者+化疗患者单独化疗12.9个月。
在安全性方面,多加一种药物也导致不良事件显着增加。采用双免疫+化疗方案治疗的患者严重不良事件发生率为45%,显着高于+化疗方案的32%和单纯化疗方案的36%。
显然,双重免疫方案在小细胞肺癌的治疗上有点“过头”,但得不偿失。研究人员仍需再接再厉,不断寻找新的突破点。
02
阿特珠单抗:进入前线!长期疗效优势显着
另一种获得 FDA 批准的用于治疗小细胞肺癌的免疫方案来自 (,)。 2019年3月19日,FDA批准联合依托泊苷和卡铂的联合方案用于广泛期小细胞肺癌患者的一线治疗。
此批准基于 III 期研究的结果。研究结果显示,接受+化疗的患者中位总生存期为12.3个月,明显超过单纯化疗患者的10.3个月。
同样, 方案在生存方面取得了一定的优势。接受阿特珠单抗+化疗的患者,6个月无进展生存率为30.9%,12个月无进展生存率为12.6%,均显着高于2 2.4% 和 5.4% 的患者接受化疗。
这两个成功的项目有什么共同点?
由于没有找到类似的权威分析和研究成果,小慧冒险总结、总结和猜测。
①PD-L1抑制剂和PD-1抑制剂哪个更合适?
两个成功的一线免疫治疗药物是PD-L1抑制剂,这让人不得不猜测,或许PD-L1抑制剂在治疗小细胞肺癌方面会更有优势。当然,没有临床试验就没有说服力。或许在找到更合适的治疗方案后,主要的 PD-1 抑制剂也能表现出相似或更显着的优势。
②化疗方案的“配合”很重要
小细胞肺癌是肺癌的一种亚型,对化疗和放疗比较敏感,但单靠化疗不能携带小细胞肺癌治疗“大旗”的重要原因之一是小细胞肺癌化疗后极易产生耐药或复发[3]。
与癌症的斗争是一场漫长而艰巨的“战斗”,而一个只能持续几个月的解决方案显然不是我们期望找到的。免疫疗法的加入在一定程度上提高了小细胞肺癌的治疗效果,但显然还需要更多的努力才能真正使患者的生存期达到医患双方都满意的水平。
上文提到的小细胞肺癌化疗新药阿比卡丁很有希望成为小细胞肺癌治疗的新突破。我们非常期待看到联合免疫疗法的临床试验,这可能成为治疗小细胞肺癌的新希望。
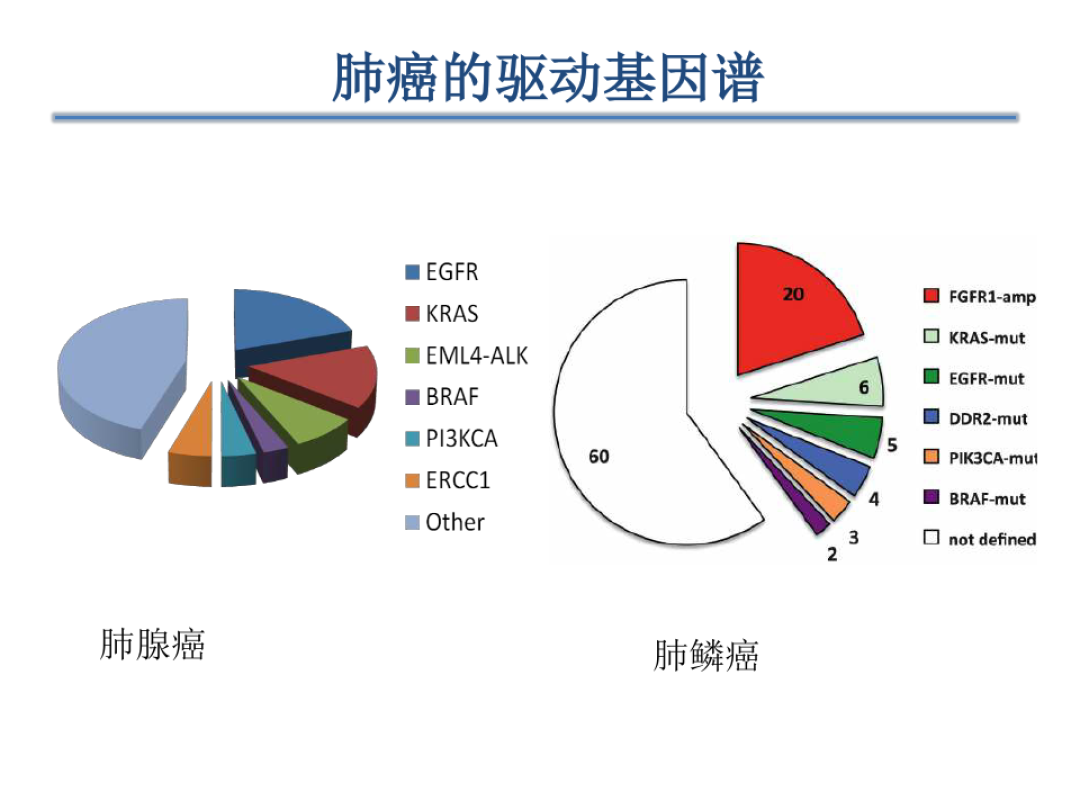
靶向治疗:需要更多研究
早些年,研究人员尝试利用治疗非小细胞肺癌的思路,使用各种靶向药物治疗小细胞肺癌,但效果并不如预期。
p>
治疗非小细胞肺癌的重要靶向药物EGFR抑制剂(EGFR-TKI)吉非替尼在治疗小细胞肺癌方面完全失败。随后的研究发现,小细胞肺癌中EGFR的突变率仅为4%。
伊马替尼治疗小细胞肺癌,无论是单药还是联合化疗,均无明显疗效。随后的研究发现,SCLC中KIT突变的发生率也很低,同时极有可能出现PI3K/Akt/mTOR信号通路的异常激活,这使得SCLC对伊马替尼耐药高度敏感。
但这还不足以让研究人员望而却步。
众所周知,小细胞肺癌是一种易发生转移的癌症。癌细胞转移到人体的其他部位并发展成病变。一个非常必要的“基础设施”措施是建立新的血管并从人体中吸收足够的营养——而这种类型的靶向治疗药物恰好被使用。抑制新血管的形成,即抗血管生成抑制剂。
这种药物有望成为小细胞肺癌靶向治疗的新“突破口”吗?
已应用于临床的抗血管生成抑制剂药物种类繁多,其中几种已在小细胞肺癌的治疗中“早期开发”。
01
安罗替尼:中国自主研发的新药,打破治疗空白
目前被权威诊疗指南提及并推荐为三线治疗的靶点,目前唯一可用的药物是我国自主研发的安罗替尼。安罗替尼是一类小分子多靶点酪氨酸激酶抑制剂,属于抗血管生成抑制剂类。安罗替尼与安慰剂在小细胞肺癌三线及以上治疗中的II期研究结果显示,安罗替尼将小细胞肺癌患者的中位无进展生存期从0.7个月延长至< @0. @4.1 个月,中位总生存期从 2.6 个月增加到 6.3 个月。
作为一线治疗药物,安罗替尼也显示出非常有前景的疗效。安罗替尼联合化疗一线治疗,客观缓解率达到77.78%,中位无进展生存期9.6个月,疾病控制率达到96.@ >3%,明显超过现有一线治疗方案的疗效。
02
贝伐单抗:小研究有一定效果,需要在更大的研究中验证
根据一项II期研究[4] 接受顺铂-依托泊苷治疗的32例复发小细胞肺癌患者(28例可评估病灶),接受贝伐单抗+伊立替康治疗的结果,总反应率为25 %,2个月疾病控制率为89%;中位缓解持续时间为 6 个月,中位无进展生存期为 3 个月,中位总生存期为 6 个月。
总的来说,疗效是有的,但还不够,还需要更大规模的研究来证实。
03
AMG-757:初步研究结果刚刚公布,进一步研究正在进行中
除抗血管生成抑制剂外,专门针对小细胞治疗的肺癌新靶向药物的研发从未落伍。 2020年底,安进公布了其新药AMG-757治疗小细胞肺癌的首个临床数据。
在 38 例可评估病灶的患者中,总体缓解率为 16%,29% 的患者病情稳定。作为剂量递增试验的结果,该数据具有一定的预期价值,但需要进一步研究。我们将密切关注研究成果,及时为您带来最新资讯。
参与临床试验,把握新药新方案治疗机遇
鉴于目前小细胞肺癌最有效的方案仍以化疗、免疫+化疗为主,基因药物汇汇为大家收集了一些相关的临床试验,为小细胞肺癌患者提供一个通道申请。
有需要的患者可以咨询Gene ()了解试验招募详情,然后在专业医疗顾问的指导下做出选择。
希望每一位患者都能找到适合自己的方案,获得更长的生存期。
临床试验重点推荐-盐酸米托蒽醌脂质体
米托蒽醌也是获批药物市面上的经典靶向药物与多柔比星()属于同一类蒽环类药物。是目前最有效的化疗方案之一。适合蒽环类药物的癌症类型包括白血病、淋巴瘤、乳腺癌、子宫癌、卵巢癌和肺癌。
临床研究表明,米托蒽醌比多柔比星的心脏毒性更小且更安全。其抗肿瘤活性与多柔比星相当或略高,明显高于环磷酰胺、氟尿嘧啶、甲氨蝶呤、长春新碱和阿糖胞苷,抗肿瘤谱广,可用于多种癌症类型的治疗。米托蒽醌与多种常用抗肿瘤药物有协同作用,与阿霉素仅部分交叉耐药。
脂质体是一种高效低毒的制剂,转染率更高,疗效更显着。招募患者,有需要的患者可联系全球肿瘤医师网络医学部()申请。
参考文献
[1]
[2](20)-8/
[3]
[4]
[5]- 细胞肺, , 5 和 10 年以上
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话