欢迎光临吉康旅!
第三代EGFR-TKI()奥希替尼是一种强效口服不可逆EGFR-TKI,一经问世就引起了全世界的关注。主要是因为大部分EGFR突变患者在服用一、二代TKI(易瑞沙、特罗凯、凯美瑞等)9-12个月后会出现耐药,其中约60%是由于突变而出现的。过去,没有更好的办法来应对突变,但它的出现,可以说是解决了世界的难题。作为第三代EGFR-TKI,对EGFR突变和耐药突变均有抑制作用。
奥希替尼是目前二线EGFR TKI耐药后继发突变患者最常用的治疗方法。 2017年3月24日,CFDA批准奥希替尼用于治疗第一代和第二代EGFR-TKI耐药突变患者。奥希替尼获批仅用了7个月,表明我国新药研究国际化进程有所提升。奥希替尼是FDA和CFDA批准的第三代药物,主要基于一系列AURA研究的阳性数据。
1.研究
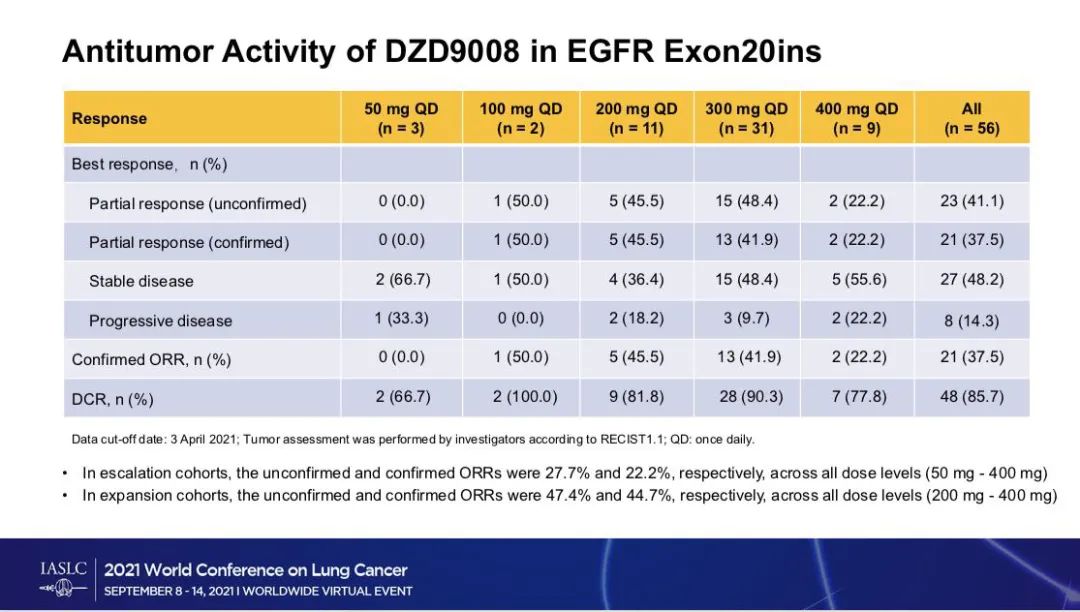
AURA 研究是一项多中心开放标签 I/O,旨在评估奥希替尼在进展后的第一代 EGFR-TKI 患者中不同剂量递增组的安全性、耐受性、PK 和抗肿瘤活性。二期研究。 AURA研究的I期结果于2015年4月30日发表在国际顶级期刊《新英格兰医学杂志》上。共有253名经EGFR-TKI治疗后被诊断为疾病进展的晚期肺癌患者入组剂量递增组31例,5个剂量扩展组222例。药物方案是奥希替尼 20 至每天一次。研究终点是药物的安全性、药代动力学和疗效。收集剂量扩展组。研究前患者的组织活检结果用于评估突变状态。
测试结果:
总体客观缓解率 (ORR) 为 51%。 127例检出阳性突变的ORR为61%,中位无进展生存期(PFS)9.6个月; 61例未检测到突变的ORR为21%,中位PFS为2.8个月。
随着治疗剂量的增加,剂量递增组未发现剂量限制性毒性。剂量扩大组常见的不良反应为腹泻、皮疹、恶心和食欲下降。
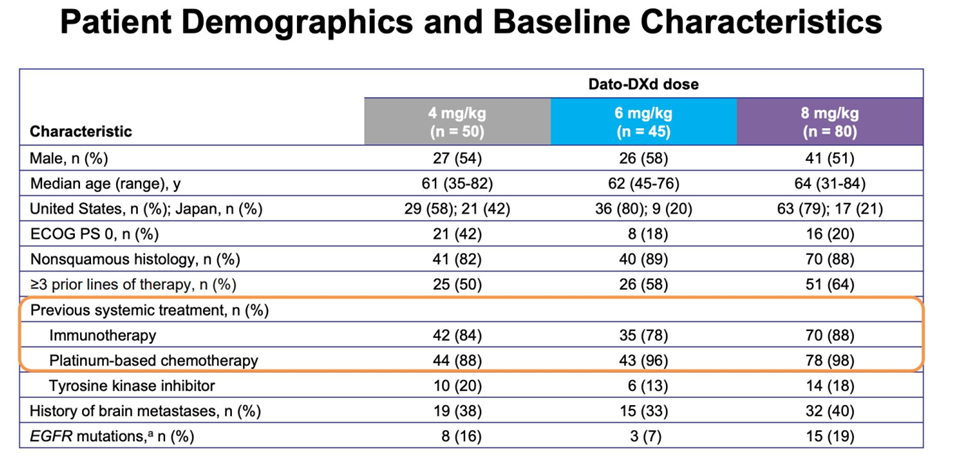
1.研究
研究是一项单臂开放标签 II 期研究,评估奥希替尼在接受 EGFR-TKI 治疗后进展的局部晚期或转移性疾病阳性患者的安全性和抗肿瘤活性。
测试结果:
中位随访时间为 13.0 个月(IQR7.6-14.2)。对 140 名患者的独立中心评估发现 6 名患者有完全缓解(3%),134名(67%)患者部分缓解,mPFS为9.9m。
1.研究
该研究招募了在一线 EGFR-TKI 治疗后出现突变的患者。该研究结果在 2016 年世界肺癌大会上公布,并几乎同时发表在《新英格兰医学杂志》上。共有 419 名患者被随机分配接受奥希替尼(n=279) 和培美曲塞铂(n=140))。
奥希替尼组和培美曲塞铂组mPFS分别为10.1m和4.4m(HR=0.30,95%CI0.23–< @0.41,p
2017年3月,奥希替尼获cFDA批准作为第三代EGFR-TKI用于治疗EGFR-TKI耐药后的晚期突变体。如有需要,请咨询康美星海外医疗医疗顾问:或扫码加下方微信,我们将竭诚为您服务!点击展开阅读:奥希替尼/奥沙替尼()的发展历程及治疗优势
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话
坦西莫司作用的靶点mTOR蛋白是极其重要的一类蛋白,是哺乳动物代谢调节的中枢,参与多种细胞与组织的生理活动,在细胞生长、分化、转移...
FDA批准伊布替尼用于治疗患有以下疾病的成人患者: 1. 既往至少接受过一种治疗的套细胞淋巴瘤(MCL) 2. 慢性淋巴细胞性白血病(C...
根据世界卫生组织国际癌症研究机构(IARC)近期发布的2020年全球最新癌症负担数据报告,乳腺癌首次超越了肺癌,成为了世界上新发患者数...
米哚妥林 (midostaurin,米哚妥林)在2017年被批准用于急性髓性白血病(Acute myeloid leukemia, AML)的治疗后,米哚妥林就被认为开创...
劳拉替尼是一种激酶抑制剂(TKI),对ALK染色体重组的潜伏期肺癌病例呈现高度的活性。劳拉替尼是专为抑制对其它ALK抑制剂产生抗药性的肿...








