欢迎光临吉康旅!
传统化疗疗效差,新兴免疫疗法反应率低。三阴性乳腺癌的治疗一直是一个非常棘手的问题。
最近一项贝伐单抗治疗三阴性乳腺癌的研究表明,单剂量的贝伐单抗降低了原发性三阴性乳腺癌患者血管生成素 2 阳性血管的密度并改善了 CD4。+T 和 CD8+ T 细胞和成熟树突细胞的浸润。该研究结果为将贝伐单抗添加到三阴性乳腺癌的新辅助治疗以增强免疫治疗的疗效提供了强有力的依据。
01
三阴性乳腺癌,治疗“老难”
三阴性乳腺癌(TNBC)是指雌激素受体、孕激素受体和人表皮生长因子受体(HER2,又称HER2)表达阴性的乳腺癌亚型,约占15%~20%。这种类型的乳腺癌通常进展迅速,具有侵袭性,并且预后非常差。三阴性乳腺癌是乳腺癌研究的热点和难点。
图1
由于其独特的临床病理学和分子特征,激素治疗药物和 HER2 靶向治疗对三阴性乳腺癌均无效。传统化疗是主要治疗方法,但疗效较差,患者中位生存期仅为12-25.7个月。
随着免疫检查点研究的深入,一项随机III期临床研究显示,新辅助抗PD-1抗体派姆单抗联合化疗对局部三阴性乳腺癌有显着疗效,但只有约30%的患者对治疗有反应. 在另一项派姆单抗治疗三阴性乳腺癌的研究中,派姆单抗联合化疗可将转移性三阴性乳腺癌患者的中位无进展生存期延长 2-4 个月。尤其对于PD-L1高表达(CPS≥10)的患者,效果更显着。
02
机制明确,治疗有针对性
对三阴性乳腺癌患者的研究仍在进行中,研究人员正在瞄准抗血管生成药物。既往研究发现,阻断血管内皮生长因子受体-2(VEGF)可使肿瘤血管正常化,增加CD8+T细胞浸润,使肿瘤治疗药物发挥更好的作用。三阴性乳腺癌患者血管内皮生长因子(VEGF)的表达水平明显高于非三阴性乳腺癌患者,这为抗血管生成药物的应用提供了理论依据。
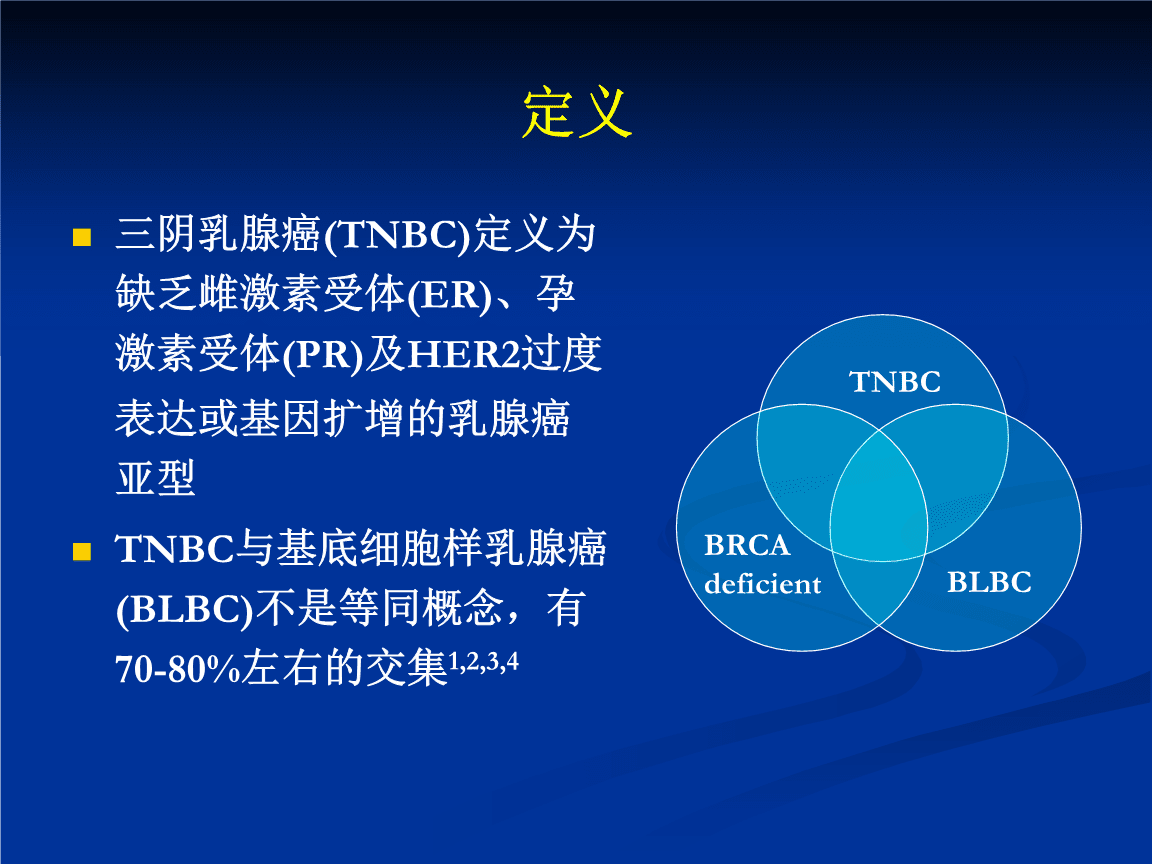
图 2
同时,抗EGFR-2治疗可以降低乳腺癌模型中血管生成素2(Ang2))的表达。血管生成素2可以使血管不稳定,增加免疫抑制细胞聚集,并与免疫治疗耐药相关。黑色素瘤患者。因此,降低 -2 的表达有助于血管正常化并改善抗肿瘤免疫反应。
此外,血管内皮生长因子可以直接抑制树突状细胞(DC)的成熟,因此可以推测抗血管内皮生长因子抗体-贝伐单抗可以使肿瘤血管正常化并降低血管生成素-2水平,增加浸润性三阴性乳腺癌中的 T 细胞和其他免疫刺激细胞,包括 DC。
基于上述理论基础,我们研究了贝伐单抗对活检中免疫细胞的脉管系统和肿瘤内浸润的影响。
03
前后对比,治疗效果显着
在一项针对三阴性乳腺癌患者的新辅助贝伐单抗(10 mg/kg)的 II 期试验中,研究人员在单剂贝伐单抗治疗前和两周后评估了 10 次活检。阻断血管内皮生长因子对血管系统和免疫细胞瘤内浸润的影响。
在多重和免疫荧光测定后,发现贝伐单抗显着降低了 CD31+ 和 CD31+Ang2+ 的总量,但没有降低与血管正常化相关的 CD31+Ang2- 血管密度。通过阻断血管内皮生长因子,CD8+T细胞整体浸润明显增加,同时贝伐单抗可促进三阴性乳腺癌记忆T细胞成熟和MHC-I表达。此外,贝伐单抗治疗导致三阴性乳腺癌组织中 +-CD68- 和 ++CD68- 树突状细胞密度显着增加。
图 3 (a) 贝伐单抗降低 CD31+Ang2+ 血管密度。贝伐单抗治疗前后 CD31 和 Ang2 的代表性免疫荧光(来自同一患者的配对样本的图像)。(bd) 三阴性乳腺癌血管的定量分析。
04
概括
在这项研究中,10 对接受单剂量贝伐单抗治疗的三阴性乳腺癌患者的免疫荧光显示,贝伐单抗降低了血管生成素-2 阳性血管的密度,同时改善了三阴性乳腺癌。乳腺癌患者中 CD4+ T 和 CD8+ T 细胞以及成熟树突状细胞的浸润。
这一结果提示贝伐单抗可能提高三阴性乳腺癌患者免疫治疗的疗效,同时贝伐单抗诱导的浸润性免疫细胞变化也可以作为治疗效果的预测性生物标志物,用于指导选择免疫联合药物。我们期待在临床研究中进一步验证这一发现。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话