欢迎光临吉康旅!
奥希替尼耐药了怎么办,EGFR TKI治疗后出现的RET基因突变融合是什么,已经上市和在研的RET抑制剂有哪些?
EGFR突变肺癌人群是最幸运的晚期肺癌患者。目前开发的一、二、第三代TKI靶向药物的口服治疗,可以让患者获得长期高质量的生存,是目前肿瘤精准治疗的一种模式。尤其是随着2017年奥希替尼在中国的上市,其生存优势被提升到一个新的高度。
奥赛替尼虽然为EGFR突变型非小细胞肺癌患者带来了新的选择和新的希望,但与其他靶向药物一样,它仍然无法摆脱耐药性的噩梦。RET融合是非小细胞肺癌的驱动基因之一,占比约2%。
同时,RET融合是奥希替尼获得性耐药的机制之一。值得一提的是,获得性对奥希替尼耐药的患者RET融合发生率4.9%(中国患者约为4%),远高于第一代和第二代TKI0.8%。因此,RET融合也是第三代TKI获得性耐药机制的研究热点。
虽然RET基因融合的突变率较低,但对阳性患者的靶向治疗获益良多,因此对患者进行全基因检测具有重要意义。
今天, Free Home 的编辑将分享一个 EGFR 突变和获得性 RET 融合患者的临床治疗案例。
三年两次靶向耐药,疾病进展中发现RET突变,对症治疗后肿瘤缩小78%
为探究奥希替尼的耐药机制,麻省总医院于2014年7月至2018年8月使用奥希替尼单药治疗41例EGFR突变型非小细胞肺癌患者进行耐药评估。
其中有一份发人深省的病理报告。这是一位 60 岁的女性患者,她被诊断出患有 del 19 EGFR 突变的晚期非小细胞肺癌。医生给了阿法替尼治疗。结果,疾病在1年后进展。基因检测发现突变,报告提示患者对阿法替尼耐药,下一步医生自然会使用奥希替尼。然而,经过18个月的奥希替尼治疗,患者的病情再次恶化。然后她接受了胸膜活检,发现存在 -RET 融合。基线组织的 RET 荧光原位杂交 (FISH) 为阴性,表明确实获得了 -RET 融合。
结果出乎意料。患者居然在两次耐药后发展为RET融合!
幸运的是,基因检测又进行了。主治医生根据成功的临床经验调整了患者的用药方案,从每天 80 mg+(BLU-667,)200 mg 开始,然后 BLU-667 治疗 2 周后剂量增加至 300 mg。
情况开始发生惊人的逆转。经过几天的奥希替尼+BLU-667方案治疗,患者的呼吸困难得到明显改善。8 周后,成像显示肿瘤缩小了 78%。在治疗 16 周后进行的后续成像中可以看到确认的部分缓解!
患者 1 对奥希替尼和 BLU-667 治疗的反应。胸部连续冠状动脉对比增强计算机断层扫描图像显示,在用 BLU-667 和奥希替尼(右)治疗 8 周后,基线(左)肺肿块和胸膜结节(红色箭头)可见于右下叶,部分反应。
本案的耐人寻味之处在于,RET融合是奥希替尼获得性耐药的机制之一,这在以往的临床工作中可能没有引起足够的重视。

根据该患者的治疗经验,临床医生确定了一位相似的患者(患者2)。一位67岁的女性患者,她接受了手术和辅助顺铂/培美曲塞治疗,随后复发。她接受了阿法替尼联合西妥昔单抗2年,然后进行肺活检。NGS 测试证明获得性 RET 融合(治疗前活检中不存在))。
再次使用单独的个体患者研究新药 (IND) 计划,每天服用 80 mg + BLU-667 200 mg 连续 2 周,然后每天服用 300 mg BLU 667 连续 2 周,最后升级到每天 400 mg。8周后的扫描也显示出显着的临床改善,成像成像肿瘤缩小了78%!
与基线(左)相比,患者 2 对奥希替尼和 BLU-667 治疗的反应显示左上叶和左下叶肺混浊(右;圆圈)有显着改善。
结合以上病例报道,不难看出RET特异性抑制剂(BLU-667,)对EGFR TKI治疗后RET融合的患者具有显着的治疗效果。
《无癌家园》编辑再次强调,EGFR TKI治疗进展后,要考虑RET融合的可能性,需要积极开展基因检测,更广泛、更全面的基因检测是最佳选择。只有这样,我们才能帮助患者找到治疗目标,让他们重获生命的机会。
关于热门目标RET,赶紧来了解一下
RET 激酶的基因组变化包括融合和点突变,这会导致过度活跃的 RET 信号传导和不受控制的细胞生长。RET融合和突变发生在多种肿瘤类型中,发生频率不同。
据统计,在非小细胞肺癌中,约有1%~2%的患者存在RET基因融合。在甲状腺髓样癌中,超过 60% 的患者有 RET 基因突变,而在甲状腺乳头状癌中,10% 的患者有 RET 基因融合。对于RET基因融合,具体信息可以看下图。因此,对于做过过多基因检测的患者,可以先看看RET基因是否有突变或融合。一旦被检测出来,大家都会希望使用相关的靶向药物!如果还没有经过测试,小编建议大家选择NGS技术。综合测试。
RET融合:非小细胞肺癌2%,甲状腺癌10%·20%,胰腺癌
RET突变:甲状腺髓样癌>60%
FDA批准的两种RET突变靶向药物
2017年之前,RET突变只能用多激酶抑制剂(如and)治疗,效果不佳。

2020年,RET基因突变治疗取得巨大飞跃,两款高效抑制剂获批上市!
舍帕替尼(LOXO-292)颅内反应率高达91%!
(BLU-667) 接近 60%!
临床数据表明,无论是否接受治疗,目标病灶都会消失,疾病控制会持续很长时间!
目前有口服多靶点抑制剂药物-28(对EGFR、RET等靶点有抑制作用),我国自主研发的1类小分子创新药SY-5007(高活性RET抑制剂) ) 正在临床招募中。适应症为 RET 融合阳性肺癌患者的二线治疗。想参加临床试验的癌症朋友可以咨询无癌家园医疗部详细评估病情。
两种治疗肺癌RET基因的新药横空出世
目前,我们在临床试验网站上一共发现了46个RET临床试验,其中36个是开放的,非小细胞肺癌的临床试验有17个。在这些新药的临床研究中,出现了许多新的新药品种。该药物发表了优秀的临床试验数据,非常令人兴奋,值得期待。
01、 客观回复率75%!另一个强大的RET抑制剂来袭
药品名称:RXDX-105
对象:RET/BRAF 研发公司:罗氏
药物介绍:RXDX-105是公司为解决耐药性问题而研发的多激酶抑制剂。
临床数据:21名参与临床试验的RET融合患者的数据在2017年ESMO会议上公布。这些患者此前均未接受过 RET 融合靶向治疗,其中 13 例为 -RET 融合,8 例为非 RET。结果显示,13例-RET融合患者中无客观肿瘤缓解病例,仅3例病情稳定超过6个月。8例非RET融合患者中,6例(75%)肿瘤客观缓解。
02、二代RET抑制剂TPX-0046曙光初现
药品名称:TPX-0046
目标点: RET 研发公司:
药物介绍:TPX-0046是第二代RET抑制剂,TPX-0046的分子量(MW)
临床数据:
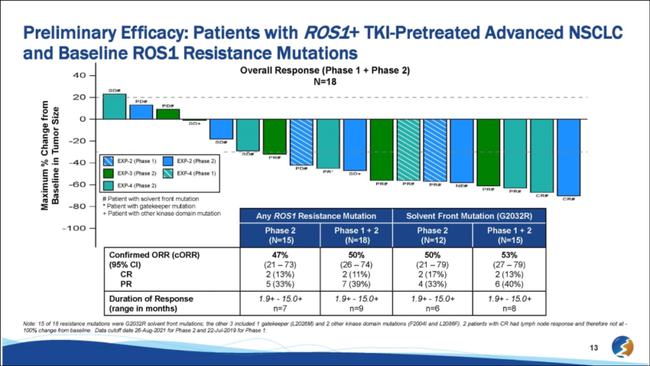
2021年4月5日,TPX-/2 -1研究的初步临床数据显示,共有21例RET改变或MTC患者接受了TPX-0046治疗,其中5例未接受RET TKI治疗,其中, 4 显示肿瘤消退;在 9 名 TKI 预处理患者中,3 名患者出现肿瘤消退。
我有话要说
过去,RET基因融合的非小细胞肺癌患者只能接受一线和二线化疗。BLU-667和LOXO-292有望改变中国RET融合阳性非小细胞肺癌患者的治疗标准。在肺癌精准治疗领域,RET靶点的研发是继EGFR、ALK、ROS1、NTRK等靶点之后的又一重大突破!
提示:哪些患者需要寻求国际专家的帮助
事实上,无癌家园提倡在了解病情后,通过远程会诊,获得国际诊疗的第二意见,再决定进一步的治疗方案。这可能会给你带来更多的选择。详情请咨询医药部。.
以下几类患者需要重点国际会诊:
1、 在治疗药物的选择上遇到了瓶颈;
2、病情复杂,诊断不明确;
3、对治疗方案或效果不满意,想寻求新的方案;
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话