欢迎光临吉康旅!
奥希替尼耐药怎么办,奥希替尼耐药后怎么办,靶向药物奥希替尼耐药后怎么办
相信对于各类癌症患者来说,第三代EGFR抑制剂“奥希替尼”的名字可以说是“瑞冠尔”,彻底开启了非小细胞肺癌治疗的新纪元。
这类药物的最大特点是,无论是用于初治患者还是已治疗患者,都能发挥远超第一代药物的作用,大大延长患者的生存期,造福更多的患者。
奥希替尼可以破解第一代和第二代EGFR抑制剂的耐药后突变,但癌细胞太狡猾了,可能还是会产生相应的针对该药物的耐药突变,如MET、HER2/3、EGFR突变等。等待。如何破解这些耐药突变已成为进一步探索奥希替尼临床潜力的关键之一。
目前,关于奥希替尼耐药的各种治疗方案的研究非常丰富,进展也各不相同。奥希替尼开创了治疗EGFR突变型非小细胞肺癌的“奥希替尼时代”。这些新药、新疗法将成为“后奥希替尼时代”的先行者,为患者开辟一个全新的时代。对待情况。
新药研发如火如荼:开启“后奥希替尼时代”
使用第四代药物或另一种新药来克服第三代药物的耐药突变是新药开发最主流的思路之一。根据基因分析结果,第三代EGFR抑制剂耐药后最常见的突变类型包括MET(约25%)、EGFR//和//三重突变(约20%~40%)和HER2/3等。
目前,MET突变和突变是“后奥希替尼”新药研发的主要方向。
01、EGFR抑制剂:第四代EGFR抑制剂,“国研”全球领先
目前,第一个进入临床试验的第四代EGFR抑制剂是中国药企研发的新药。该药不针对EGFR等突变,而是专门针对EGFR三代耐药后常见的突变,因此对三代耐药后患者的治疗效果更佳。
目前,临床前试验已经显示出良好的效果,进一步的人体试验项目正在进行中,我们将密切关注试验结果。
此外,国外药企研发的BLU-945在临床前研究中也显示出优异的潜力,目前正在进行进一步的临床试验。
02、MET抑制剂:多种新药问世,耐药及脑转移患者可受益
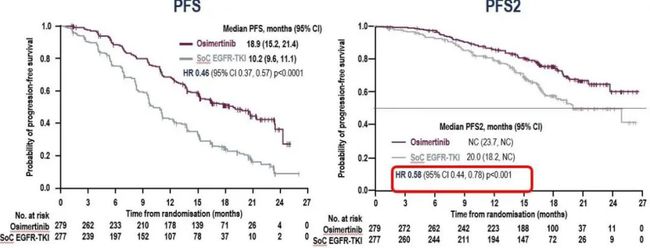
MET突变可能作为原发肿瘤原因存在,也是导致EGFR抑制剂耐药的“罪魁祸首”之一。
目前已经批准上市的MET抑制剂有两种,分别是日本批准上市的和美国FDA批准上市的卡马替尼。这两种药物在耐药患者的治疗中均显示出较为理想的效果。
其中瑞帕替尼治疗总体缓解率达到42.4%,卡马替尼治疗总体缓解率达到67.9%,两药疾病控制率均超过90% ,缓解持续时间分别为12.39个月和9.72~11.14个月。
在治疗脑转移患者方面也显示出良好的潜力。患者全身客观缓解率为52.4%,疾病控制率为76.2%;中位缓解持续时间9.5个月,中位无进展生存期9.5个月。
目前,MET抑制剂的研发项目非常丰富,各种MET突变亚型的临床试验正在招募中。有此类突变的患者可以联系全球肿瘤学家网络医学部进行详细咨询,匹配合适的临床试验项目。
03、EGFR-MET双抗体:“双管齐下”突破耐药困境
既然MET突变是EGFR耐药的最重要原因之一,那么使用双靶点抑制剂,或者说“双抗体”药物,能否将治疗效果提升到一个更高的水平呢?
这种治疗思路也受到了关注。一项使用EGFR-MET双靶点抑制剂治疗第三代EGFR抑制剂耐药患者的I期临床试验初步结果在ASCO会议上发表,引起广泛关注。
结果显示,在接受第三代EGFR抑制剂治疗的47例患者中,总体缓解率达到21%;在 c-MET 扩增和其他突变类型的患者中观察到缓解。
目前,该药与相同靶点药物治疗非小细胞肺癌的临床试验正在进行中。有需要的病人可联络医药部了解详情。
04、HER3抑制剂:ADC“一家”又出“救命药”,疾控率极高
HER2/3 突变也是奥希替尼耐药的主要原因之一。日本U3-1402是HER3抗体偶联药物。在之前的ESMO会议上,研究人员已经公布了该药物治疗EGFR抑制剂耐药患者的疗效数据,疾病控制率达到了惊人的70%!
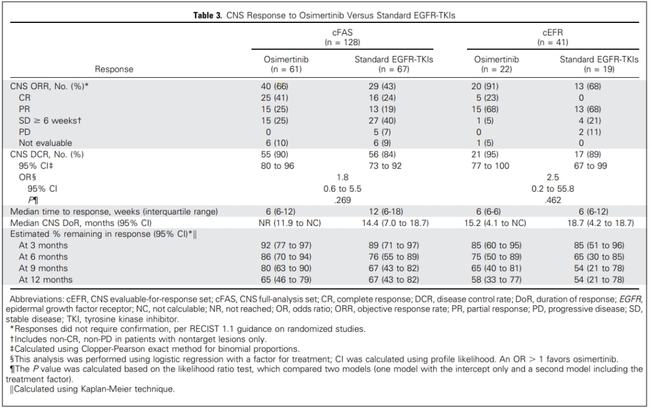
研究中,86%的患者接受过奥希替尼治疗,90%的患者接受过化疗;患者的治疗线中位数为 4 线,包括 2 线 EGFR 抑制剂治疗。
当然,U3-1402最大的突破意义在于,根据ASCO会议和WCLC会议公布的结果,无论是何种类型的耐药突变,都可以从这种药物的治疗中受益。这意味着,一旦该药成功获批上市,对EGFR抑制剂耐药的患者,极有可能等待一个“普适价值”的重磅新药。
“奥希替尼+”:联合计划成为克服耐药性的新突破
新药虽好,但研发周期一般都比较长。从初步数据公布到正式批准,可能需要几年时间。因此,研究人员提出了另一个想法:从“冷板凳”中发现一些潜在的“参与者”,并结合应用现有的药物。他们能否组成“聪明的士兵”来抑制耐药突变?
01、 从癌细胞表面抗原突破:cyst“无视”耐药性
相信很多患者对()这个名字都有些熟悉。的确,这种药物虽然已经获批肺鳞癌适应症,但对患者疗效的改善并不明显,表现一直不温不火,错过了各种“突破”的消息。
然而,在2019年的ASCO大会上,成为了一匹“黑马”,再次被发现了前所未有的新潜力。在治疗对多种EGFR抑制剂耐药的患者中,联合奥希替尼取得了优异的缓解率。
其中,对第一代和第二代EGFR抑制剂耐药的患者联合治疗总体缓解率为29%;对第三代EGFR抑制剂耐药患者的治疗总体缓解率为13%;其中,治疗/双突变的患者,总体缓解率达到了50%!
是一种非常有特色的药物。作为一种大分子药物,其作用部位是癌细胞表面的EGFR受体,而不是小分子药物靶向的细胞内酪氨酸激酶。随着越来越多的小分子药物取代了具有压倒性优势的大分子药物,这种药物再次以“黑马”的身份出现,让人不得不感叹。或许并不是药物在很多情况下无效。,但没有找到这种药的最佳适应症,导致药的“力”不足。
02、回归一二代:部分患者可受益于上一代药物治疗
EGFR抑制剂耐药引起的突变也分为顺式突变和反式突变,对耐药后的治疗有重要影响。
我们都知道人类DNA是双链结构。当突变出现在同一条DNA链上时,称为/cis突变,当两个突变出现在不同DNA链上时,称为/突变。. 在临床实践中,顺式突变较为常见,约占85%。
但从治疗的角度来看,这些相对少见的突变患者可能更“幸运”——这部分患者对第一代+第三代EGFR抑制剂的组合更敏感。
许多临床应用案例证实了该方案的效果,小规模试验的结果也在ASCO会议上发表。采用第一代EGFR抑制剂吉非替尼+第三代EGFR抑制剂奥希替尼联合治疗,患者的中位无进展生存期约为22.5个月,总体缓解率高达88.9%; 在病情持续进展的患者中,耐药的原因是旁路扩增等,未检测到突变或突变。但该方案的缺点是患者在治疗过程中出现的不良反应较为明显,耐受性稍差。
相信很多患者已经从这种治疗模式中受益。我们非常希望研究人员能够进一步优化治疗方案,明确适应症范围,减少或减少不良反应,让更多患者从中受益。
03、 “个体化”治疗的尝试:一个有前途的实验
该实验是一个真正具有巨大潜力的“个性化”研究项目。
在研究中,所有接受测试的奥希替尼耐药患者将再次接受活检,并根据活检结果进行治疗。例如,一些因MET扩增而表现出耐药性的患者,则接受奥希替尼+伏立替尼(一种MET抑制剂)治疗方案;部分患者有EGFR突变,则接受奥希默汀Ni+吉非替尼治疗;RET融合突变患者将接受奥希替尼+舍帕替尼(即LOXO-292).
显然,这个程序的设计并不复杂,甚至有“对症下药”的意思,但它可以针对每个患者不同的抵抗机制应用合适的程序。
我们非常期待这项研究的结果。极有可能验证这种“对症下药”的想法能否开创治疗的新时代,或被打入临床试验的某个阶段。但可以肯定的是,这种个性化的治疗思路必将成为未来研究的重要方向,引领众多新兴临床试验的设计思路。
“后奥希替尼时代”,新药来袭,先行试验
看完这篇总结,相信你已经看到了“后奥希替尼时代”多样化、个性化的治疗方案。但如果要选择适合自己的,首先要明确自己的耐药突变类型。
随着癌症精准治疗的发展,基因检测已成为每个癌症患者确诊后的必备检测项目。无论是新治疗的患者,还是经过一系列治疗产生耐药性的患者,都应在基因检测的指导下选择最可能的受益方案,真正有效地延长生存期。
关于基因检测、新药和临床试验项目,您可以联系全球肿瘤学家网络()医学部寻求帮助。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话