欢迎光临吉康旅!
EGFR,非小细胞肺癌的药物靶点。
简介:易瑞沙多久见效?
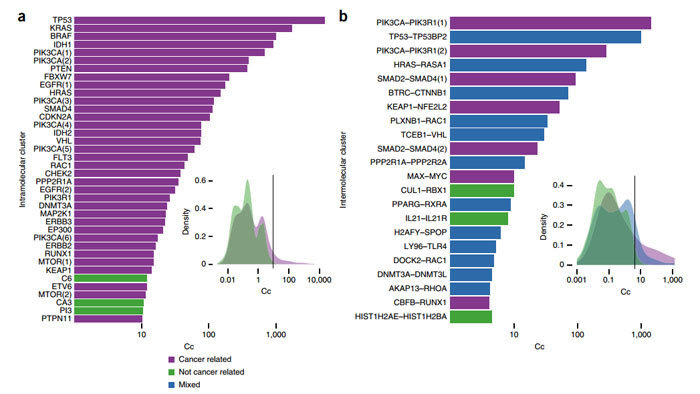
【微信ID:】:陈万清,全国癌症备案核心专家教授,相当于2016年1月25日在CA期刊发表2015年我国癌症统计数据。如原文所述男性中最常见的五种癌症是:肺癌和支气管癌、胃癌、食道癌、肝癌和结直肠癌,占所有癌症病例的三分之二。女性最常见的五种癌症是:乳腺癌、肺癌和支气管癌、胃癌、结直肠癌和食道癌,占所有癌症病例的 60%。2015年,我国约有429.2万癌症病例,281.4万人死于癌症。肺癌已成为最常见的癌症,这也是癌症死亡的主要基本原理。
. 在我国,非小细胞肺癌()病患者约占肺癌病例数的85%,其中约30%-40%会出现EGFR基因突变。EGFR基因突变的关键包括4种类型:外显子19缺失基因突变、外显子21点突变、外显子18点突变和外显子20插入基因突变。最常见的是外显子19()和外显子21点突变()的缺失基因突变,这两种突变都是EGFR-TKI的敏感基因突变。外显子20基因突变与EGFR-TKI继发耐药有关。EGFR-TKI是EGFR基因突变患者一线治疗的标准疗法。因此,EGFR阻滞剂的产品开发是肺癌治疗的一大科研网络热点。EGFR靶向治疗药物的种类现阶段,已经上市的EGFR靶向治疗药物共有三代。第一代是不可逆靶向治疗药物,第二代是不可逆靶向治疗药物。与一代相比,二代的疗效靶点较多,相对而言药物不良反应更高。更重要的是,第一代吸毒后,第二代无法摆脱药物。虽然一、二代靶向治疗药物取得了显著成效,但大多数患者在用药1-2年后就会出现病理改变。在接受药物治疗的EGFR阻滞剂患者中,50%接受药物治疗的药物与基因突变有关。
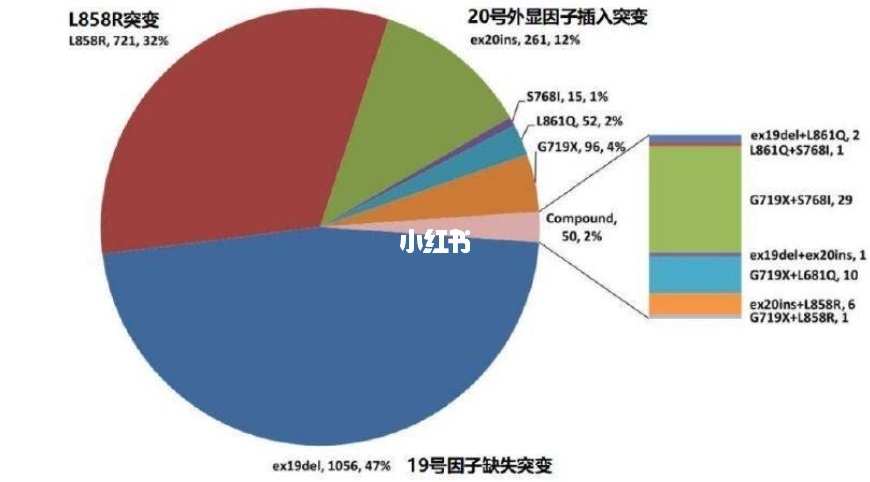
第三代EGFR靶向治疗药物可与EGFR敏感基因突变和基因突变域融合,抑制基因突变引起的恶性肿瘤药物的接受。但是,第三代靶向治疗药物也难免会产生耐药性。耐药性的基本原则是耐受药物基因突变。第四代靶向治疗药物可以对付第三代靶向治疗药物以抵御药物问题,但尚未上市。我国首个第四代药物ES-072已进入临床用药第一阶段,并融入症状。包括携带EGFR药物基因突变的患者及其携带EGFR药物基因突变的患者。上市药品详细介绍< @1、易瑞沙(吉非替尼)易瑞沙是由阿斯利康产品开发的,用于治疗EGFR。2002年首次获得PMDA批准,后又获得FDA、EMA和CFDA批准,是第一个上市的EGFR-TKI缓凝剂。易瑞沙整合的症状是单药应用,用于EGFR基因敏感基因突变的晚期、中晚期或迁移和传播疾病患者的一线治疗。药物最常见的副作用是腹泻和皮肤反应(包括皮疹、粉刺、皮肤干燥和瘙痒),一般在服药后 30 天内常见,并且一般是可逆的。注意间质性肺病、肝毒副作用、胃肠道穿孔、严重或持续性腹泻、
我国除进口外,只有齐鲁药业(海南)有限公司有批文并通过一致性评价。2016年,易瑞沙在我国的销售额达到12亿元,是我国EGFR总销售额中最大的。现阶段,我国已有25家企业申请假冒。2、 (易瑞沙) 是由基因高科技(由罗氏回收)和安斯泰来产品开发的。它于2004年首次获得FDA批准,并在未来获得。获 EMA、FDA 和 CFDA 批准,是第一代 EGFR-TKI 阻滞剂。厄洛替尼作为单药适用于过去至少接受过一种有机化疗方法后的晚期、中晚期或迁移扩散的部分患者。药物最常见的副作用:皮疹和腹泻,大部分为I/II级,可操作,无需干扰治疗。注意事项:间质性肺病;腹泻,干燥,电解质紊乱和肾功能衰竭; 脑损伤事故;血小板减少症引起的毛细血管溶血性贫血; 肝炎疾病,肝功能衰竭; 肝功能异常和肝脏功能障碍疾病患者;大疱性或剥脱性皮肤变化;眼部疾病等。厄洛替尼仅在我国进口。现阶段已有30家企业申请仿制。2016年,厄洛替尼在我国的销售额达到4亿元。易瑞沙在我国的销量远高于厄洛替尼,但在国外则相反。我国境外销售差价的基本原则,
中晚期或既往接受至少一种器质性化疗后迁移扩散。以往有机化疗的重点是铂类协同有机化疗。药物最常见的副作用:皮疹、腹泻和谷丙转氨酶升高,多为I/II级,一般在服药后1-3周,一般是可逆的,不需要处理,它可以自动消失。注意事项:间质性肺病、肝毒副作用、腹泻、恶心、恶心和呕吐。埃克替尼是中国首个自主研发的EGFR-TKI缓释剂,2016年在中国的销售金额为7亿元,虽然不及易瑞沙,但远超厄洛替尼。4、阿法替尼(吉特瑞,) 阿法替尼是勃林格殷格翰公司开发的产品,2013年开始获得FDA批准,并获得EMA、PMDA和CFDA的批准。它是第二代 EGFR-TKI 阻滞剂。
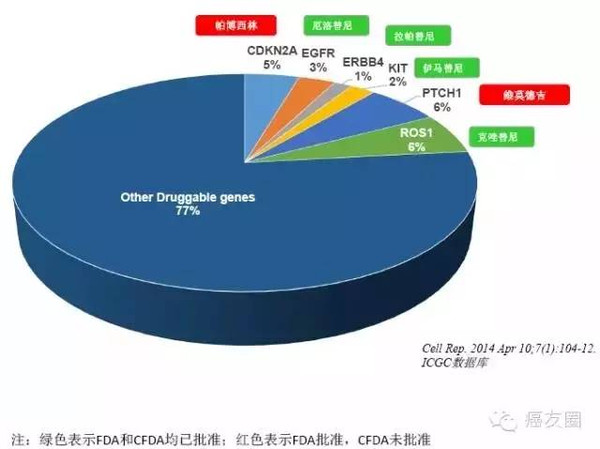
阿法替尼用作 EGFR 外显子 19 缺失或外显子 21() 替代基因突变的一线治疗。药物最常见的副作用:腹泻、皮疹、口腔溃疡、指甲沟、皮肤干燥、食欲下降和瘙痒。注意事项:腹泻、剥脱性大疱性皮肤病、间质性肺病、肝毒副作用、结膜炎。阿法替尼仅在我国进口,2022年获准进入市场,现阶段已有19家企业申请假冒。由于二代药物不良反应与一代相比
它太大了,无法处理第一代药物承受药物的问题。现阶段,二代药不受青睐。5、 (,) 是由阿斯利康 () 产品开发的。它于2015年首次获得FDA批准,随后投放市场。它还获得了 EMA、PMDA 和 CFDA 的批准。,是第三代EGFR-TKI阻滞剂。奥希替尼主要用于治疗一些既往接受EGFR-TKI治疗或治疗后确诊EGFR基因突变的晚期、中晚期或迁移性和扩散性成人疾病患者。药物最常见的副作用:腹泻、皮疹、皮肤干燥和指甲毒副作用。注意事项:基因突变阳性,间质性肺病,QTc间期增加,和心脏收缩力的变化。AURA科研数据显示客观缓解率为66%,6个月后疾病降低78%,疾病控制率91%,无病发展生存时间9.7个月。我国亚组:客观缓解率59.7%,延迟时间(3个月以上)89.9%,控制发病率88.2% . 奥希替尼可以摆脱申请后出现的一、二代药物,但奥希替尼在申请一年后会导致基因突变接受药物。现阶段还没有能够摆脱奥希替尼药物。的药品投放市场。奥希尼布仅在我国进口,2022年将获准上市。现阶段,没有高新技术企业申请假冒。6、奥莫替尼() 奥莫替尼于2016年获得韩国食品药品安全部(MFDS)批准,是第三代EGFR-TKI阻滞剂,用于治疗晚期、中晚期或迁移扩散基因突变。积极的。该化学物质最初是由韩美制药工业开发的。2015年11月,再鼎医药获得中国大陆(含港澳地区)产品研发、制造及商业化的控制权。2016年5月,再鼎医药向CFDA提交了临床用药申请(1.1化学药),产品开发代码为ZL-2303。有消息称,在奥莫替尼整个临床试验过程中,有两名患者因相对严重的药物不良反应死亡。研究药物论文参考文献:<@1、 Chen。在,2015.CA:
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话