欢迎光临吉康旅!
SCI论文():
【摘要】目的:观察贝伐单抗联合化疗对晚期结直肠癌患者的治疗效果。方法:选取80例晚期结直肠癌患者作为研究对象,按照随机数字表法分为对照组和观察组各40例。对照组给予化疗,观察组在对照组基础上给予贝伐珠单抗注射液治疗。比较两组治疗前后的客观缓解率和肿瘤标志物[癌胚抗原(CEA)、碳水化合物抗原125()、细胞角蛋白19片段(-1)和糖原抗原19-9(CA19-<) @9)) 水平和不良反应发生率。结果:
【关键词】贝伐单抗;化疗方案;先进的; 结直肠癌; 肿瘤标志物;客观反应率;不良反应
0 前言
结直肠癌初期缺乏典型症状,肿瘤体积增大可改变患者的排便习惯,导致腹泻、便秘、便血等,并可能出现消瘦、贫血等全身反应。晚期,危及患者生命安全[1]。晚期结直肠癌患者通常失去了最佳手术时间,经常接受化疗。化疗方案(伊立替康+氟尿嘧啶+亚叶酸)是常用的化疗方案。贝伐单抗是一种单克隆抗体,对血管内皮生长因子有抑制作用[2]。本文观察贝伐单抗联合化疗治疗晚期结直肠癌患者的效果。
1 材料与方法
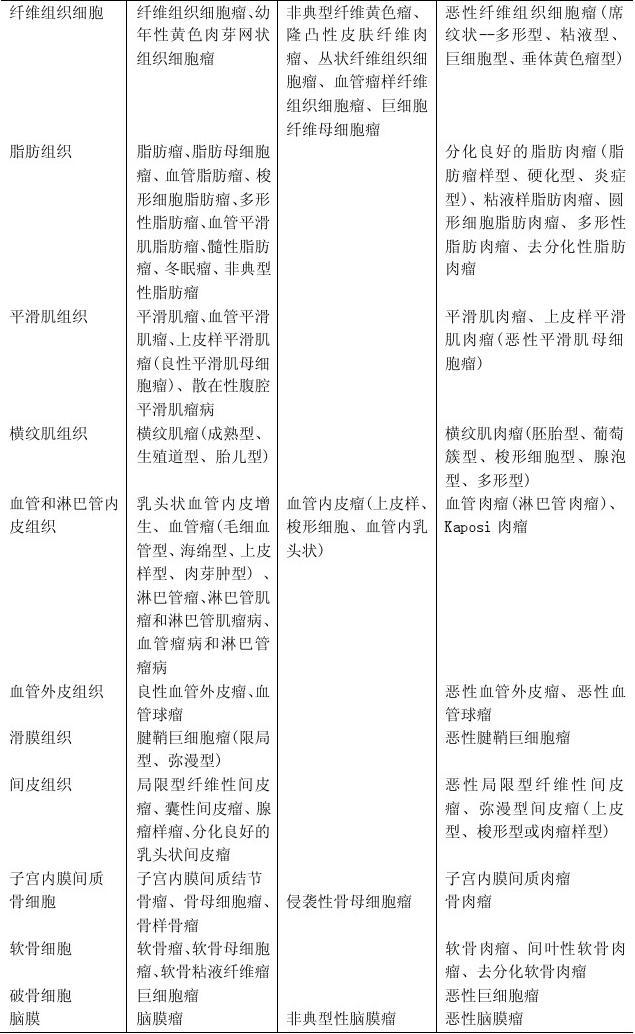
1.1 一般资料 选取2018年2月至2020年2月我院收治的80例晚期结直肠癌患者作为研究对象。纳入标准:经结肠镜检查、X线钡剂灌肠及组织病理学检查证实,符合《消化系统恶性肿瘤的诊断与治疗》中结直肠癌的相关诊断标准[3]; 预计生存时间> 6 个月。排除标准:严重器质性疾病者;患有其他类型的恶性肿瘤者;那些正在接受其他治疗的人;临床资料不全者及中途退出者。患者及其家属了解本研究内容并自愿签署知情同意书,本研究获得本院伦理委员会批准(批号:)。根据随机数字表法将他们分为对照组和观察组,每组40例。对照组男性22人,女性18人;年龄40~75岁,平均(60.12±6.56)岁;病程6-25个月,平均(15.27±2.44)个月;疾病类型:结肠癌19例,直肠癌21例;分化程度:低分化8例,中分化22例,10例高分化病例 观察组男24例,女16例;年龄42-74岁,平均(60.32±6.45)岁;平均8 -24 个月,
1.2 方法 对照组给予化疗。盐酸伊立替康注射液[齐鲁药业(海南)有限公司,国家药品标准,2mL:40mg]/m2,第一天静脉注射。第1~2天:注射用左叶酸钙(齐鲁药业,国药标准,25mg)/m2,静脉滴注1小时;注射用氟尿嘧啶(海南中化联合药业有限公司,国家药品标准,0.5 g)600 mg/m2,静脉滴注22小时。每2周重复一次为一个周期的化疗,共3个疗程。
观察组在对照组[()有限公司,注册号,(16mL)/瓶]静脉滴注治疗的基础上联合贝伐珠单抗注射液,5mg/kg,每2周重复1次为1一个化疗周期,共3个治疗周期。
1.3个观察指标(1)比较两组临床疗效[4]。完全缓解:所有可见的靶标和非靶标病灶完全消失并维持≥4周;部分缓解:基线病灶总长度减少≥30%并维持≥4周;稳定:基线病灶总长度减少20%,或出现新病灶客观缓解率=(完全缓解+部分缓解)例数/总病例数×100%。(2)比较两组治疗前后肿瘤标志物水平,包括癌胚抗原(CEA)、糖类抗原125()、细胞角蛋白19片段(-1) 和糖原抗原 19-9)(CA19-<@9) 水平。(3)比较两组不良反应发生率。
1.4 统计方法采用SPSS 21.0软件进行统计分析,测量数据表示为(x—±s),采用t检验,计数数据表示为率(%),采用χ2测试到 P
2 结果
2.1 两组临床疗效比较观察组客观缓解率为52.50%(21/40),明显高于27.50%的对照组(11/40),差异有统计学意义(P
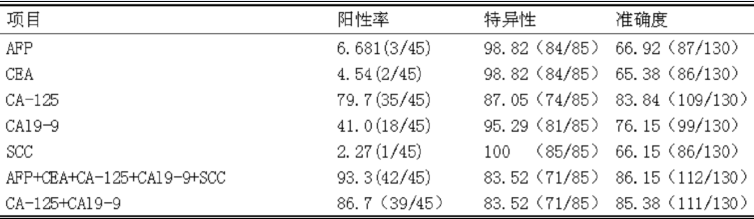
2.2 两组治疗前后肿瘤标志物水平的比较。治疗前,两组CEA、-1、CA19-9水平比较差异无统计学意义(P>0.05);治疗后,CEA、- 1、CA19-9 两组均低于治疗前,且观察组显着低于对照组,差异有统计学意义(P
2.3 两组不良反应发生率比较对照组不良反应发生率为10.00%,观察组不良反应发生率为5.@ >00%,两组不良反应发生率比较,差异无统计学意义(P>0.05)。见表3。
3 讨论
晚期大肠癌患者不能接受手术治疗。药物化疗可用于改善其临床症状。临床上经常使用化疗。然而,这个程序在杀死肿瘤细胞的同时,也会破坏正常的组织细胞,使人体的免疫系统受到损害。损失[5]。贝伐珠单抗是一种分子靶向药物,可以竞争性结合VEGF受体,抑制新生血管的形成,降低血管通透性,从而控制疾病的进展[6]。
本研究结果显示,观察组的客观缓解率高于对照组,提示贝伐珠单抗联合应用可提高晚期结直肠癌患者的治疗效果。CEA是常用的肿瘤标志物,其水平随肿瘤分化或转移呈上升趋势;可用于判断多种癌症,尤其是消化系统恶性肿瘤的发生发展和治疗效果;CA19-9是消化系统肿瘤的高特异性抗原之一,其水平升高提示大肠癌进一步发展;-1的水平可以随着大肠癌细胞的转移而增加[7]。本研究的结果还表明,CEA、观察组-1、CA19-9低于对照组。原因是贝伐珠单抗可抑制肿瘤组织血管内皮生长,从而破坏肿瘤组织的血供,降低血清肿瘤标志物水平[8]。本研究的结果还表明,两组不良反应发生率无统计学差异。建议联合贝伐单抗治疗不会增加安全风险。本研究的结果还表明,两组不良反应发生率无统计学差异。建议联合贝伐单抗治疗不会增加安全风险。本研究的结果还表明,两组不良反应发生率无统计学差异。建议联合贝伐单抗治疗不会增加安全风险。
综上所述,贝伐珠单抗联合化疗治疗晚期结直肠癌可提高客观缓解率,降低肿瘤标志物水平,其效果优于单独化疗。
参考
[1] 林延平,龙廷峰,周永春,等。2005-2014年云南省肿瘤医院结直肠癌临床流行病学特征趋势分析[J]. 中国癌症, 2020, 29 (7): 497-502.

[2] 聂俊峰,刘晓华,王翠英,等。贝伐单抗联合化疗对可切除结直肠癌患者细胞增殖因子表达的影响及临床疗效分析[J]. 肿瘤药学, 2019, 9 (1):76-81.
[3]许希明,周中银,杨继远. 消化系统恶性肿瘤的诊治[M]. 北京:科学出版社,2009:21-22.
[4]杨学宁,吴一龙。实体瘤疗效评价标准-[J].循证医学, 2004, 4 (2): 85-90.
[5] 曾立贤,林泽龙,梁宏光.奥沙利铂联合卡培他滨同步放化疗治疗晚期直肠癌的临床效果观察[J]. 中国实用医学, 2020, 15 (21) :131-133.
[6] 魏荣,周江华,李勤.贝伐单抗治疗结直肠癌的研究进展[J]. 癌症进展, 2020, 18 (23): 2388-2391.
[7] 郝元元.贝伐单抗联合化疗治疗晚期结肠癌的效果及对细胞免疫功能的影响[J]. 中国现代医学应用, 2019, 13 (14): 114-116.
[8] 王玉英,朱晓峰,薛玉玲,等。4项凝血项与肿瘤标志物联合检测在结直肠癌中的临床意义及诊断价值[J]. 现代肿瘤医学, 2019, 27 (4): 615-618.
关注SCI论文创作与发表,寻求SCI论文修改润色、SCI论文代发表等服务支持,请锁定SCI论文网!
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话