欢迎光临吉康旅!
肿瘤靶向治疗的研究进展突飞猛进,但都逃不过耐药性的魔爪。第一代→第二代→第三代TKI(靶向药物)耐药后,患者似乎筋疲力尽。幸运的是,基因检测技术(如NGS)的进步给耐药患者带来了新的希望,精准、精准、精准地打破了传统的TKI顺序用药思维。在某一突变类型(如EGFR)中,对某一基因型的异常进行进一步细化,利用该位点的有效TKI进行治疗。
有很多临床病例报道,部分患者在TKI耐药第三代后第一代已见效。今天小编就带大家一睹各种EGFR/ALK/ROS1/MET突变的神奇精准用药治疗案例。
EGFR文章
用第一代药物拯救奥希替尼耐药突变,吴一龙/陆顺教授国内真实案例验证
说到EGFR,目前市面上最强的TKI就是众所周知的第三代TKI奥希替尼()。三代耐药后怎么办?首先要明确耐药机制,才能对症下药。
1.奥西替尼用于初始治疗,单突变介导的耐药性;二线使用,/共突变介导的耐药性
突变是奥希替尼耐药的主要原因。然而,奥希替尼的不同用途引起的突变是不同的。
研究发现,奥希替尼用于一线和后线应用时(即1/2代耐药后发生突变时),引起的突变结构不同。
奥希替尼用于一线(初始治疗)时,由于是直接抑制,耐药后只会出现单突变(不伴随),第一代TKI治疗有效。
奥希替尼用于后排。耐药后出现的共突变(和同时)分为顺式(cis)和反式()两种结构,其中反式结构可用于1代+3代处理,情况为详细显示如下。
2.奥希替尼一线耐药后出现单突变,第一代TKI治疗可逆转耐药!
第一代TKI(易瑞沙、特罗凯、)对单突变治疗敏感,临床病例也有报道。
一名 78 岁女性晚期肺腺癌患者在服用阿法替尼 30 个月后出现耐药。发现有突变,用了奥西替尼,7个月后进展,基因检测阳性,但阳性,无突变。基于未发生突变,患者再次挑战1代吉非替尼(/天)以达到部分缓解PR。
图A为阿法替尼治疗前后对比,图B为奥西替尼治疗前后对比,图C为吉非替尼治疗前后对比。
虽然本案二线并未使用奥希替尼,但理论上奥希替尼一线应用只会出现单突变,只需使用一代药物即可挽救。耐药后,可能会检测到突变。 可以再次使用。通过这种药物顺序安排,患者可以有两次机会受益于奥希替尼。所以,从耐药机制来看,其实还是建议尽早使用奥希替尼,耐药后的治疗比较简单。
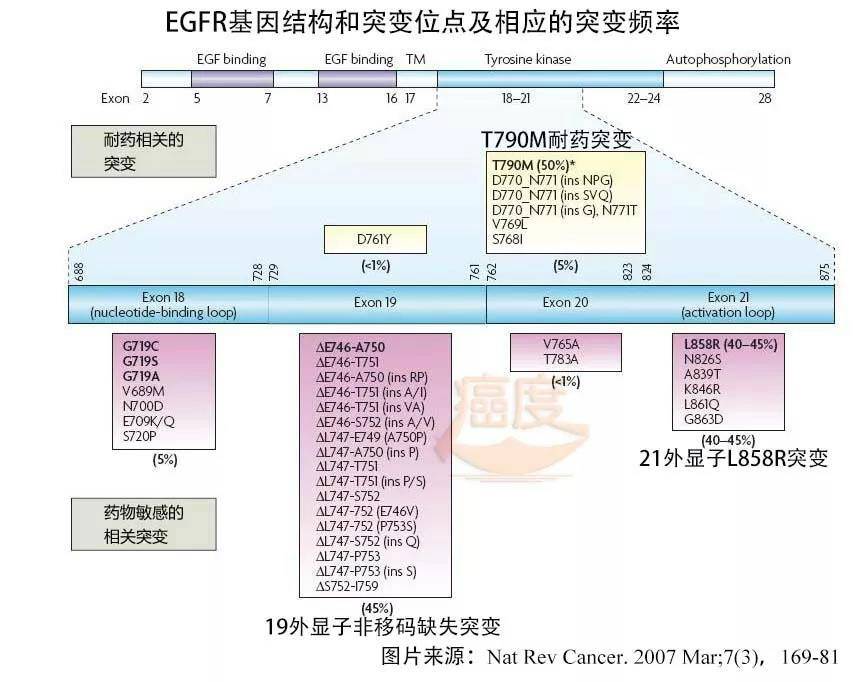
3. -采用1+3代,吴以龙教授/陆顺教授精彩案例展示
今年,吴一龙教授团队在JTO上发表了国内首例转突变完整治疗案例。患者为一名 44 岁男性,患有肺腺癌。接受阿法替尼治疗后发现突变,他接受了奥希替尼治疗。7.四个月后,病情恶化,NGS检测发现了19个del和3个突变。它是一种反式突变。患者接受了第一代和第三代TKI治疗(厄洛替尼+奥希替尼)。1周内症状明显缓解,1个月后突变消失,2个月后突变消失。CT 也显示部分缓解。三个月后又进展,出现顺式突变。用阿维替尼、化疗+贝伐珠单抗治疗后,脑膜进展,顺式和反式共存。反式丰度更高。患者接受了三代和一代TKI治疗,次日头痛呕吐立即缓解。该患者于2018年9月因脑膜进展而去世,从确诊晚期肺癌开始的总生存时间达到3.7年。
陆顺教授最近也在JTO杂志上发表了国内的嬗变疗法案例。一名 42 岁女性肺腺癌患者在多线耐药(厄洛替尼、化疗)后接受奥希替尼治疗。3年后出现耐药,共突变,转结构,1代+3代治疗,联合贝伐珠单抗8个月。
总结:奥希替尼耐药并不是死胡同。首先,必须明确耐药机制,寻找次要驱动基因突变。突变是产生耐药性的部分原因。对于单突变和转突变结构,可采用1代±3代进行处理。总之,耐药的治疗还是很讲究个体化、靶向用药的,动态基因检测是最好的“指南针”。
ALK篇
洛拉替尼耐药后用克唑可挽救,精准用药可为ALK患者带来长期生存
多项研究表明,ALK阳性患者的生存期可超过6-7年。这不是偶然的,也不是单独一个强TKI的结果,而是多个ALK-TKI的结果。
虽然不同的1/2/3代ALK-TKI针对的是ALK靶点,但每种药物对不同ALK亚型的敏感性差异很大,这也提醒我们在耐药后要积极寻找异常部位,选择对治疗最敏感的目标TKI出人意料地获胜。跳出传统的1代→2代→3代顺序用药模式,可以更灵活地切换到最有效的TKI,同时解决三代耐药后无药可用的困境。
下表显示了几种ALK靶向药物对不同基因位点的IC50(数字越小,对肿瘤的敏感性越好,绿色=更敏感,黄色=中度敏感,红色=不敏感)。
1.劳拉出现耐药后,用克唑替尼逆转耐药
一名52岁女性ALK重排患者在克唑替尼耐药后接受二代TKI色瑞替尼治疗,再次进展后接受化疗(卡铂-培美曲塞)治疗,6个月后出现缓解。复发后再次接受克唑替尼治疗无效,参加了劳拉替尼的临床试验,肿瘤缩小。八个月后,肝转移恶化,总胆红素水平升高(0.8mg/dl)。劳拉被迫停药。患者接受低剂量长春瑞滨治疗未见缓解。
基因检测显示存在两个耐药突变 (-),表明克唑替尼可能再次易感。患者再次开始使用克唑替尼,效果显着。随着肝功能衰竭的好转,患者的临床情况迅速好转。出院后继续接受克唑替尼维持治疗,效果持续6个多月。
印度廉价抗癌药的对与错
印度仿制药抗癌药被称为医药界的“超级A货”,因为其价格只有合法“洋药”的十分之一甚至更少,因此买不起药的患者跃跃欲试为他们。. 然而,这些仿制药被认为是“假药”,因为它们在中国没有被批准。近日,南京一对夫妇因代购销售印度抗癌药而被检察院起诉。因为没有专利
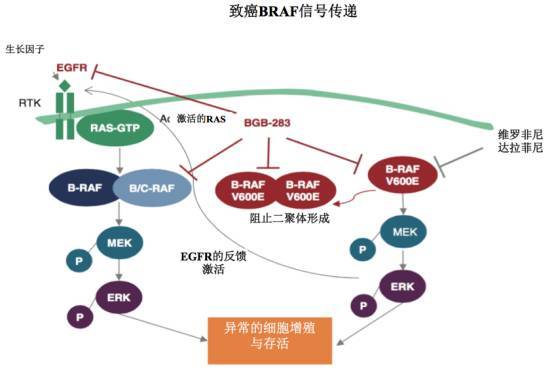
图A为患者的治疗史;图B为劳拉替尼治疗前后的CT图像,从左到右:劳拉替尼治疗前、劳拉替尼治疗后缓解、劳拉替尼耐药、克唑替尼再次挑战治疗后缓解
2.劳拉发现耐药后“MET扩增”罪魁祸首,巧妙使用克唑啉逆转病情,活了6年多
2012 年 10 月,一名 40 岁女性晚期肺腺癌脑-ALK 重排患者在放疗后接受克唑替尼治疗,进展后接受培美曲塞 + 卡铂治疗。再次进展后,他接受了第二代TKI 治疗。耐药后,使用多西他赛和克唑替尼无效。2016 年 6 月,该患者参加了劳拉替尼试验。9个月后,纵隔淋巴结缓慢增大,继续使用劳拉替尼7个月。考虑到可能发生多发转移,医生建议进行全身治疗。患者拒绝化疗(之前化疗的副作用比较大)。考虑到已有克唑啉复治成功案例,患者对克唑啉耐受性较好。2017年10月再次使用克唑替尼,效果良好。目前已实现PR部分缓解14个多月,已活了6年多。
为了探究耐药的原因以及克唑啉药效的原因,研究人员对治疗前后患者的脑部病变和淋巴结进行了Dx Test的NGS基因检测,发现所有样品显示出高 MET 蛋白。表达。然后用v3检测治疗后的纵隔淋巴结病灶标本,发现ALK-和MET扩增(2.61)。结果还显示MET通路的异常是 Ni耐药的原因,克唑替尼可以同时针对ALK和MET靶点,有效攻克耐药性。
总结:从以上两例ALK阳性病例来看,虽然ALK-TKI的种类很多,但还是要合理安排用药顺序,解决耐药问题。仍然需要寻找耐药性的二次突变,并针对不同的靶点给出相应的TKI。对待。此外,靶向耐药后,必须注意其他通路的激活,如MET扩增。只有及时的基因检测和精准的用药才能实现长期生存。
ROS1
克唑啉耐药机制大盘点,从基因检测角度分析耐药后个体化治疗
克唑替尼是唯一获得 FDA 批准的用于 ROS1 重排/融合的靶向药物。耐药后机制复杂,如何处理是临床难题。然而,目前有多种 ROS1-TKI 正在开发中(包括劳拉替尼、卡博替尼、恩曲替尼、色瑞替尼等)。近日,SCI还发表了对克唑啉耐药机制的解释。让我们来看看。
1.ROS1点突变是克唑类耐药的主要原因,可通过新的靶向药物治疗
ROS1阳性耐药的机制包括EGFR、KIT等旁路激活,以及下游通路异常(如RAS/RAF/MEK通路、PI3K通路、JAK/STAT通路等)。此外,点突变,如,,/F,和。
对于旁路和下游信号激活的患者,可选择化疗或新一代ROS1-TKI。对于 ROS1 点突变,不同的亚型对应不同的 TKI 治疗敏感性。例如,最常见(占 80%)的潜在可用靶向药物是卡博替尼。每个位点突变的治疗药物选择不同,如下表所示。
2.ROS1耐药序贯治疗案例展示,体现精准用药理念
在另一篇新发表的 SCI 文章中,我们还总结了 ROS1 突变亚型的 TKI 敏感性。
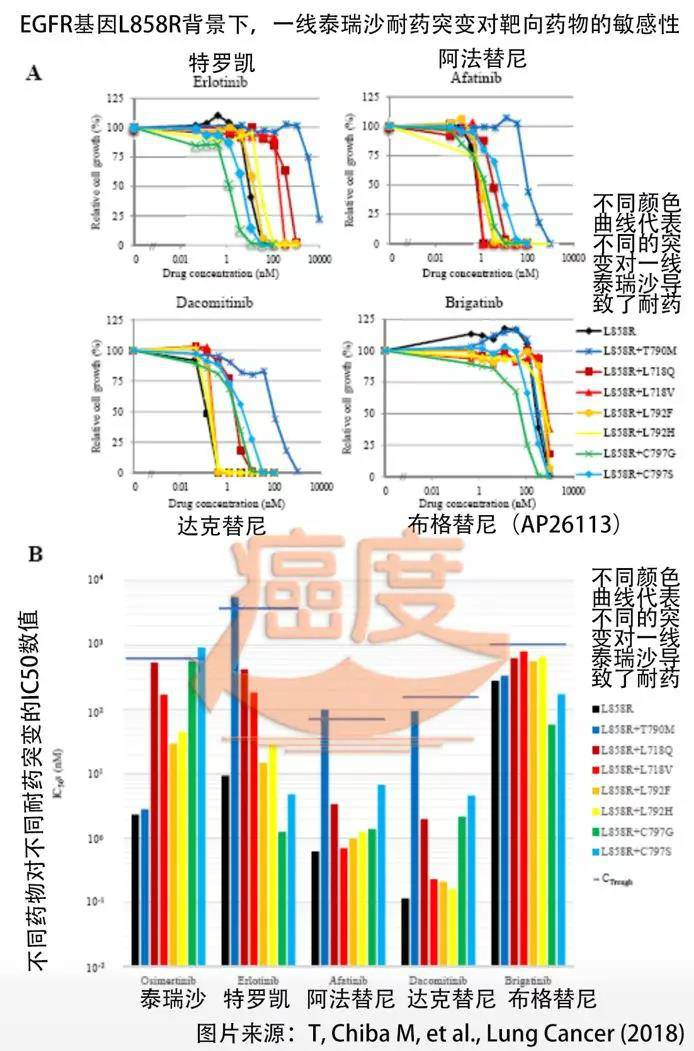
下表显示了不同位点突变的ROS1-TKI的IC50(数值越低灵敏度越好,绿色=更敏感,黄色=中度敏感,红色=不敏感),标记*表示它有发生在患者身上。, $ 表示在生物信息学模拟中发现的。
与EGFR/ALK靶点不同,ROS1市场上靶向药物较少,耐药性处理困难,病例报告较少。编辑器将向您展示一个 ROS1 案例。虽然失败了,但是整体的治疗方法是明确的,大家都可以使用。参考。
2017年1月,一名59岁的ROS1融合、一线克唑替尼耐药的女性患者接受了劳拉替尼治疗。2018年1月,病情有所进展。胸膜活检显示 ROS1- 突变,没有发现其他途径的激活。由于研究表明卡博替尼是敏感的,因此患者接受了卡博替尼 60 毫克/天的治疗。由于2级恶心和肌痛,剂量不能进一步增加到标准剂量(/天)。肿瘤继续进展,患者接受卡铂+培美曲塞化疗,培美曲塞维持治疗。进展后,肝脏病变的基因检测显示 ROS1 突变仍然存在,没有其他途径被激活。患者接受卡铂+紫杉醇治疗,2个周期化疗后病情进展。
总结:ROS1靶向进展不如EGFR/ALK快,但治疗模式也遵循“精准”二字,靶向TKI给药也是未来耐药治疗的发展方向。在这种情况下,当反复确保没有其他途径被激活时,卡博替尼的使用未能缓解疾病的进展。研究人员首先认为患者不能耐受标准剂量的卡博替尼,导致疗效不够。但是,在病例中使用动态基因检测指导用药的想法值得借鉴。
MET文章
吴义龙教授用卡博替尼+奥希替尼挽救MET继发突变引起的克唑替尼耐药
患者,女性,44岁,IV期肺腺癌,EGFR突变,吉非替尼治疗后发生突变,转用奥希替尼治疗。第一次液体活检显示 MET 扩增、突变和奥希替尼联合克唑替尼治疗,实现了 PR 的显着改善(图 A)。3个月后病情复发。患者进行了第二次基因检测,发现MET获得性耐药突变,/H,突变伴随着突变,是新的突变,以前没有报道过。患者同意试验药物并开始使用卡博替尼(每天 80 毫克)联合奥希替尼进行治疗。一周后,呼吸困难和不适症状缓解,可以下床活动,体力逐渐恢复,并且减少了疾病的焦点。. 一个月后,病情恶化,第三次液体活检发现突变,而其他三个突变消失,突变从44%增加到65%。
计算机预测分析显示/H/V和位点突变导致对克唑替尼耐药,但对卡博替尼影响不大。然而,单独的突变会导致 MET 蛋白的环结构域不稳定,影响卡博替尼的疗效解释了患者的进展。
总结:本案例完美诠释了动态基因检测指导用药的精髓。奥希替尼耐药后MET的激活是通过组合方式控制的,然后MET耐药对克唑啉的共突变,随后吴教授巧妙的改用对这个位点敏感的卡博替尼,挽救你的生命。最终分析还揭示了卡博替尼耐药的分子原因。
总结
从肺癌EGFR/ALK/ROS1/MET靶向耐药的案例来看,耐药的原因层出不穷,极其复杂。要选择最合适的治疗方案,动态基因检测是非常必要的。只有找到“凶手”才能破案!
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话