欢迎光临吉康旅!
众所周知,肺癌的发病率和死亡率均居恶性肿瘤之首。在诊断时,65%-70% 的患者已经处于 IIIb/IV 期 [1]。晚期非小细胞肺癌患者的5年生存率()仅为15.8%左右[2],1年生存率仅为30%-40%。近年来,表皮生长因子受体(EGFR)突变靶向治疗取得突破性进展,为晚期患者带来新希望。吉非替尼是一种EGFR酪氨酸激酶抑制剂,是首个获批上市用于治疗局部晚期或转移性EGFR突变的靶向药物。但是,服用吉非替尼大约一年后,大多数患者会逐渐产生耐药性,而突变是最常见的原因。对于接受吉非替尼治疗后出现耐药性和突变的患者,奥希替尼的上市给了他们希望。它在临床实践中的应用如何?现在给大家分享一例老年男性晚期肺腺癌,吉非替尼治疗后改用奥希替尼。
案例信息
患者,男,71岁,2018年3月因反复咳嗽、咯血、声音嘶哑2个多月,胸部CT显示完美:左肺上叶软组织密度不规则肿块,边缘粗糙,边界清晰, 大小约7.9*7.8cm,增强扫描略增强不均,左侧上肺动静脉局部受侵,左侧有少量胸腔积液。经皮肺活检:“左肺组织”,发现腺癌。完成基因检测,EGFR突变检测显示19-del。
体检
ECOG评分1分,NRS评分0分,双侧颈部及锁骨上及浅表外淋巴结未触及肿大,胸腔正常,左上肺呼吸音稍低,余肺呼吸音清晰,未闻及准确干湿罗音,无胸膜摩擦;窦性心率,节律规律,各瓣膜无明确杂音,腹部检查阴性,下肢无肿胀,病理征阴性。
过去的历史
否认高血压、糖尿病病史。
初步诊断
左上叶腺癌伴淋巴结转移 IV 期 EGFR (+)、ALK/ROS1 (-)。
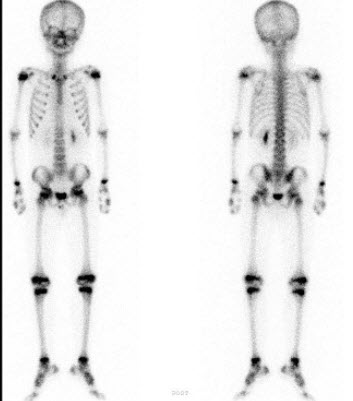
1.治疗后
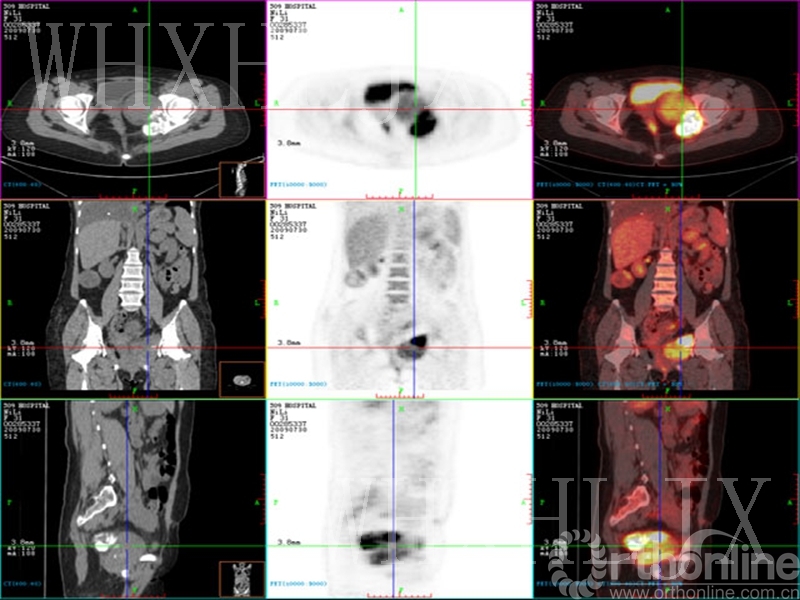
患者病情较晚,无手术指征。2018年3月27日开始口服吉非替尼qd靶向治疗,2018年5月复查CT(图片1),右肺肿块阴影较之前明显缩小,疗效评定为部分缓解( PR),继续吉非替尼靶向治疗,定期随访,患者出现骨痛,2019年5月8日复查CT(图片2):左肺上叶见不规则软组织密度肿块,分割较浅,边缘粗糙,最大横截面约5.3*< @3.5cm,增强扫描轻度不均匀增强;扫描多个颈椎、胸椎,双侧多发肋骨,双侧肩胛骨,右锁骨,右侧肱骨多发混合性骨破坏,考虑广泛骨转移患者病情进展,服用吉非替尼13个月以上,考虑耐药。耐药基因的第二次活检显示阳性突变。该患者于 2019 年 5 月 29 日开始服用奥希替尼 80 mg qd,并同时给予唑来膦酸抑制破骨细胞活性和抗骨转移治疗。患者疼痛症状减轻,骨转移症状改善。一个月后复查CT(图3),肺部病灶比以前小,建议患者继续第三代靶向药物治疗,定期复查随访。考虑广泛骨转移患者病情进展,服用吉非替尼13个月以上,考虑耐药。耐药基因的第二次活检显示阳性突变。该患者于 2019 年 5 月 29 日开始服用奥希替尼 80 mg qd,并同时给予唑来膦酸抑制破骨细胞活性和抗骨转移治疗。患者疼痛症状减轻,骨转移症状改善。一个月后复查CT(图3),肺部病灶比以前小,建议患者继续第三代靶向药物治疗,定期复查随访。考虑广泛骨转移患者病情进展,服用吉非替尼13个月以上,考虑耐药。耐药基因的第二次活检显示阳性突变。该患者于 2019 年 5 月 29 日开始服用奥希替尼 80 mg qd,并同时给予唑来膦酸抑制破骨细胞活性和抗骨转移治疗。患者疼痛症状减轻,骨转移症状改善。一个月后复查CT(图3),肺部病灶比以前小,建议患者继续第三代靶向药物治疗,定期复查随访。该患者于 2019 年 5 月 29 日开始服用奥希替尼 80 mg qd,并同时给予唑来膦酸抑制破骨细胞活性和抗骨转移治疗。患者疼痛症状减轻,骨转移症状改善。一个月后复查CT(图3),肺部病灶比以前小,建议患者继续第三代靶向药物治疗,定期复查随访。该患者于 2019 年 5 月 29 日开始服用奥希替尼 80 mg qd,并同时给予唑来膦酸抑制破骨细胞活性和抗骨转移治疗。患者疼痛症状减轻,骨转移症状改善。一个月后复查CT(图3),肺部病灶比以前小,建议患者继续第三代靶向药物治疗,定期复查随访。
图1 患者治疗前肺部CT(上)和服用吉非替尼2个月后肺部CT(下)
图2 2019年5月8日肺部CT
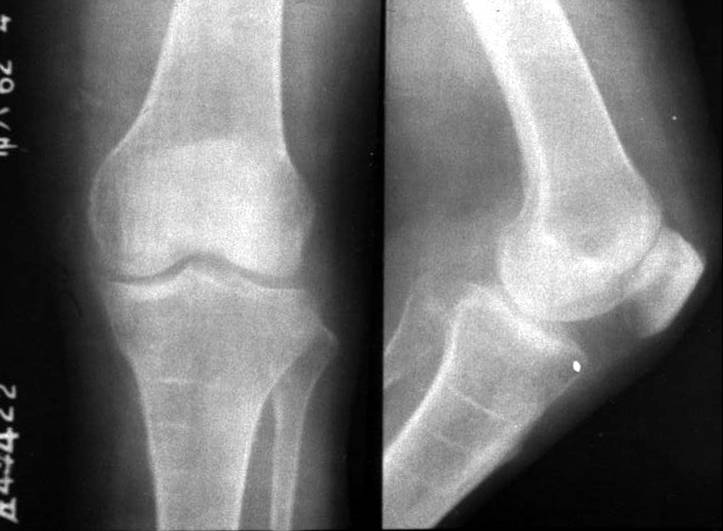
图3 2019年6月29日肺部CT
2.讨论
肺癌是世界上最常见的恶性肿瘤之一,约占肺癌总数的80%。但肺腺癌患者预后差,5年生存率低。高转移率是肺腺癌病死率高的重要原因。一般而言,患者在接受治疗时癌细胞已发生不同程度的转移[3]。铂类化疗的有效率仅为30%-40%,1年生存率仅为30%-40%。随着分子生物学技术的发展以及从细胞和分子水平对发病机制的进一步了解,肺癌靶向治疗进入了一个新时代。
患者中最常见的EGFR突变为外显子19缺失和外显子21突变。吉非替尼是首个获批上市用于治疗局部晚期或转移性EGFR突变的靶向药物。其作用机制可能是抑制EGFR酪氨酸激酶,从而阻断EGFR下游激活的细胞增殖和细胞迁移血管生成和细胞存活的信号转导过程[4]。吉非替尼治疗的中位 PFS 为 9. 6 个月。产生耐药性的原因有很多,但最常见的是突变,约占突变的60%。其他包括 HER2 扩增。、C-MET扩增、KRAS突变、BRAF突变、突变、EGFR 20外显子插入突变、转化为小细胞肺癌[5]。吉非替尼耐药后,建议进行第二次活检。对于有突变的患者,推荐使用奥希替尼。
奥希替尼一线治疗晚期EGFR敏感突变患者的中位PFS为18.9个月,OS接近39个月[6]。本研究的目的是比较奥希替尼与铂类联合培美曲塞化疗对EGFR-TKI治疗进展后EGFR突变阳性晚期患者的疗效和安全性。该研究纳入了来自18个国家和地区126个中心的419名患者,均在一线EGFR-TKI治疗失败后经活检证实为突变阳性。患者的中位年龄为 62 岁(20-90 岁),15% ≥75 岁,64% 为女性,32% 为白人,65% 为亚洲人,68% 不吸烟,所有患者PS 评分为 0 或 1,54% 的患者有远处转移,包括 34% 的脑转移,23% 的肝转移和 42% 的骨转移。所有患者以 2:1 的比例随机分组,接受奥希替尼(N=279,80 mg,每天一次口服)和铂类(N=140,[顺铂 75 mg/m2 或卡铂曲线下面积(AUC ) 5] 联合培美曲塞(500 mg/m2) 化疗,3周为1个周期,共6个周期;培美曲塞维持治疗)。主要研究终点是研究者对无进展生存期(PFS)的评估). 研究结果表明,奥希替尼治疗组的中位PFS显着高于铂+培美曲塞治疗组(10.1个月对比4.4个月;P< 0.001),差异有统计学意义,两组总体反应率(ORR)分别为65%和29%。
该研究是一项随机、双盲、国际多中心 III 期临床研究。共纳入556例既往未接受过任何治疗的局部晚期或转移性EGFR外显子19缺失或外显子突变患者,旨在评估奥希替尼与现行标准EGFR TKI方案(SOC组:吉非替尼或厄洛替尼)的有效性和安全性. 556例患者随机分为奥希替尼组(N=279)和SOC组(吉非替尼N=183,厄洛替尼N=94)。患者的中位年龄)64岁(26-9 3),54%的患者<65岁,63%的患者为女性,62%的患者为亚洲人,64%的患者为非吸烟者,5%的患者分期为IIIB,95%的患者分期为 IV,63% 的患者有 EGFR 外显子 19 缺失,37%的患者有EGFR外显子21突变,5名患者同时有突变。研究结果表明,两组的中位无进展生存期(mPFS)分别为18.9个月和10.2个月,具有显着的统计学差异。两组的总体反应率 (ORR) 分别为 77% 和 63%。两组的缓解持续时间(DoR)分别为17.6个月和9.6个月。
在患者出现吉非替尼耐药后,第二次活检基因检测显示阳性突变。换用奥希替尼后,效果明显。目前,奥希替尼已获批一线治疗适应症,为广大患者提供了额外的治疗选择,希望未来进一步提高患者的生存时间和生活质量。
参考
[1] 张明,蓝海涛,陈琳.培美曲塞联合奈达铂治疗70例肺腺癌的近期疗效及安全性评价[J]. 实用医院临床杂志。2014;3(2):111-11<@3.
[2] L, D,. ,2018.[J].CA:a for ,2018,68(1):7-30.
[3] DH, JH, Jr BP. 肺 [J]. J Clin .2014;32(10):973-82.
[4] M,LJ。::其在/非细胞肺中的应用[J].,2009,69(16):2303-2328
[5] EL, Tan SZ, Liu G, et al. 和 EGFR 与 EGFR-a [J]. Lung Res, 2015, 4 (1) :67-81.
[6] SS,YANG JC,LEE CK,et al. 作为EGFR-细胞肺的线[J].J Clin,2018,36(9):841-849.
以上内容仅供医疗专业人士阅读
CN- 日期:2020-2-24
【本站为非营利性学术交流平台,部分信息来源于网络。如有涉及版权问题,请及时联系管理员;所有文章仅用于公益交流,不代表本站。欢迎提供资料、资料等,投稿邮箱:一经采用,将收取一定的费用。】
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话