欢迎光临吉康旅!
人民网北京1月26日电(同)25日,国家食品药品监督管理总局在官网发布《关于修改吉非替尼片说明书的公告》(以下简称《公告》) 》)为进一步保障公众用药安全,国家药监局决定对吉非替尼片说明书中的【不良反应】和【注意事项】项目进行修改。
国家食品药品监督管理局发布的《吉非替尼片修订说明书要求》显示,添加【不良反应】包括上市后经验:吉非替尼片上市后观察到以下不良反应这些不良反应来自无法确定样本量的自发报告,并且难以准确估计其频率。皮肤及皮下组织异常:皮肤不良反应是吉非替尼片非常常见的不良反应之一,可发生于身体任何部位,通常表现为轻中度皮疹、干燥、瘙痒等。上市后不良反应反应监测已收到手掌足底红肿综合征(手足综合征、手足皮肤反应)的报告,表现为手掌和足底感觉异常、红斑、脱屑、水疱、出血、皲裂、水肿或角化过度等。
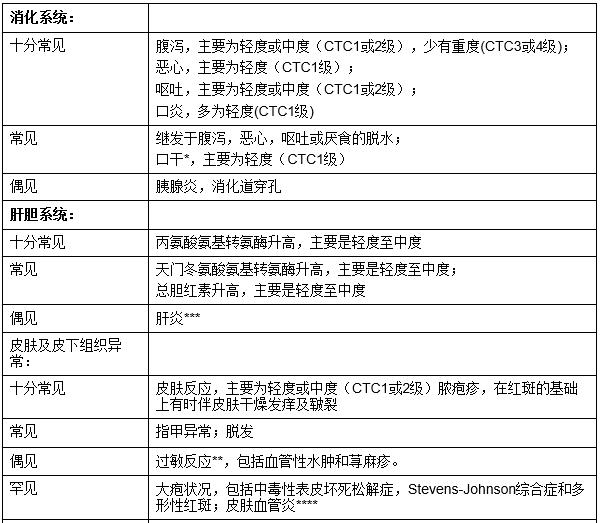
【注意事项】新增内容包括皮肤毒性:严重皮肤反应(NCI 3级以上)需暂停用药(见【用法用量】),皮肤反应早期干预有利于吉非替尼的持续治疗。用药期间出现皮肤感觉异常、红斑、脱屑、水疱、出血、皲裂、水肿或角化过度的患者应及时就医。上市后不良反应监测已收到手掌及足底肿胀综合征(手足综合征、手足皮肤反应)的报告。患者服药时应注意减少皮肤压力和摩擦,尤其要防止手掌和足底受压。 (注:手册其他内容如与上述修订要求不一致,应一并修订。)

《公告》要求各吉非替尼片生产企业按照《药品注册管理办法》等有关规定,按照药品说明书修改要求,提交说明书修改补充申请。吉非替尼片(见附件)。 2021年4月20日前报国家药品监督管理总局药品审评审批中心或省级药品监督管理部门备案。修改内容涉及药品标签的,应当一并修改;标签的使用说明及其他内容应与原批准内容一致。已出厂药品的说明书和标签应在补充申请提交之日起9个月内全部更换。

《公告》提醒吉非替尼片生产企业要深入研究新的不良反应发生机制,采取有效措施,开展使用和安全问题的宣传培训。涉及药品安全的内容变更应立即实施。以适当方式通知药品经营者和使用单位,引导医师、药师合理用药。临床医师和药师应仔细阅读吉非替尼片说明书的修订内容,在选择药物时,应根据新修订的说明书进行充分的获益/风险分析。患者应严格按照医生的处方用药,并在服药前仔细阅读说明书。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话
帕纳替尼(Ponatinib)是阿瑞雅德(Ariad)开发的三代BCR-ABL酪氨酸激酶抑制剂(TKIs),商品名为Iclusig。其经过一期和二期临床试验,...
伏立康唑属三唑类抗真菌药物,其抗菌谱广,抗菌活性高。美国感染疾病协会( IDSA) 2016年最新更新的指南中将伏立康唑作为侵袭性曲霉菌、...
瑞戈非尼/瑞格非尼(Regorafenib)是VEGFR酪氨酸激酶小分子抑制剂,是第一个证实的对生存有益的酪氨酸激酶抑制剂,可特异性与多个酪氨酸激酶...
商品名:Lynparza(利普卓) 通用名:olaparib(奥拉帕尼/奥拉帕利) 靶点:PARP 原研厂家:阿斯利康 规格:150/100mg ...
随着分子生物学技术的飞速发展,学术界对髓母细胞瘤的分子分型有了较为深入的研究。2016年WHO分类标准将髓母细胞瘤分为三个亚型,即WNT型...








