欢迎光临吉康旅!
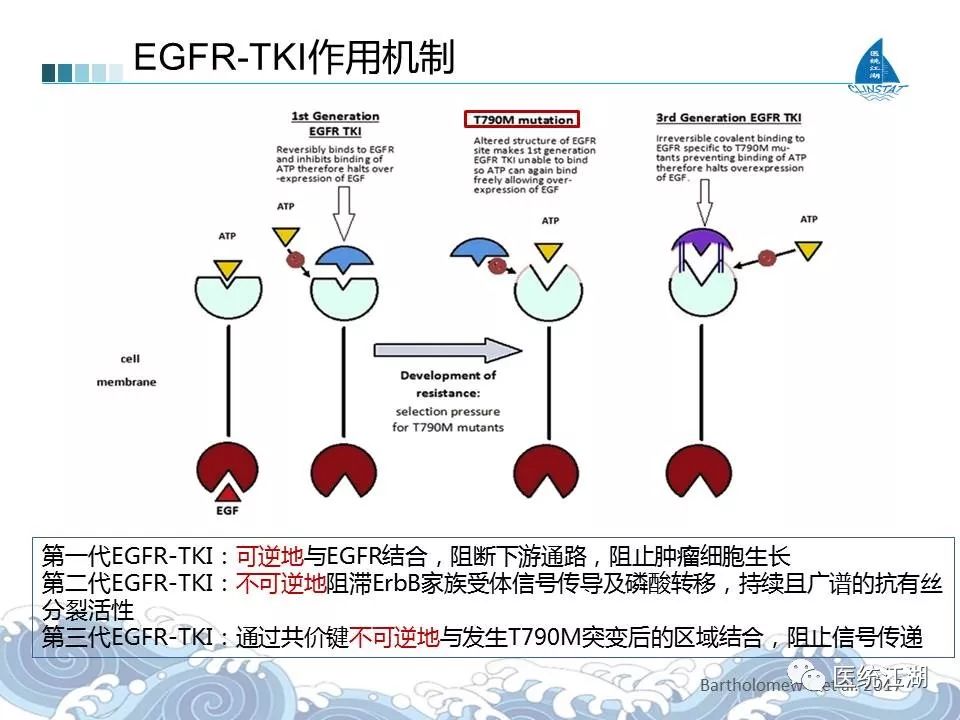
对于 EGFR
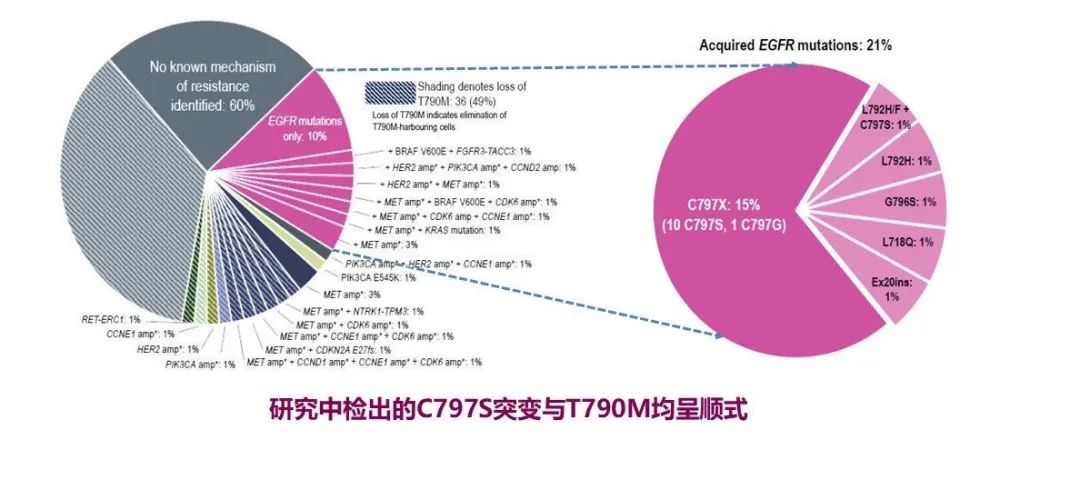
外显子 19 突变或点突变的患者,第一和第二代表皮肤生长因子受体 (EGFR) 酪氨酸激酶抑制剂 (TKI) 可以提高其客观缓解率 (ORR) 和无进展生存期 (PFS),但大多数患者将在治疗后 9 至 13 个月内产生获得性耐药。疾病进展时,约60%的患者出现编码EGFR突变的外显子20点突变,这是获得性TKI获得性耐药的主要机制。
奥西替尼()作为第三代EGFR拮抗剂,在治疗EGFR突变激活患者和酶功能相对保留的野生型患者方面优势明显。在I期奥希替尼试验(剂量增加组)中,138例患者中有127例发生突变,奥希替尼治疗组的有效疾病控制率可达61%(95%CI,52-70),中位数生存时间 (PFS) 为 9.6 个月。在 AURA
在第 2 项试验中,突变阳性患者每天服用 80 毫克奥希替尼(推荐剂量)。 199例患者客观有效率69%,中位生存期9.9个月。 2015年11月,美国FDA食品药品监督管理局批准奥希替尼作为EGFR-TKI治疗后出现进展的患者的治疗方案,但很多国家并不认可这组药物的结果,还需要更多的实验来证实,光环
3 提供了一项随机、开放、国际 3 期试验,比较了奥希替尼和铂类联合培美曲塞治疗晚期非鳞癌患者和第一代或第二代 EGFR-TKI 治疗突变患者的疗效。
这项随机研究比较了 279 名接受奥希替尼治疗的患者和 140 名接受铂类联合培美曲塞治疗的患者的预后。最常见的EGFR-TKI是吉非替尼>厄洛替尼>>阿法替尼。有脑转移但无症状或稳定的患者也包括在研究中(不需要治疗)。对于疑似脑转移的患者,进行中枢神经系统成像。铂类联合培美曲塞化疗4个周期后,未进展的患者继续接受培美曲塞维持治疗(约占初始治疗患者的54%)。在研究开始后 4 个月进行评估和调整。铂类联合培美曲塞治疗的患者客观疾病进展后,可转为奥赛替尼组(约60%的患者)。
无进展生存期是研究的终点。奥希替尼组中位时间为10.1个月,铂类联合培美曲塞组中位时间4.4个月[危险比(HR)0.30;
95% CI,0.23-0.41;
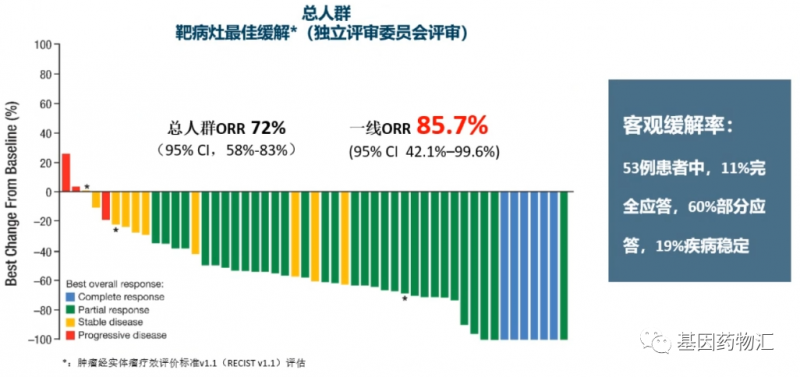
65-76) 明显优于铂类联合培美曲塞组(31%;95% CI,24-40)(优势比,5.39; 95 % CI,3.47-8.48;
P
3.0-5.6),总体生存数据尚不完整。
在药物安全性和副作用方面,与联合化疗组相比,奥希替尼组很少出现3级以上的药物副作用(23%
对比 47%)。在奥希替尼组中,常见的副作用包括恶心 (41%)、皮疹 (34%)、皮肤干燥 (23%) 和甲沟炎 (22%)。在联合化疗组中,最常见的副作用是厌食 (49%)、食欲不振 (36%)、便秘 (35%) 和贫血 (30%)。奥希替尼治疗组间质性肺的发生率为 4%(9 名患者出现 1 级或 2 级和 1 级死亡),而联合化疗的发生率为 1%。奥希替尼组QT间期延长事件发生率为4%(均为1级或2级,仅1例为3级),联合化疗组发生率为1%(≤2级)。与联合化疗组相比,奥希替尼很少因副作用而停药(7%
对比10%)。
为什么要通过临床 III 期随机试验来比较奥希替尼和联合化疗的效果?
当然,AURA
3项试验有效证明奥希替尼对EGFR突变阳性患者疗效较差。结果并不意外,但AURA
3 试验最大的问题可能是监管机构为什么首先进行试验来验证疗效。
在使用EGFR-TKI的EGFR突变患者中,各III期试验比较了第一代或第二代EGFR-TKI联合一线铂类治疗的疗效,结果显示EGFR-TKI在ORR方面具有优势和 PFS 优势 (1-4, 12-15)。在两项关于奥希替尼治疗 -EGFR 突变患者疗效的独立研究中,奥希替尼与第一代或第二代 EGFR-TKI 进行了比较。临床效果较好,因此应从AURA开始
3 在实验过程中获取我们还不清楚的信息。并且试验的初步数据通过研究终点预测了奥希替尼在试验中的作用。然而,对化疗耐药的分子机制的研究仍在进行中,最重要的是探索突变患者化疗的机制。
试验中所有偏差的质量控制。试验中,将患者随机分为铂类联合培美曲塞治疗组,分析突变是否影响联合化疗对EGFR突变患者的疗效。客观地说,这是有争议的。一方面,在EGFR酪氨酸激酶抑制的情况下,突变可以理解为重新建立EGFR信号和下游信号通路,增加对化疗的敏感性。另一方面,突变中EGFR激酶信号通路的激活机制可能与最初的激活突变不同,同一个体可能出现多种耐药机制。即使驱动被初始化,第二或共同驱动机制的影响可能会超过初始治疗的机制可能会影响化疗对疾病本身TKI的敏感性。
在 LUX-LONG
在3个试验的临床资料中,3345例非鳞状EGFR突变阳性患者在接受6个周期的铂类治疗后,随机分为阿法替尼组和铂类联合培美曲塞组。化疗对照组ORR可达23%,中位PFS6.9个月。试验中,265例一线吉非替尼治疗后进展的EGFR突变非鳞状患者随机分为6个周期的铂类联合培美曲塞化疗,继续使用吉非替尼或对照组(20).继续服用培美曲塞未纳入研究,单纯化疗组ORR可达34%,中位PFS5.4个月。联合化疗的优势在于LUX-LUNG
3且试验尚未出现,我们考虑试验中的患者是否在突变后对吉非替尼产生耐药,且所有疾病进展的患者均未出现突变。在试验中,对突变阳性患者的亚组分析显示,接受化疗的患者的 ORR 和中位 PFS 分别为 39% 和 5.3 个月,而在突变阴性患者中为 32%。而4. 6 个月。这表明联合化疗对突变的敏感性与否没有显着差异。 4、6周期铂类联合用药对比,或培美曲是否维持治疗,可与AURA对比
3 试验不相关。但试验中详细讨论了培美曲塞在维持非鳞状患者治疗中的作用,结果显示ORR的变化不超过15%,中位PFS的变化不超过1个月.
经过研究人员的努力,部分患者及其家属的期望和要求得到了AURA
3 试验通过,数据结果更新。然而,表1和表2中的结果数据并非全部都可用,但不难推断出AURA 3试验中的大部分结果是可信的。
为什么这项研究很重要?
随着越来越多的分子亚型分析时代的到来,我们需要拓宽思路,以便更深入地研究靶向治疗和化疗相关机制,思维的停滞不利于发现新的溶液,进而影响患者的治疗效果。对于一些新的治疗方法和有效的预测指标,可以衡量一些具体的治疗方案,而这种对化疗效果的跳过随机研究是不值得提倡的。喜欢AURA
像3个试验一样,有意义的临床前试验结果将有助于化疗药物耐药性研究,明确各亚型的相关癌基因。或许是时候考虑何时完成靶向治疗试验(需要化疗组作为对照)。
英德康探索国际新药研发,为国内患者提供全球上市药物的咨询服务,如丙肝新药印度吉III、肝癌新药印度多吉美、PD-1、PD-L 1、肺癌等,帮助国内患者选择更新更有效的治疗药物和方法,更多药品信息和购药渠道,敬请咨询:、、微信:
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话