欢迎光临吉康旅!
1月15日,恒瑞医药发布公告称,其子公司苏州盛迪亚生物制药近日已获得国家食品药品监督管理局颁发的贝伐珠单抗注射液和SHR-1701注射液药物临床试验批件。通知》,近期将启动临床试验。
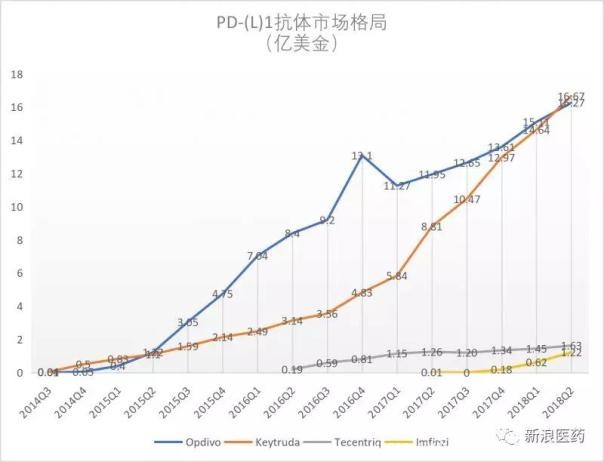
1、药物的基本情况
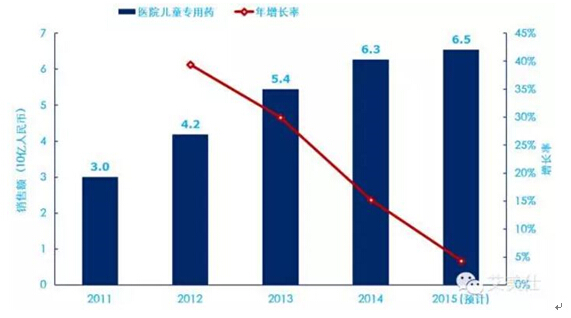
2、药物的其他条件
贝伐珠单抗是一种人源化抗VEGF单克隆抗体,由罗氏子公司基因泰克和中外制药共同开发。2004年美国食品药品监督管理局首次批准上市(),适应症为转移性结直肠癌,随后批准用于治疗非小细胞肺癌、恶性胶质瘤、转移性肾细胞癌、转移性宫颈癌癌症、腹膜癌、肝细胞癌等应用 该病目前在中国和世界许多国家上市。除阿瓦斯汀外,目前还有两种贝伐单抗注射液获准在中国上市。它们是2019年12月获批的安踏(齐鲁药业)和2020年6月获批的大友通(齐鲁药业)。信达生物)。同时,国内多家企业的同类产品已向国家药品监督管理局提交上市申请。目前状态为“审批中”,包括苏州盛迪亚、绿叶药业、贝达药业、生物科技、东方药业、复宏翰林等。查询数据库后,2019年贝伐珠单抗全球销售额约为7美元2.63亿美元,其中原研销售额约7美元1.18亿美元。截至目前,该产品已累计投入研发费用 生物科技、东方耀药业、复宏翰林等查询数据库后,2019年贝伐珠单抗全球销售额约7美元2.63亿美元,其中原研销售额约7美元1. 18 亿美元。截至目前,该产品已累计投入研发费用 生物科技、东方耀药业、复宏翰林等查询数据库后,2019年贝伐珠单抗全球销售额约7美元2.63亿美元,其中原研销售额约7美元1. 18 亿美元。截至目前,该产品已累计投入研发费用
约万元。SHR-1701能促进效应T细胞的活化,同时能有效改善肿瘤微环境中的免疫调节,最终有效促进免疫系统杀伤肿瘤细胞。经查询,KGaA的同类产品目前在国内外正在进行临床试验,适应症主要是晚期恶性肿瘤。国内外尚无同类标的产品获批上市,也无相关销售数据。截至目前,该产品累计研发费用约为人民币12,634万元。根据我国药品注册相关法律法规的要求,药品在取得药品临床试验批件后,
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话
坦西莫司作用的靶点mTOR蛋白是极其重要的一类蛋白,是哺乳动物代谢调节的中枢,参与多种细胞与组织的生理活动,在细胞生长、分化、转移...
FDA批准伊布替尼用于治疗患有以下疾病的成人患者: 1. 既往至少接受过一种治疗的套细胞淋巴瘤(MCL) 2. 慢性淋巴细胞性白血病(C...
根据世界卫生组织国际癌症研究机构(IARC)近期发布的2020年全球最新癌症负担数据报告,乳腺癌首次超越了肺癌,成为了世界上新发患者数...
米哚妥林 (midostaurin,米哚妥林)在2017年被批准用于急性髓性白血病(Acute myeloid leukemia, AML)的治疗后,米哚妥林就被认为开创...
劳拉替尼是一种激酶抑制剂(TKI),对ALK染色体重组的潜伏期肺癌病例呈现高度的活性。劳拉替尼是专为抑制对其它ALK抑制剂产生抗药性的肿...








