欢迎光临吉康旅!
随着靶向治疗的不断发展,EGFR突变的肺癌患者选择EGFR-TKI作为一线治疗已成为不争的事实。然而,耐药性问题是靶向吸毒者难以逾越的鸿沟。盲目地寄希望于第四代药物显然是不现实的。探索其他方式使现有药物的价值最大化也是当前的主流研究方向。
药物联用或许可以达到1+1>2的目的,两种药物的相互作用可以激发彼此的潜能,使其发挥更好的治疗效果。贝伐单抗(,简称A)联合厄洛替尼(,简称T)的“A+T”方案就是其中一种联合方案。
A+T方案最早由日本学者提出,一项前瞻性随机对照II期临床研究(研究)证实,与单独使用厄洛替尼相比,该方案可提高患者的PFS,延长耐药时间。+T方案正式进入历史舞台。
为进一步确认A+T项目的可行性,吴一龙教授和周庆教授团队在我国开展了国家多中心、随机对照、开放标签III期研究。临床研究,旨在比较晚期EGFR突变阳性的中国一线贝伐单抗(A)联合厄洛替尼(T)和厄洛替尼(T)单药治疗的疗效和安全性。
经过6年的潜心研究,我们获得了可喜的结果,A+T方案可以降低45%的恶化风险,降低52%的脑部进展,对21外显子点突变患者同样有效。因此,-的研究成果于当地时间2021年8月12日正式发表在《Cell 》期刊( 31.74分),成为该期刊发表的第一期第三期文章与临床研究有关。
A+T方案有哪些优势?
疗效优于单一药物
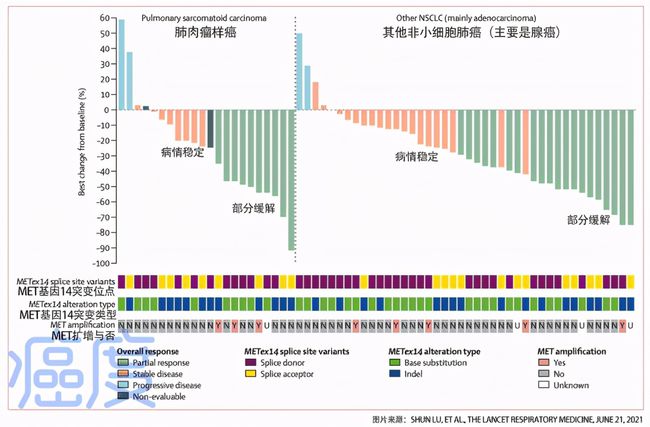
311名受试者中,A+T组共154人,厄洛替尼单药治疗组157人,分别接受厄洛替尼qd+贝伐单抗15 mg/kg q3w或qd厄洛替尼治疗。结果显示,A+T组的无进展生存期(PFS)为17.9个月(95%置信区间[CI],15.2-19. 9),11.2 个月的无进展生存期 (PFS)(95% CI,9.7-13.8)@ 在厄洛替尼单药治疗组) >(风险比 [HR] = 0.55;95% CI,0.41–0.73;p
可控的安全性
A+T联合方案的毒性可控、可耐受,未发现新的安全性信号。86 名 (54.8%) 和 40 名 (26.1%) 患者分别发生了 3 级或更高级别的治疗相关不良事件。生物标志物探索性分析显示,A+T 组和厄洛替尼单药组患者具有相似的基线突变谱,包括 EGFR、癌基因融合、扩增、MAPK/PI3K 通路和进展时的细胞周期进展,但获得性耐药谱略有不同两组间比较,联合治疗组EGFR突变发生率略低于单药组,由于样本量有限,未达到统计学意义。在 A+T 组中,52% 的患者具有未知的耐药机制,相比之下,单剂组为 36%。EGFR突变的动态在两组中显示出相似的模式。
治疗脑转奇迹
贝伐单抗加厄洛替尼治疗的脑转移亚组也显示出 PFS 改善(HR = 0.48;95% CI,0.27–0.84;p = 0.00< @8),也就是说联合用药可以将脑转移的风险降低52%,相比单药厄洛替尼是一个相当大的进步。
19、21 个突变有效
在以往的研究中,大多数药物对19个突变比21个突变更有效,而贝伐单抗加厄洛替尼不仅延续了厄洛替尼单独对19外显子缺失突变的治疗效果,还完成了对21外显子点突变疗效的超越,PFS 达到了惊人的 19.5 个月。可以说,对于有突变的患者来说,它是一种非常值得治疗的方法。
外显子19缺失突变患者的PFS曲线
外显子21点突变患者的PFS曲线
一线治疗新模式
贝伐单抗加厄洛替尼的 A+T 方案显着改善了未经治疗的转移性 EGFR 突变患者的 PFS,特别是对于基线中枢神经系统 (CNS) 转移或具有外显子 21 点突变的患者。
值得一提的是,在 EGFR-TKI 治疗期间,无论是否使用贝伐单抗,EGFR 突变的分子动力学都没有改变。这意味着A+T的耐药模式与厄洛替尼单药几乎相同,超过50%的患者耐药后可使用第三代药物作为后续治疗。
治疗效果更好,治疗范围更全面,不影响后续治疗。A+T方案无疑比单独使用厄洛替尼具有综合优势,因此我们非常有必要将其作为一线治疗。考虑。
目前——研究成果已写入中国临床肿瘤学会(CSCO)《原发性肺癌诊疗指南》(2020年版),A+T方案也成为首批——晚期 EGFR 突变患者的线选择,特别是对于有中枢神经系统 (CNS) 转移或外显子 21 点突变的基线患者。
相信在未来,A+T治疗方式将为更多患者带来新的治疗益处。同时,伴随着A+T的良好开端,VEGF和EGFR的双重抑制组合可能会有更多新的合作伙伴给我们带来惊喜!
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话