欢迎光临吉康旅!
肝癌免疫治疗,2020年肝癌PD-1/PD-L1免疫治疗成果
2020年12月23日,国家癌症中心主任、中国科学院院士何杰指出,近十年来,我国癌症患者5年生存率提高了10个百分点左右,从 30.9% 到 4. 0.5%。尽管与医疗水平较发达的国家仍有一定差距,但越来越多的患者成功挺过了“带瘤”甚至“无癌”的五年。
但在各类癌症中,总有5年生存率较高的癌症,如乳腺癌;还有一些癌症的总体 5 年生存率较低,患者生存率令人担忧,例如肝癌。肝癌主要是指肝细胞癌,是我国发病率非常高的癌症。我国每年新增肝癌患者人数占全球新增患者总数的50%以上,死亡人数也占50%以上。
目前,我国肝癌患者整体5年生存率仅为12%左右。最重要的原因之一是80%以上的患者在确诊时已经发展到中晚期,不能再接受根治性手术。对于这些患者来说,药物治疗已成为延长生存期的最重要手段之一。
2020:肝癌免疫治疗的“黄金时代”
2020年,晚期肝癌免疫治疗迎来多项突破。其中,阿特珠单抗与贝伐单抗的联用堪称肝癌一线治疗“十余年一遇”的重大突破。
二线治疗方面,纳武利尤单抗和易普利姆玛双联免疫联合用药获批,为接受索拉非尼治疗的患者送上了一份“大礼”。
此外,卡瑞利珠单抗在我国获批,多项免疫联合方案取得重大进展,一种肝癌新药获得孤儿药称号,开启肝癌治疗新篇章。
随着2021年的临近,基因医学中心总结了2020年肝癌免疫治疗的重大突破,希望患者能带着更多希望进入新的一年。
肝癌的双重免疫疗法
纵观2020年全年免疫治疗发展,我们可以发现,双免疫联合治疗方案正逐渐成为免疫治疗的重要研究方向。今年越来越多的团体发表了新的研究成果,令人眼花缭乱。各种免疫检查点抑制剂都在用数据证实双免疫联合疗法正在成为免疫疗法发展的必由之路。
在肝癌的适应症上,两组免疫联合均取得了较好的效果。
01、O+Y:33% 的总体响应率,31% 的响应超过 24 个月
2020 年 3 月 11 日,FDA 批准了纳武单抗 (,) 和易普利姆玛 (,) 的联合方案 (“O+Y”),用于治疗已接受索拉非尼 (,) 治疗的肝细胞癌患者。
根据I/II-040期研究结果,接受O+Y治疗的患者总体缓解率为33%,其中完全缓解率为8%,部分缓解率为24%;根据修改后的v1.1标准,总体缓解率为35%,其中完全缓解率为12%,部分缓解率为22%。
患者对治疗的反应持续时间从 4.6 个月到 30.5 个月或更长时间不等,88% 的患者反应超过 6 个月,56% 的患者超过 12 个月,31%的患者超过 24 个月。
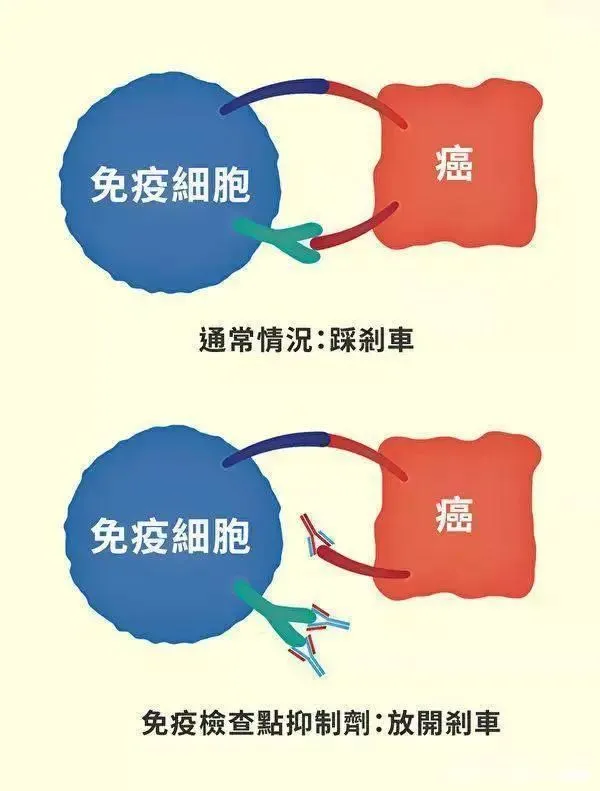
“O+Y”可以说是免疫治疗方案中的一对“黄金搭档”,已在10多个适应症的治疗中显示出良好的潜力或获批。以“O+Y”为代表的双免疫联合疗法也成为当前免疫疗法研究的重点。
02、I+:总生存期长达 18.7 个月
(,)也尝试了双免疫联合治疗的思路,选择了(原名,CP-675,206)这个新药作为“帮手”。它是CTLA-4抑制剂,由的研发公司阿斯利康开发,最初在治疗黑色素瘤、间皮瘤和非小细胞肺癌等癌症方面进行临床试验,但均未成功。
与 联用是这两种药物的全新尝试。I+组合在肝癌、消化系统肿瘤和肺癌脑转移瘤的治疗中显示出一定的潜力。
根据2020年国际肝癌协会虚拟会议公布的结果,在一项I/II期研究中,+二线治疗晚期肝癌患者在部分剂量下取得了显着疗效。
接受 300 mg 一次和 1500 mg 每月一次 的患者中位总生存期为 18.7 个月,18 个月生存率为 52.0%,总反应率为 24.@ >0%;
在接受 750 mg 每月单药治疗的患者中,中位总生存期为 15.1 个月,18 个月生存率为 45.7%,总缓解率为 7.2%;
对于每月接受 1500 mg 单药治疗的患者,中位总生存期为 13.6 个月,18 个月生存率为 35.3%,总缓解率为 10.6% ;
在接受 4 个月剂量 75 mg 加 1500 mg 的患者中,中位总生存期为 11.3 个月,18 个月生存率为 34.7%,总反应率为 .5%。
免疫联合抗血管生成治疗
免疫检查点抑制剂药物与抗血管生成药物的联合应用也是免疫治疗的一个重要发展方向。机制上,一方面,抗血管生成药物不仅可以逆转血管内皮生长因子(VEGF)引起的免疫抑制作用,还可以使肿瘤血管正常化,促进T细胞和其他免疫效应分子的传递;另一方面,免疫检查点抑制剂可以通过激活效应 T 细胞使肿瘤血管正常化,并增加效应 T 细胞的浸润和杀伤功能。
两类药物作用互补,在肾癌、肝癌、非小细胞肺癌等多种癌症的治疗中均显示出良好的疗效。
01、A+T:改写一线治疗标准,缓解率翻倍
2020年5月30日,FDA批准(,)和贝伐单抗(,)的联合方案(“A+T”)用于不可切除或转移性肝细胞癌患者的一线治疗。多位专家盛赞该方案为肝癌一线治疗十余年来的首次突破。
根据迄今已发表的试验结果,截至 2019 年 8 月 29 日,中位随访时间为 8.6 个月。接受A+T治疗的患者中位无进展生存期为6.8个月,6个月无进展生存率为54.5%;接受索拉非尼治疗的患者中位无进展生存期为4.3个月,6个月无进展生存率为37.2%。
总生存率方面,A+T治疗组6个月生存率为84.8%,12个月生存率为67.2%;索拉非尼治疗的患者分别为 72.2% 和 54.6%。
根据1.1标准的评价结果,A+T治疗患者总体缓解率为27.3%,疾病控制率为73.6%;而接受索拉非尼治疗的患者总体反应率仅为11.90%,疾病控制率为55.3%。
2020年10月31日,“A+T”计划在中国获批;11月3日,该计划在欧洲再次获得批准。如此迅速的审批进度,也从侧面印证了该方案的有效性。
给二线治疗带来新挑战
针对这一方案获批,肝癌专家D. Kim博士指出,虽然这一方案在一线治疗上带来了巨大突破,但也对耐药后的二线治疗提出了挑战。
目前,尚无研究或证据证实其中任何一种方案均可成为“A+T”组合后的二线治疗方案。目前,卡博替尼、瑞戈非尼、乐伐替尼、派姆单抗+雷莫芦单抗、纳武利尤单抗、纳武利尤单抗与易普利姆玛联合用药的现有临床“O”方案“+Y”等方案尚未获批用于“A+”的后线适应症T”,因此是否对“A+T”耐药患者有益尚不清楚。
对其他癌症(如结直肠癌)的研究结果表明,对这些治疗有抗药性的患者可以使用抗血管生成药物进行治疗,但在肝癌中没有类似的数据。
显然,需要更多的研究来制定新的护理标准。相信2021年会有更多相关研究项目启动。
02、 + :现有或突破性指定,但加速批准申请延迟
(,) 和 (,) 的联合疗法于 2019 年 7 月被 FDA 授予突破性疗法指定,用于一线治疗不可切除的肝细胞癌患者。
根据 Ib-524/116 期试验的结果,接受 + 治疗的患者的总体缓解率为 46%,根据修改后的标准,中位缓解持续时间 8.6 个月;根据标准评价,患者总体缓解率为36%,中位缓解持续时间为12.6个月。综合评价这两个标准,患者的疾病控制率为88%。
调查人员已向 FDA 提交加速批准申请,但被 FDA 拒绝。原因在于该组合的疗效并未超过今年5月获批的“A+T”组合的疗效。
尽管如此,派姆单抗+乐伐替尼联合用药的疗效还是很好的,为其他方案的开发提供了一个很好的思路。
04.0@>+阿帕替尼:OS 20.3 个月
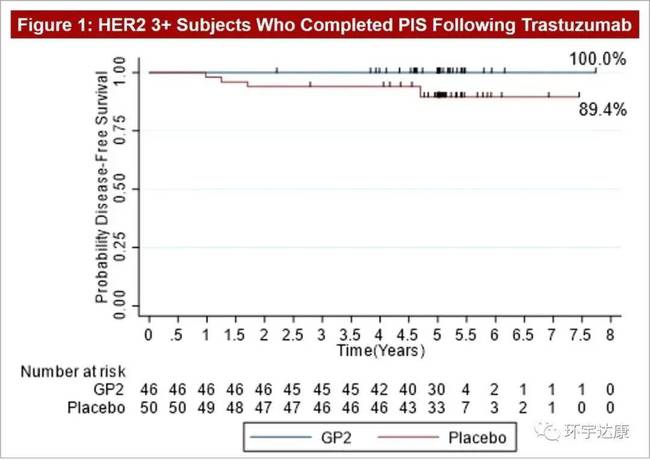
是国产PD-1抑制剂,在全球14个国家拥有50多个临床研究项目。
根据II期试验结果,使用卡瑞利珠单抗+阿帕替尼治疗晚期肝癌,初治患者总体缓解率为34%,中位无进展生存期5.7个月, 中 中位总生存期为 20.3 个月;对一线靶向治疗无效的既往治疗患者的总体反应率为23%,中位无进展生存期为5.5个月。
初治患者9个月生存率为86.7%,12个月生存率为74.7%,18个月生存率为58.3 %; 79.1%、68.2% 和 56.4%。
2020年3月,卡瑞利珠单抗在中国获批肝癌适应症,标志着中国肝癌治疗正式进入免疫时代。
就在几天前,2020 年的医疗保险谈判刚刚结束。一向以低价策略竞争的卡瑞利珠单抗有可能下跌80%,同时选择所有四个适应症(涉及肺癌、食道癌、肝癌和霍奇金淋巴瘤)。我们相信,中国的癌症免疫治疗正朝着“可用药”和“用得起的药”的未来大踏步前进。
04、 + 贝伐单抗:死亡风险降低 43.1%
继与安罗替尼联手取得42.9%的缓解率后,信迪利单抗与贝伐单抗再次联手挑战肝癌适应症。根据2020年ESMO亚洲大会披露的-32试验数据,在晚期肝癌一线治疗中使用辛迪单抗+贝伐单抗与使用索拉非尼相比,死亡风险降低了43%。
接受 + 的患者1年生存率为62.4%;接受索拉非尼治疗的患者 1 年生存率为 48.5%。
早期研究数据:纳武单抗在新辅助治疗中的初步疗效
肿瘤直径
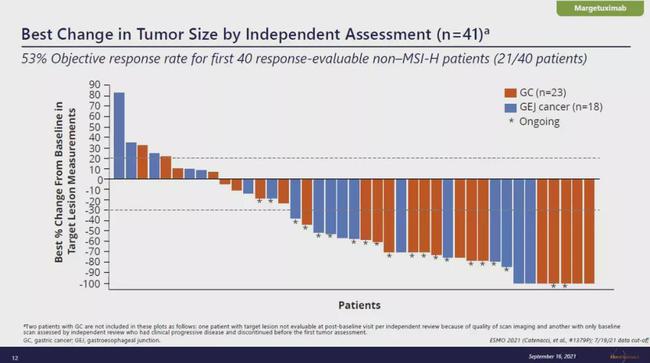
在试验中,研究人员使用了纳武利尤单抗作为新辅助治疗方案,结果显示,29%的患者肿瘤体积缩小,为后续治疗创造了条件。
免疫疗法临床试验火爆,免费招募机会不容错过
为了帮助您更好地熟悉抗癌药物和治疗癌症,基因药物整理了正在免费招募患者的免疫治疗新药临床试验项目,为您提供新药试验申请途径。药物种类很多,可以先咨询,然后在医学顾问的指导下选择适合自己的新药。
符合条件的患者可将基因检测报告、诊断报告的电子版或清晰照片发送至新药招募中心邮箱()进行申请,并在邮件中留下联系方式;或联系全球肿瘤学家网络医疗部()进行详细咨询。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话