欢迎光临吉康旅!
02 获批的创新抗肿瘤药物能否撑起大旗?
作为医药领域最大的细分市场,抗肿瘤药赛道一直是创新药企业的“角力”。恒瑞一半的收入来自抗肿瘤产品。
2020年,恒瑞抗肿瘤产品实现销售收入152.68亿元,占总收入的55.05%,同时贡献58.45%的利润,远高于麻醉和造影剂业务。
经过多年的研发,恒瑞拥有多个重磅创新抗肿瘤药物,包括卡瑞利珠单抗、阿帕替尼、硫培非格司亭、吡咯替尼、氟唑帕尼、达西利等。
1、卡瑞利珠单抗
作为恒瑞的核心抗肿瘤产品,卡瑞利珠单抗已获批用于经典霍奇金淋巴瘤、二线肝癌、一线非鳞状非小细胞肺癌、二线食管鳞癌、三线鼻咽癌癌、一线鼻咽癌有6个适应症,其中前4个适应症已纳入医保。
从适应症布局来看,有望在2022-2024年获批多个适应症。其中,食管癌一线治疗和肺鳞癌一线治疗有望于2022年获批,卡瑞利珠单抗联合阿帕替尼一线治疗进入III期临床治疗肝癌有望于2022年申请FDA BLA。
不过,恒瑞现在面临的问题是如何在已经是竞争红海的PD-1市场保持稳定增长。
截至目前,已有8个PD-1 mAb获批上市(2个进口,6个国产)。如果乐普生物和复宏汉霖的PD-1在2022年也顺利获批,10款竞品将展开激烈竞争。
截至2022年1月6日,全球PD-1靶向药物临床试验总数已达3471个,中国有675个,约占全球的19.5%。
毫无疑问,未来卡瑞利珠单抗的销售压力将继续加大。虽然85%的价格包含在医保中,但量价交换的效果还没有完全发挥出来。入院难、各地医保实施时间不同等问题依然存在,导致卡瑞利珠单抗销售收入环比出现负增长。
显然,面对“前面打虎挡路,后面有饿狼”,如果过分依赖卡瑞利珠单抗,恒瑞突破“至暗时刻”的概率将非常小。
2、阿帕替尼
阿帕替尼是治疗晚期胃癌的药物,是恒瑞继非甾体抗炎药埃瑞昔布之后第二个获批的1.1类创新药,也是恒瑞首个获批的抗肿瘤靶向药物。
事实上,阿帕替尼于2005年获得Labs授权给恒瑞医药,2014年获批上市,用于晚期胃癌或胃食管结合部腺癌的三线及以上治疗;晚期肝癌二线及以上治疗的两种适应症。
从市场结构来看,除阿帕替尼外,目前获批治疗胃癌的药物还有曲妥珠单抗、纳武单抗、派姆单抗、雷莫芦单抗、维迪。西妥珠单抗。
其中礼来的雷莫芦单抗和阿帕替尼均为-2抑制剂,除获批用于胃癌/胃食管结合部癌的二线治疗外,还获FDA批准用于肺癌、肝癌、胃癌癌症和胃癌。直肠癌和许多其他适应症。目前,雷莫芦单抗已在中国申请上市,预计2022年第一季度获批。
相比之下,阿帕替尼的优势在于具有一定的广谱性,对多种癌症类型有效(已开展24项临床试验),还可与PD-1单克隆抗体联合用于主要核心适应症. 临床试验具有巨大的市场潜力。
在纳入医保之前,2015年和2016年阿帕替尼的销售额分别约为3亿元和10亿元。2017年,纳入医保后,保额快速增长。当年终端销售额达到13亿元,2020年将大幅提升至23.9亿元。
3、替培非格司亭
1991年2月,安进公司研制的世界上第一个重组人粒细胞集落刺激因子(rhG-CSF,俗称“美白剂”)非格司亭(第一代rhG-CSF)于2002年获得FDA批准上市。长效剂型培非格司亭也上市,几乎垄断了全球长效G-CSF的销售。
所谓美白剂主要用于肿瘤患者化疗后中性粒细胞过度减少的治疗,包括短效和长效。
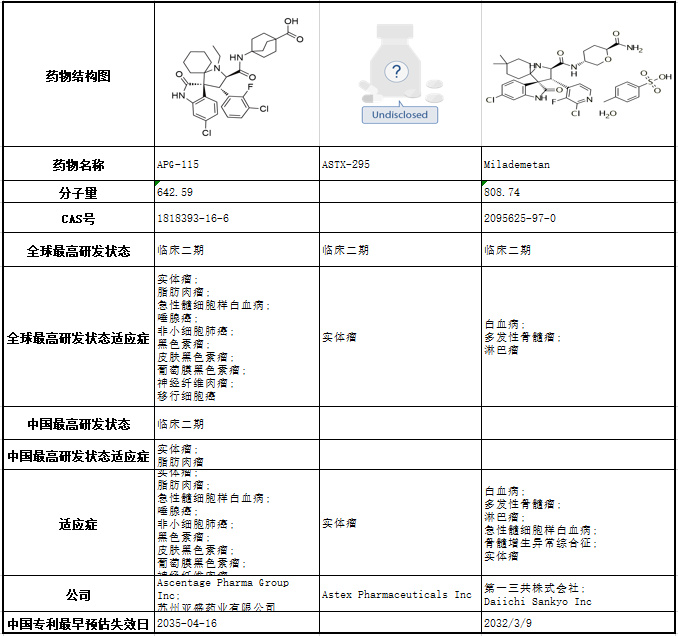
恒瑞医药参照培非格司亭优化G-CSF结构,成功获得具有专利优势的聚乙二醇重组人粒细胞刺激因子-HHPG-19K。
恒瑞的硫培非格司亭注射液(商品名:Aido)于2018年5月上市,适用于非髓系癌患者。目前,全球 G-CSF 市场以疗效更好的长效制剂为主。中化百克(2011年上市)金优利(2011年上市)和齐鲁药业新瑞白(2015年上市)两款长效G-CSF产品在爱多之前获批,占据先发优势。
被纳入2019年医保目录后,爱多的体量大幅增加。2020年销售额达到4.96亿元,2021年上半年达到4.12亿元,但仍低于齐鲁和十药白。克同类产品出售。PDB数据显示,2021年上半年,国内长效G-CSF产品样本医院市场格局呈三足鼎立趋势,齐鲁、石药百科、恒瑞分别占据40%、34%、26%的市场份额。分别占市场份额。
此外,恒瑞还要面对G-CSF赛道上众多竞品的竞争。
在短效G-CSF方面,杭州九元、双鹿药业等18家国内企业已获批。
长效G-CSF方面,山东新时代药业于2021年5月成功获得“第四届国内长效白药”配额;已提交上市申请的双鹿药业有望抢占第5个国产药;有很多公司处于临床后期。此外,在创新长效制剂方面,一帆药业旗下建能龙F-627的上市申请已于2021年5月获得FDA受理,预计将对现有市场产生影响。
未来,随着越来越多的竞品陆续获批,无疑会给恒瑞带来更大的挑战。
4、吡咯替尼
恒瑞的马来酸匹罗替尼片于2018年8月获批,是中国首个双靶点EGFR(HER-1)和HER-2抑制剂),一种小分子、不可逆的泛ErbB受体酪氨酸激酶抑制剂(TKI)。该产品与卡培他滨联合用于未接受或之前接受过曲妥珠单抗治疗的 HER2 阳性晚期或转移性乳腺癌患者。在使用本产品之前,患者应接受过蒽环类或紫杉类化疗。
此外,吡罗替尼联合曲妥珠单抗和多西他赛用于HER2乳腺癌的新辅助治疗已于2021年9月提交国内NDA,预计2022年获批上市。
目前,国内外已上市用于治疗乳腺癌的EGFR/HER2小分子抑制剂包括拉帕替尼(2013年中国获批)、来那替尼(2020年中国获批)和图卡替尼(也获中国获批)未上市在国内)。
相比之下,吡咯替尼在乳腺癌适应症中的临床结果超过了拉帕替尼。根据头对头实验,吡咯替尼的临床结果与拉帕替尼相比,客观缓解率提高约21%,中位无进展生存期(PFS)提高11.1个月,超过 159% 的帕替尼组患者的疾病进展或死亡风险降低了 63.7%。
此外,吡咯替尼的选择性优于来那替尼,临床疗效和安全性优势显着。从分子结构上看,与相似,但的靶向选择性略优于,ORR和SAE结果也优于。
由于吡咯替尼具有一定的产品优势和本地渠道优势,且在2019年纳入医保后,销售增速较快。根据PDB药品综合数据库,样本医院2018-2020年和2021年上半年吡咯替尼销售额分别为171.28万元、2148万元、2.28亿元、1.57 亿。
5、氟唑帕尼胶囊
2020年12月获批的PARP抑制剂氟唑帕尼已获批两个适应症:用于既往接受过二线及以上化疗或原发性腹膜癌的铂敏感复发性卵巢癌和生殖系BRCA突变的输卵管癌;在对铂类化疗完全或部分反应后,对铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成年患者进行维持治疗。
不过,目前全球还有其他五种PARP抑制剂获批上市,分别是奥拉帕尼(阿斯利康)、尼拉帕尼(再鼎医药)、帕米帕尼(百济神州)以及塔拉佐帕尼和鲁卡帕尼,其中前三种已在中国上市。此外,国内部署PARP抑制剂的企业也不在少数。
6、 羟乙基磺酸盐片
2021年12月获批的羟乙基磺酸盐片是首个中国来源的CDK4/6抑制剂。该适应症与氟维司群联合用于内分泌治疗后激素受体(HR)阳性、HER2阴性患者。晚期复发或转移性乳腺癌的治疗。
在 获批之前,全球已经批准了四种 CDK4/6 抑制剂,包括辉瑞的 (2015 年)、诺华的 (2017 年)和礼来的 (2017 年)。) 和 G1/先声药的 (2021)。其中,和均获准在中国上市。
此外,至少有10家国内公司正在开发CDK4/6抑制剂。其中,嘉禾生物的(口服)和玄珠药业的吡罗西尼(口服)已经处于III期临床试验阶段。

更值得一提的是,2020年12月获批的齐鲁药业仿制药正在率先颠覆CDK4/6抑制剂市场。目前,国内已有十余家企业布局仿制药。可见,未来一旦大量仿制药获批上市,无疑将对CDK4/6抑制剂创新药和赛道带来不小的冲击。
03 获批的非抗肿瘤创新药的市场价值是多少?
除了抗肿瘤领域,恒瑞医药还全面布局自身免疫性疾病、疼痛管理、代谢疾病、感染性疾病等非肿瘤领域。
然而,非肿瘤市场的竞争不亚于创新药战场。
比如恒瑞首个获批用于缓解骨关节炎疼痛症状的COX-2抑制剂埃瑞昔布,就不得不面对辉瑞研发的两大原研药帕瑞昔布和塞来昔布。25家药企注射用帕瑞昔布钠获批。
数据显示,2020年注射用帕瑞昔布钠终端销售总额为21.96亿元,市场份额排名前五为:辉瑞、湖南科伦药业、齐鲁正大天晴药业、江苏奥赛康药业。
在血液领域。恒瑞的 乙醇胺片于 2021 年 6 月获批,适用于慢性原发性血小板减少症(ITP)和严重再生障碍性贫血(TPP)。、()、艾曲波帕乙醇胺(葛兰素史克/诺华)和重组血小板生成素(沉阳阳光药业),抢占先发优势。其中,2020年艾曲波帕乙醇胺片全球销售额约17.38亿美元,国内样本医院销售额7029万元。
2022年1月11日,海曲波帕III期临床试验获美国FDA批准。恒瑞计划在美国、欧洲和澳大利亚开展治疗恶性肿瘤化疗引起的血小板减少症的临床研究。
脯氨酸恒格列净片于2021年12月获批,是国内首个获批用于改善成人2型糖尿病血糖控制的创新SGLT-2抑制剂。这也是恒瑞经过10年研发终于在糖尿病领域获批的首个创新药,具有里程碑意义。
但从目前的市场情况来看,恒力晶要改变国内降糖药市场仍以传统降糖药为主的格局似乎并不容易。
根据医药魔方数据库,全球共有8款SGLT-2抑制剂获批上市,强生、阿斯利康、默克等公司的竞品已在中国上市。
与此同时,很多公司都盯上了SGLT-2抑制剂1类新药。如四环医药旗下玄珠生物研发的加格列净、阳光药业研发的容格列净、赛诺菲的进口药索格列净等均处于III期临床试验阶段。
此外,与达西力一样,扰乱市场的SGLT-2抑制剂仿制药也与创新药并存。数据库显示,除2020年7月新上市的艾格列净外,恩格列净、卡格列净和达格列净分别有5、3、2个国产仿制药。批。可见,SGLT-2抑制剂市场竞争激烈。
(国内上市的SGLT-2抑制剂来源:数据库)
04 即将获批的创新药能否扭转局面?
如前所述,虽然恒瑞医药目前拥有10个创新药,但这些创新药产品,像卡瑞利珠单抗一样,也面临着众多同类竞品的压力。
展望未来,恒瑞若想突破“至暗时刻”,无疑将加快在研创新药的研发。截至目前,恒瑞有50多个创新药在临床研发,240多个国内外临床试验正在进行中。
从研发进度来看,恒瑞目前至少有3个新药在市场应用,如DPP4抑制剂瑞格列汀、第二代AR拮抗剂,还有10多个新药处于临床III期。
(恒瑞临床3期新药来源:数据库)
1、
是恒瑞斥资1亿多美元向公司引进的新型口服唑类抗真菌药物。上市申请于2022年1月5日被国家药监局受理,适应症为急性外阴阴道念珠菌病。
公司于2021年7月向美国FDA提交了NDA,并于2022年1月27日被纳入优先审评审批日期,审批在即。
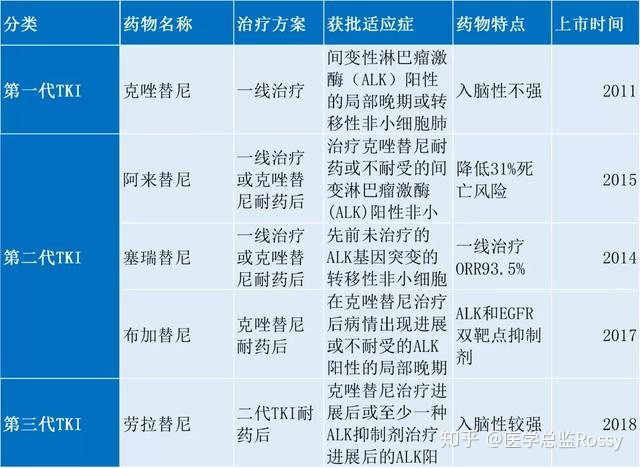
但目前,国内外已获批氟康唑(辉瑞)、伊曲康唑(公司)、伏立康唑(辉瑞)和艾沙康唑(公司)等同类产品上市,且均已在国内获批。列出。
2、
是恒瑞研发的第二代AR拮抗剂。与第一代AR拮抗剂相比,AR抑制作用更强,无激动作用。2021年8月,该片剂被国家食品药品监督管理总局列入《建议突破性治疗品种公开目录》,适应症为高肿瘤负荷的转移性激素敏感性前列腺癌。
但也有许多竞争产品。比卡鲁胺(第一代)、恩杂鲁胺(第二代)、(新一代)6款AR拮抗剂已在全球上市,其中比卡鲁胺(阿斯利康)、恩杂鲁胺(安斯泰来/辉瑞)、阿帕鲁胺(西安杨森)、达洛他胺(拜耳)已全部获准在中国上市。
3、雷格列汀
瑞格列汀是恒瑞研发的用于治疗2型糖尿病的DPP4抑制剂,其结构与默克公司的西格列汀相似。
然而,DPP-4抑制剂的市场竞争更加激烈。据西南证券研报显示,目前全球已有12个DPP-4抑制剂获批上市,其中西格列汀、维格列汀、沙格列汀、利格列汀、阿格列汀及相关化合物制剂已在中国获批。
同时仿制江苏奥赛康获批的沙格列汀片、江苏汉森维格列汀片、齐鲁药业维格列汀片、雅宝药业阿格列汀片等国产DPP-4抑制剂。制药公司也进来扰乱游戏。
此外,在恒瑞的Ⅲ期临床新药中,阿德贝利木单抗(SHR-1316)、SHR-1701、苹果酸法米替尼)等抗肿瘤药物备受关注。
是恒瑞研发的PD-L1单克隆抗体。目前,贝利木单抗联合化疗一线治疗广泛期小细胞肺癌的III期研究已经成功,将提交上市申请,预计2022年或2023年获批。
目前,我国共有4个PD-L1单克隆抗体获批上市(国产2个,进口2个),科伦李氏制药厂的PD-L1预计2022年获批上市。 PD-L1 mAb 市场的竞争不亚于 PD-1 mAb。
SHR-1701是恒瑞研发的靶向PD-L1/TGFβ的双特异性抗体。.
目前,SHR-1701的两个适应症已进入III期临床阶段,分别是联合化疗一线治疗胃癌、联合(贝伐单抗生物类似药)和化疗一线治疗晚期结直肠癌。
然而,万众瞩目的临床试验却一次次遭到滑铁卢的重创,试验不得不再次终止。
法米替尼是恒瑞自主研发的小分子多靶点酪氨酸激酶抑制剂,对多种受体酪氨酸激酶具有良好的抑制活性。恒瑞已申请并开展了多项PD-1单克隆抗体联合法米替尼的临床试验,涉及多个大癌症类型。
此前,卡瑞利珠单抗+苹果酸法米替尼联合疗法被国家食品药品监督管理局纳入突破性疗法,用于治疗一线治疗失败、目前处于临床III期的复发转移性宫颈癌。阶段。
以多靶点抑制剂为例。目前,在中国获批上市的多靶点抑制剂包括索拉非尼(拜耳)、舒尼替尼(辉瑞)、帕唑帕尼(诺华)等。
结论:随着集中采购常态化和仿制药销量下滑,市场对恒瑞医药提出了更高的要求。
尽管恒瑞拥有10款创新药,创新药销售额占总收入的比重已提升至40%,但从2021年“高开低走”的股价表现来看,显然未能达到市场预期。
同时,在恒瑞实施的从我也是到仿我的创新药转型战略下,纵观现有和未来在研管线,存在错失先发优势的问题。
基于此,恒瑞除了依托强大的研发团队和商业化团队,还实现了“后发力”。布局。
或许,这也是恒瑞医药能够找到的突破“至暗时刻”,重回巅峰的最佳“药方”。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话