欢迎光临吉康旅!
2021年6月28日,美国旧金山和中国苏州——信达生物制药(港交所代码:),一家致力于治疗肿瘤、代谢疾病、自身免疫等重大疾病药物研发、生产和销售的生物制药公司创新药生物制药公司宣布,国家药品监督管理局(NMPA)正式批准创新PD-1抑制剂®(信迪利单抗注射液)联合®(贝伐单抗注射液)用于无法切除的一线治疗或之前未接受过全身治疗的转移性肝细胞癌。这是全球首个获批用于肝癌患者一线治疗的PD-1免疫联合疗法。
这是大博舒®(信迪利单抗注射液)第四个获批适应症,大禹通®(贝伐单抗注射液)第四个获批适应症。2018年12月,达博舒®(辛迪利单抗注射液)获NMPA批准用于治疗复发或难治性经典霍奇金淋巴瘤,2021年2月获NMPA批准与培美曲塞、铂类联合用于一线治疗2021年6月获国家药监局批准联合吉西他滨和铂类化疗一线治疗晚期鳞癌。此前,大禹通®(贝伐单抗注射液)已获国家药监局批准用于晚期非小细胞肺癌、转移性结直肠癌和成人复发性胶质母细胞瘤三个适应症。
该适应症的批准是基于一项随机、开放标签、III期对照临床研究(-32)-®( 注射液)联合 ®(贝伐单抗) 注射液),用于首次-不可切除或转移性肝细胞癌的一线治疗。根据独立数据委员会(iDMC)对中期分析结果的审查,®(辛迪单抗注射液)联合®(贝伐单抗注射液)与索拉非尼单药治疗相比,显着延长了总生存期(OS)和无进展生存期( PFS),达到预设的优越性标准。联合治疗是安全的 性数据与之前的报告一致,没有新的安全信号。-32 研究结果的全文于 2021 年 6 月 15 日发表在《柳叶刀肿瘤学》(The ) 上。
复旦大学附属中山医院范嘉院士说:“肝癌是我国第四大常见恶性肿瘤,死亡率居第二位,五年生存率只有10%左右,肝癌不敏感免疫疗法的出现改写了肝癌的治疗谱,以免疫疗法为基础的联合疗法取得了历史性的突破。-32研究表明,一线治疗信迪利单抗联合贝伐单抗 延长晚期肝癌患者的无进展生存期和总生存期,给患者带来巨大的临床效益。这将为我国乃至全世界的肝癌患者提供新的治疗选择,也为我国“健康中国2030”目标的实现做出了贡献
信达生物制药集团总裁刘永军博士表示:“就死亡率而言,肝癌是全球第三大恶性肿瘤。中国约占全球肝癌患者的一半,其中85-90%是肝细胞癌,严重威胁着中国人民的生命健康,给社会和家庭带来了严重的疾病负担,我们很高兴看到两个国家重大新药创制项目——大博舒®(信替利单抗注射液)而大禹通®(贝伐单抗)这也是全球首个获批用于肝癌患者一线治疗的PD-1免疫联合疗法,信达生物将继续秉持研发高品质、物美价廉的生物药的初衷普通人.,为更多患者带来生命希望,为全面实施“健康中国2030”癌症防治规划继续贡献力量。”
关于肝癌
肝癌是世界上常见的消化系统恶性肿瘤。中国肝癌患者人数约占世界的一半。肝癌严重威胁着我国人民的生命和健康。肝癌的主要病理类型为肝细胞癌(HCC),占85%~90%;少数为肝内胆管癌(ICC)和HCC-ICC混合型。在我国,HCC主要由乙型肝炎病毒(B,HBV)和/或丙型肝炎病毒(C,HCV)感染引起。
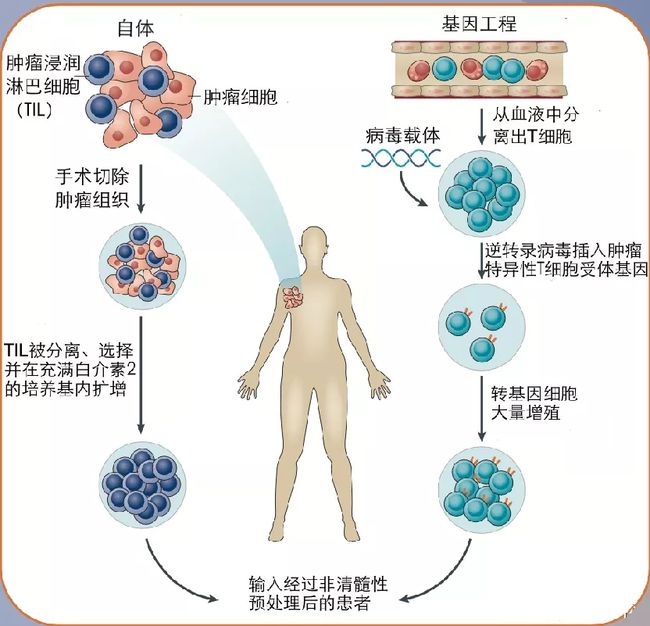
关于-32研究
-32研究是比较达博舒®(信迪利单抗注射液)联合大禹通®(贝伐单抗注射液)和索拉非尼一线治疗晚期肝癌的疗效和安全性随机、对照、开放标签、多中心期III 临床研究(NCT)。该研究共招募了 571 名受试者,主要终点是独立影像审查委员会 (IRRC) 根据 v1.1 评估的总生存期 (OS) 和无进展生存期 (PFS)标准。
根据独立数据监测委员会 (IDMC) 进行的中期分析,®(辛迪单抗注射液)联合 ®(贝伐单抗注射液)比索拉非尼单药治疗更有效。总生存期(OS)和无进展生存期(PFS)延长。联合治疗方案的安全性数据与以往报道一致,未出现新的安全性信号。-32 研究结果的全文于 2021 年 6 月 15 日发表在《柳叶刀肿瘤学》上。
关于信迪利单抗
信迪利单抗,中文品牌名称为大博舒®(信迪利单抗注射液),是信达生物制药与礼来公司联合开发的具有国际品质的创新PD-1抑制剂药物。是一种人免疫球蛋白G4(IgG4)单克隆抗体,可特异性结合T细胞表面的PD-1分子,从而阻断PD-1/程序性死亡受体配体1(-1,PD-L< @1)通路,重新激活淋巴细胞的抗肿瘤活性,从而达到治疗肿瘤的目的。目前已有二十多项临床研究(其中10多项正在进行注册临床试验,以评估抗肿瘤效果)信达利单抗对各种实体瘤和血液肿瘤的疗效,信达生物也在全球范围内开展信迪利单抗注射液的临床研究。
信迪利单抗已在中国获批用于四种适应症,包括:
用于治疗至少接受过二线全身化疗的复发性或难治性经典霍奇金淋巴瘤
培美曲塞联合铂类化疗一线治疗EGFR或ALK阴性晚期非鳞状细胞癌
吉西他滨联合铂类化疗一线治疗不可切除的局部晚期或转移性鳞状细胞癌
联合®(贝伐单抗注射液)一线治疗肝细胞癌
此外,信替利单抗单药治疗鳞状细胞癌二线治疗的上市申请已获国家药品监督管理局(NMPA)受理和审评。
两项额外的 临床试验达到了研究终点,包括:
顺铂联合紫杉醇/顺铂和5-氟尿嘧啶一线治疗晚期或转移性食管鳞状细胞癌的国际多中心III期临床试验
晚期/转移性食管鳞状细胞癌二线治疗II期临床试验
2021年5月,信迪利单抗联合培美曲塞和铂类用于非鳞状细胞癌一线治疗的上市申请已被美国FDA正式受理和审评。
信迪利单抗已于2019年11月成功进入中国国家医保目录,成为当年国内首个也是唯一一个PD-1抑制剂。
关于 ®(贝伐单抗注射液)
大禹通®是贝伐单抗注射液的生物类似药,又称重组抗VEGF人源化单克隆抗体注射液。VEGF是血管生成过程中的重要因子,并且在大多数人肿瘤内皮细胞中病理性过表达。抗VEGF抗体可以高亲和力选择性地结合VEGF,通过阻断VEGF与其血管内皮细胞表面受体的结合,阻断PI3K-Akt/PKB和Ras-Raf-MEK-ERK等信号通路的转导. 可抑制血管内皮细胞的生长、增殖、迁移和血管生成,降低血管通透性,阻断肿瘤组织的血液供应,抑制肿瘤细胞的增殖和转移,诱导肿瘤细胞凋亡,从而达到抗肿瘤治疗效果。 . 自推出以来,原研药贝伐单抗注射液已在全球获批用于治疗非小细胞肺癌、转移性结直肠癌、胶质母细胞瘤、肾细胞癌、宫颈癌、卵巢癌、输卵管癌、腹膜癌等多种实体瘤,其显着的疗效和良好的安全性已得到普遍认可。在中国,达育通已获批用于晚期非小细胞肺癌、转移性结直肠癌、成人复发性胶质母细胞瘤和肝细胞癌四种适应症。其显着的疗效和良好的安全性已得到普遍认可。在中国,达育通已获批用于晚期非小细胞肺癌、转移性结直肠癌、成人复发性胶质母细胞瘤和肝细胞癌四种适应症。其显着的疗效和良好的安全性已得到普遍认可。在中国,达育通已获批用于晚期非小细胞肺癌、转移性结直肠癌、成人复发性胶质母细胞瘤和肝细胞癌四种适应症。
关于信达
“始于信念,成就于行动”,开发老百姓用得起的优质生物药是信达生物的理想和目标。信达生物成立于2011年,致力于治疗肿瘤、自身免疫、代谢性疾病等重大疾病的创新药物的研发、生产和销售。2018年10月31日,信达生物在香港联合交易所主板上市,股票代码:.
公司自成立以来,凭借创新成果和国际化运营模式,在众多生物制药企业中脱颖而出。建立了包括24个新药品种在内的产品链,涵盖肿瘤、代谢性疾病、自身免疫等疾病领域,其中6个品种入选国家“重大新药创制”项目。公司拥有5个产品(信替利单抗注射液,商品名:®,英文商标:®; ,商品名:®,英文商标:®;阿达木单抗生物仿制药,商品名:Su ®,英文商标:®;利妥昔单抗生物类似药,商品名:®,英文商标:®;口服抑制剂,商品名: ®,英文商标:®)获批上市,其中,信迪利单抗美国上市申请(BLA)获FDA受理,5个品种进入III期或关键临床研究,另有14个产品获批。进入临床研究。信迪利单抗已于2019年11月成功进入国家医保目录,成为当年国内首个也是唯一一个PD-1抑制剂。
信达生物建立了一支包括多位海归专家在内的具有国际先进水平的高端生物制药开发及产业化人才队伍,并与礼来、MD 、韩国等国际合作伙伴达成战略合作。希望与大家一起努力,提高中国生物制药产业的发展水平,满足药品的可及性和人们对生命健康的美好愿望的追求。详情请访问公司网站:.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话