欢迎光临吉康旅!
春节假期后的第一个工作日,CDE发布重磅消息:《生物类似药相似性评价和适应症外推技术指导原则》正式公布,这意味着国内生物类似药的批量采购步伐将加快。
数据显示,2030年我国生物类似药市场规模将达到589亿元,单个产品达到100亿元。业内预测,未来三年,中国有望陆续推出30~50多种生物类似药,竞争远比PD-1激烈。阿达木单抗、利妥昔单抗、曲妥珠单抗、贝伐单抗等重磅生物药被强敌包围。
生物类似药“一致性评价”来了
进入集中采集再获提速
2月18日,国家食品药品监督管理局药品审评中心(CDE)官网发布了《生物类似药相似性评价和适应症外推技术指导原则》,被称为“生物类似药版本一致性原则”。 ”业内人士说。性评价”政策。
指导文件指出,由于生物制品具有分子量大、结构复杂、生物活性对其结构完整性依赖性强、生产工艺复杂等特点,为进一步规范和指导生物类似药的开发和评价,促进生物制药行业健康发展,该指南以《生物类似药开发与评价技术指南(试行)》为基础,进一步补充了生物类似药评价和适应症外推指南,旨在为行业提供、开发商和监管机构。机构提供技术参考。
值得注意的是,与去年8月的征求意见稿相比,该指导文件对生物类似药的“相似性”进行了具体定义——候选药物与已获批注册的参比药大体相似,而它在质量、安全性和有效性方面没有临床意义的差异。
此外,对于业界普遍关注的适应症外推,文件要求这应基于候选药物与参比药物的总体相似性。当直接比对临床试验证明候选药物在至少一个适应症上与参比药临床相似时,可通过科学论证支持其用于国内批准的参比药尚未直接研究过的其他适应症与外推适应症相关的研究数据和信息。不能直接得到适应症的外推,需要根据药物作用机制的特点、发病机制的异同,来比较研究数据的充分性,
由于生物类似药的特殊性,业内分析人士此前曾指出,与化学药可以评价仿制药质量和疗效的一致性不同,生物类似药需要进行相似性评价。在国家集中采购之前,化学仿制药需要通过一致性评价。此次,国家医保局正式发布生物类似药相似性评价及适应症外推指南,极有可能为下一次生物类似药的大规模采购做准备。
生物类似药是时候进行集中收集了吗?
我国生物类似药的研发起步较晚。2015年,国内生物类似药法规明朗化,单克隆抗体研发从创新申报转向类似药申报,越来越多的企业开始布局生物制品。生物制剂和生物仿制药市场具有潜在的高度竞争性。
目前,全国第四批药品集中采购已经开展,明年两批也将成为常态。熟悉集中采购规则的人都知道,对于新进入者来说,带量采购可以节省药品营销推广成本,增加药品销售收入,毛利水平虽然低,但可以提高利润。公司作为一个整体。
将生物类似药纳入批量采购无疑将有利于新进入者,未来市场仍将是少数。国内药企有望通过进口替代或渗透来增加市场份额。不过,此前业界对批量采购生物仿制药有不同看法。
太平洋证券在去年8月的一份报告中指出,生物类似药的壁垒远高于化学仿制药,国内类似药的开发仍处于起步阶段。原研专利到期后,对比药只需进行BE核心试验。生物类似药不仅需要证明临床和非临床体外和体内数据的相似性,还需要比较临床有效性,适应症不同。外推不排除追加试验的可能,临床开发成本(包括开诊所的成本和购买原研药的成本)远高于仿制药。
虽然国内生物类似药研发企业众多,热门靶点聚集在一起,但从全球范围看,同类药与原研之间、同类药与同类药之间的替代尚无共识,且涉及外延。 -适应症。推动核心问题。太平洋证券认为,生物类似药的集中采购短期内依然困难重重,在当前竞争环境下,决定销售格局的因素将是各企业的学术推广能力。
不过,今年2月第四批全国采购招标开标后不久,国家医保局副局长陈金福在国务院政策例行吹风会上回答了有关问题,“质量评价生物类似药和化学药的仿制药方法有区别,但是有严格的质量标准,下一步肯定会纳入集中采购。完全可控……”。
还值得回顾的是,2020年10月9日,国家医保局在十三届全国人大三次会议《关于加快银屑病等疾病医疗保险水平的若干意见》的答复中明确了研究生物制品集中采购。根据政策,生物类似药不属于集中带量采购限制区,适时开展集中带量采购。
农历大年初一,生物类似药相似性评价及适应症外推指南正式上线,生物类似药纳入集中采购恐怕只是时间问题。
生物药集中采购热门品种预测——
阿达拉姆、利妥昔单抗、曲妥珠单抗……
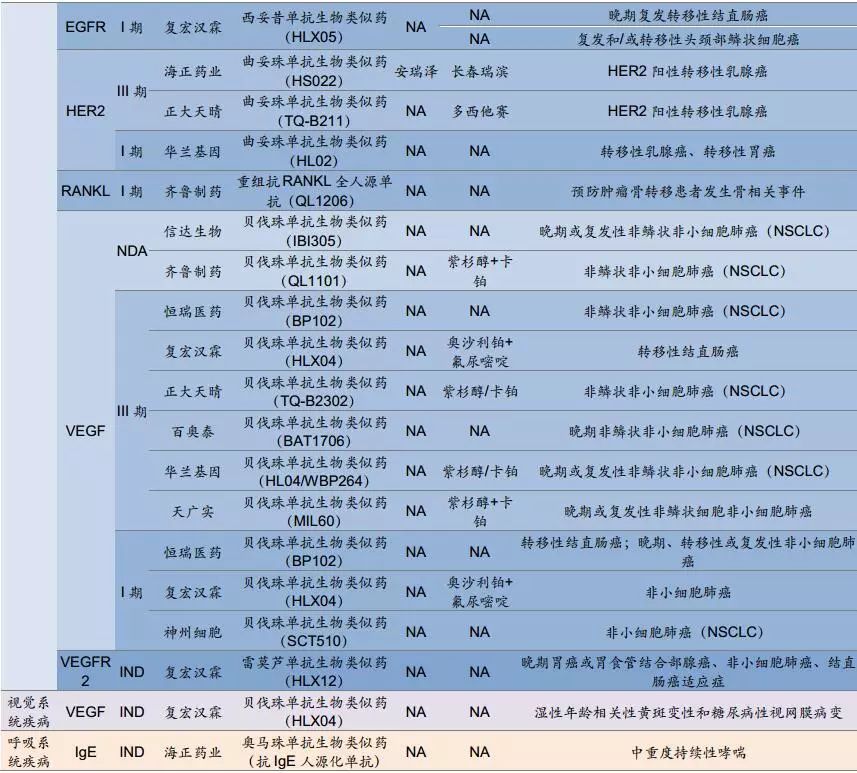
近年来,国内企业不断研发生物类似药。据相关统计,目前我国处于不同研发阶段的生物类似药约有300种,包括阿达木单抗、利妥昔单抗、曲妥珠单抗、贝伐单抗、英夫利昔单抗等。热门研发品种。
阿达木单抗,包括原生产商艾伯维在内,目前在中国最多有5家获批企业,包括Bio-Otai、海正药业、信达生物、复宏复宏汉霖、君实生物与中国生物制药的生物仿制药也在审批中。
专利到期,生物类似药陆续获批上市,2020年修美乐依然稳居第一,修美乐又逼近200亿美元,但修美乐也有隐忧,增速不容乐观,只有3.@ >5%。此前曾预测,到2026年,修美乐的全球销售额可能会下降到6美元8.3亿美元。还有传言说,快速增长的K药未来将取代修美乐成为“药王”。
根据弗若斯特沙利文报告,2023年中国阿达木单抗生物类似药市场规模将增至47亿元,2030年将达到115亿元。随着越来越多的生物类似药上市,修美乐在国内的市场份额也将逐渐被挤压。如果将已纳入医保目录的阿达木单抗纳入集中采购,后续价格将更实惠。.
除了最赚钱的修美乐,罗氏的超重度肿瘤“三驾马车”也备受关注。其三大王牌药物(,通用名: )、(,通用名: for )和(,通用名: )也面临专利到期、竞品越来越多的情况。
在罗氏的三大王牌药物中,利妥昔单抗和贝伐单抗在中国已形成1+2的竞争格局。其中,包括恒瑞医药在内的贝伐单抗有4个。即将获批上市,强敌蓄势待发。此外,根据FDA生物类似药数据库显示,截至2020年12月,FDA批准的近30种生物类似药中,有10种针对罗氏的三大生物药。
罗氏2020年财报显示,2020年三大王牌曲妥珠单抗、贝伐单抗、利妥昔单抗的销售额均将萎缩至50亿瑞士法郎以下,降幅超过预期,同比-38%,-29%,- 35%,2020 年累计减少 66 亿瑞士法郎。
近日,对2021年的热销药品进行了预测。罗氏的 和 跌出前十。前十名由修美乐、科瑞达、瑞复美、、组成。、奥迪沃、斯塔诺、比托维、艾克、拜瑞妥占据。
在生物类似药的猛烈冲击下,罗氏昔日的王牌药物将无法再延续昔日的辉煌。随着生物类似药相似性评价的出现和批量采购的发展,未来的竞争环境将更加激烈。
生物制品集中采购相关政策规则的出台无疑会有自己的“玩法”,但一旦批量采购启动,国内市场将面临洗牌,生物制品整体产业结构将有望得到优化和调整。让我们等着看。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话