欢迎光临吉康旅!
胶质瘤起源于胶质细胞,是颅内最常见的恶性肿瘤之一,年发病率约为3~6.4/100,000。胶质瘤分为局限性胶质瘤和弥漫性胶质瘤。本文主要讨论弥漫性胶质瘤。胶质母细胞瘤(GBM,WHO 4级)是最常见的弥漫性胶质瘤,即使经过手术、放疗和化疗的标准治疗,5年生存率仍低于10%。
近年来,胶质瘤诊疗的进展主要包括分子病理学的提出、传统疗法的优化和肿瘤电场疗法等。此外,分子靶向、免疫治疗等新疗法积累了越来越多的经验,但能够真正改变临床实践的成果寥寥无几。下面将介绍胶质瘤治疗的现状和研究进展,以结合最新进展加强对这一难治性疾病的认识。
1.诊断和治疗指南更新
胶质瘤的标准治疗是手术切除,结合放疗和化疗。在现代循证医学中,诊疗实践指南是规范日常临床决策和患者管理的主要依据。《中国中枢神经系统胶质瘤诊疗指南》是我国首个针对恶性中枢神经系统肿瘤制定的指南,现已更新3次(2009、2012、 2015 年版);2018 2020年,国家卫健委发布《脑胶质瘤诊疗指南》;2020年,中国胶质瘤协作组牵头,与亚洲多个神经肿瘤中心合作,发布成人弥漫性胶质瘤临床管理国际指南。血浆瘤标准化诊断和治疗的主要指南和指南。
此外,美国国家综合癌症网络(NCCN)和欧洲神经肿瘤学会(-,EANO)定期发布的相关指南也是了解胶质瘤最新进展和选择治疗方案的重要参考,一般得到世界各地临床医生的认可。
2.分子病理学和综合诊断
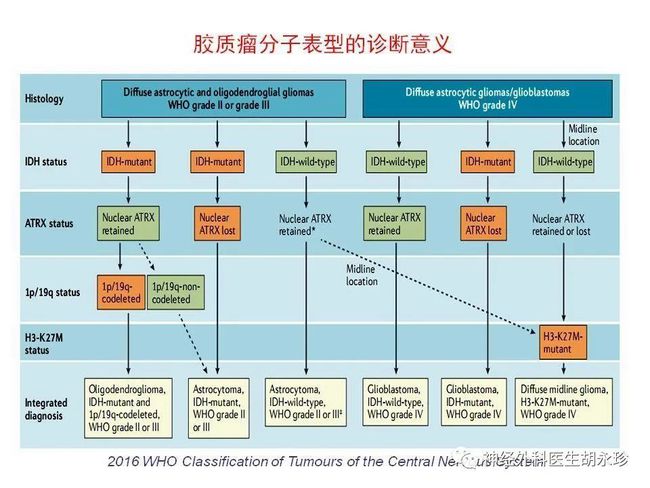
病理诊断和肿瘤分类是影响胶质瘤术后治疗方案选择的重要因素。2016版WHO中枢神经系统肿瘤分类是目前胶质瘤病理诊断的依据。其特点是引入分子病理学概念,需要检测异柠檬酸脱氢酶(IDH)突变、染色质1p/19q联合缺失等分子指标,对胶质瘤进行组织病理学和分子病理学综合诊断和分类。
越来越多的证据表明,具有 TERT 启动子突变、EGFR 扩增或染色质 7+/10- 拷贝数变异的成人 IDH 野生型星形细胞肿瘤,即使在没有微血管增殖和肿瘤坏死等组织学变化的情况下,GBM 也可以确诊;对于IDH突变型星形细胞瘤,具有/B突变的星形细胞瘤恶性程度较高,可诊断为WHO 4级星形细胞瘤,这些发现也被纳入最新版的WHO神经系统肿瘤分类中。
新的WHO分类总结并推荐了更多的分子指标,并对胶质瘤的病理分类进行了多次修订,包括胶质瘤的分类以区分成人和儿童亚型;成人弥漫性胶质瘤分类为Jane,仅提出3类(即GBM,IDH野生型;星形细胞瘤,IDH-突变型;少突胶质细胞瘤,IDH-突变合并1p/19q缺失),强调分子检测的重要性;肿瘤分级在肿瘤类型内进行,结合组织学和分子特征。这些分子指标的检测有待进一步规范,新版WHO分类将在国内临床实践中逐步推广。
3.手术治疗
手术是胶质瘤治疗的基石,最大限度安全切除是胶质瘤手术的原则。肿瘤全切除与更长的患者生存期相关;相比之下,大量证据表明,术后神经损伤和损伤不仅影响患者的生活质量,而且还与预后较差有关。因此,胶质瘤手术在尽可能保留神经功能的前提下,病灶强化的患者需要将强化病灶完全切除,无强化的患者需要切除T2/异常信号灶。
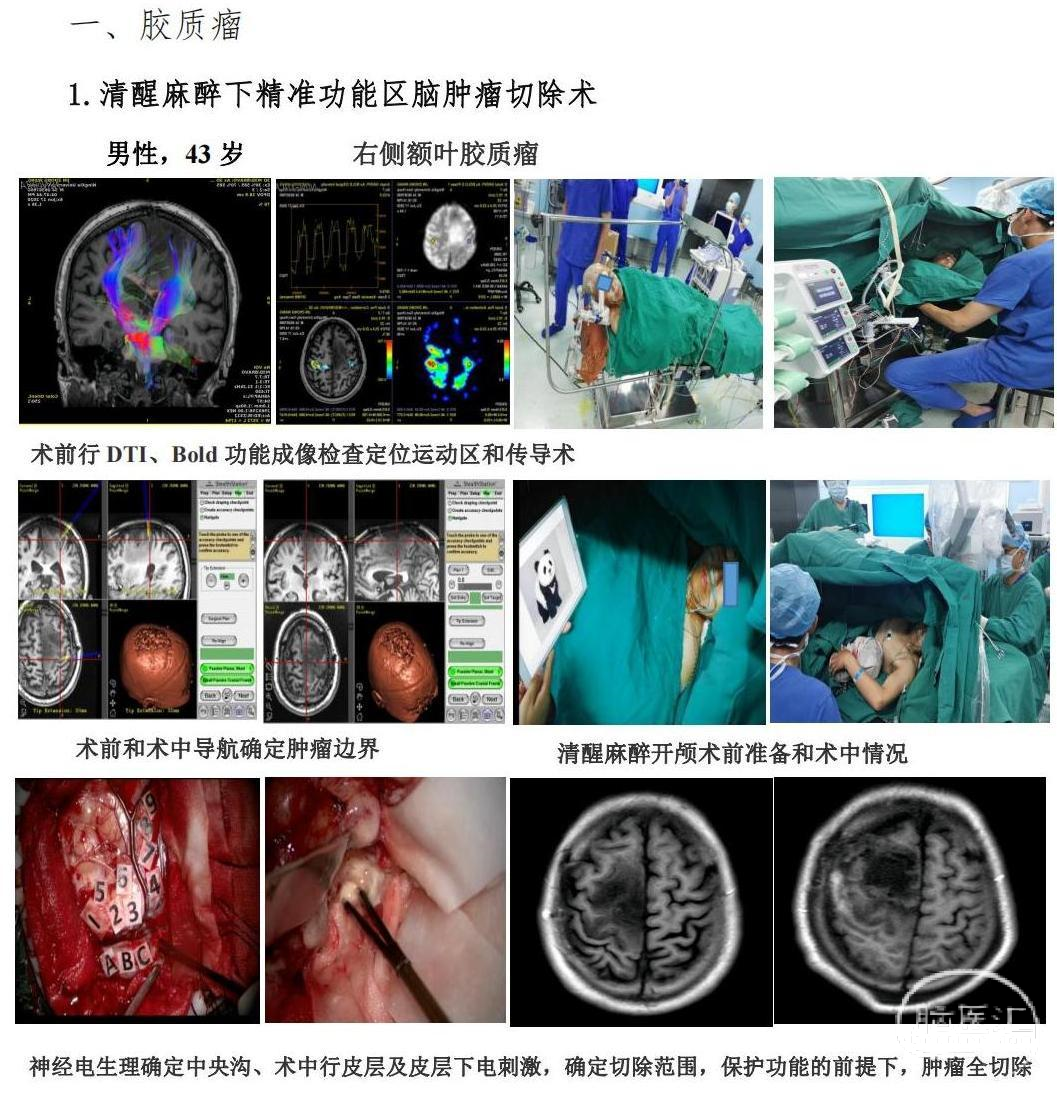
脑功能区域的局限以及胶质瘤弥漫性生长导致肿瘤边界难以区分是影响胶质瘤切除范围的主要因素。多模态MR、神经导航、皮质/皮质下刺激和唤醒手术可应用于临床。提高功能脑区的定位和保护,利用荧光辅助、术中MR、术中超声、IDH突变快速质谱等新技术提高肿瘤边界的识别和切除。
此外,扩大肿瘤切除是否能带来更多的生存获益也是一个有争议的问题。最近一项针对 GBM 的多中心回顾性研究表明,进一步切除强化的病灶可延长 65 岁以下患者和 65 岁以上 IDH 突变老年患者的总生存期 (OS),从而为临床手术决策提供依据。重要参考。激光间质热疗 (LITT) 可与术中 MR 相结合,对脑部病变进行实时、精确的消融。国内外也有报道LITT治疗胶质瘤,尤其是深部小体积胶质瘤。有条件的中心可以探索和开发这种技术。脑肿瘤治疗新技术。
4.放疗和化疗
放疗是胶质瘤治疗的重要补充,常规放疗剂量为50-60 Gy。比较高剂量(>60 Gy)与常规剂量放疗治疗低级别胶质瘤的研究(最终结果发表于 2020 年)表明,高剂量放疗不会延长低级别胶质瘤患者的生存期。另一项荟萃分析的结果也显示,大剂量放疗并未改善高级别胶质瘤的预后。
替莫唑胺(TMZ)是GBM治疗的一线药物,但TMZ等烷化剂的疗效与胶质瘤甲基鸟嘌呤-DNA甲基转移酶(MGMT)启动子甲基化状态有关,MGMT启动子未甲基化。烷化剂容易对烷化剂产生耐药性,需要探索其他处理方法。 具有独特的双功能 DNA 烷基化活性,是一种独立于 MGMT 机制的细胞毒药物。这是一项用未甲基化的 MGMT 启动子治疗新诊断的 GBM 的 I/II 期临床试验。显示了良好的效果。
相比之下,MGMT 启动子甲基化与烷化剂化疗更好的反应性和预后相关。一项 III 期临床试验(NOA-09) 比较了洛莫司汀(另一种烷化剂)联合 TMZ 与 TMZ 标准疗法治疗新诊断的 MGMT 启动子甲基化 GBM。结果显示,在联合治疗组高达48.1个月,明显高于TMZ标准治疗组(31.4个月),提示烷化剂强化治疗无效在MGMT中,启动子甲基化在胶质瘤中的积极作用,但也需要注意化疗毒性的累积。
该研究是一项大型 III 期临床研究,评估同步放疗或辅助 TMZ 化疗对 1p/19q 非组合缺失的间变性星形细胞瘤(WHO 3 级)的疗效。中期结果表明,与单独放疗相比,放疗后辅助TMZ可以延长。患者存活,但同步放疗和辅助TMZ的作用尚不清楚。
PCV(丙卡巴肼、洛莫司汀、长春新碱)方案推荐用于治疗低级别胶质瘤的一线化疗。研究发现,对于 IDH 突变的低级别胶质瘤,无论有无 1p/19q 共缺失,与单纯放疗相比,放疗联合 PCV 均可延长无进展生存期(PFS)和 OS。探讨TMZ在低级别胶质瘤中的作用,发现放疗后接受TMZ辅助治疗的患者生存率优于历史对照组。因此,TMZ在中国常用于治疗WHO 2级和3级胶质瘤。
5.肿瘤治疗领域及其他物理治疗方法
肿瘤治疗场(-,TTF)是一种头戴式脑肿瘤治疗设备,通过干扰微管蛋白和蛋白质来抑制肿瘤细胞分裂和增殖。2015年TTF治疗GBM的III期临床试验结果发现,TTF联合TMZ治疗较TMZ单独治疗可显着提高初诊GBM的OS(20.9个月vs . 16. 0 个月)。因此,国内外指南均推荐TMZ联合TTF作为新诊断GBM的一线辅助治疗(I级证据),这也是胶质瘤治疗史上的一个突破。
对于复发性GBM,虽然III期临床试验结果显示TTF与研究者选择的化疗相比并没有延长患者的生存期,但考虑到TTF全身毒副作用较小,且有改善临床结局的趋势在现实世界的研究中,治疗复发性 GBM 的指南也推荐使用它(证据 2B)。
TTF 于 2020 年正式在中国推出,但由于成本高昂,尚未普及。目前,国内多种TTF装置及联合治疗方案也在积极研发中,希望进一步扩大TTF在恶性胶质瘤中的应用。抗肿瘤药物不易穿透血脑屏障,这也是胶质瘤治疗困难的原因之一。可以对低频脉冲超声(low-,LIPU)进行编程以打开血脑屏障,一项临床试验( )正在评估复发性 GBM 中的 LIPU 装置。初步结果表明,它可以增加化疗的疗效。
6.靶向免疫治疗
即使经过手术、放化疗和TTF治疗,恶性胶质瘤的预后仍不理想,需要积极探索更多新的治疗方法。分子靶向和免疫治疗在其他恶性肿瘤中发展迅速,也是发展胶质瘤新疗法的重要方向。贝伐单抗是复发性GBM指南推荐的首个靶向药物,临床试验结果表明贝伐单抗只能延长患者的PFS,不能延长OS。
但该研究的分子亚组分析发现,贝伐单抗治疗pre-TCGA神经元GBM可以延长OS(贝伐单抗组17.1个月,安慰剂组12.8个月),结果被推荐采用最新的欧美指南。瑞戈非尼()是一种多激酶抑制剂,靶向性、FGFR等(II期临床)结果表明,与洛莫司汀相比,瑞戈非尼可提高复发性GBM患者的生存期(中位OS:7.4个月vs. 5.6 个月)。
安罗替尼是国内首创的多靶点口服小分子抑制剂。目前,有临床试验研究安罗替尼联合替莫唑胺剂量密集方案治疗复发性 GBM 的潜在疗效。另一项国内领先研究发现继发性GBM具有-MET融合基因,此类患者预后较差,而针对PRZ1-MET融合基因的MET激酶抑制剂-在临床前研究中具有良好的抗肿瘤作用,相关临床试验也在招募患者在中国多个中心。
BRAF 和 NF1 基因变化在儿童胶质瘤中很常见。BRAF抑制剂()和下游MEK1/2抑制剂()已在II期临床试验中取得初步成果。以PD-1单克隆抗体为代表的免疫检查点抑制剂成为近年来肿瘤免疫调节治疗的热点。临床试验如火如荼,在肺癌、恶性黑色素瘤、头颈癌方面也取得了成功。但从几项已完成的III期临床试验结果来看,PD-1 mAb在GBM中的疗效并不理想。
一项 III 期临床研究()比较了 PD-1 单克隆抗体纳武单抗()和贝伐单抗在复发性 GBM 中的疗效,但遗憾的是没有发现纳武单抗可以延长生存期。新诊断的具有未甲基化 MGMT 启动子的 GBM 的 -498 研究表明,与标准治疗相比,放疗联合 不会延长 OS。
-548 评估了 联合 TMZ 在新诊断的 MGMT 启动子甲基化 GBM 中的疗效,初步结果显示 PFS 没有益处,OS 结果未公布。遗传和免疫组学研究确定了具有 BRAF 和基因突变、MAPK 信号激活、更高的淋巴细胞瘤内浸润、更低的 TCR 克隆多样性和极低的突变负荷水平对治疗反应更好的 PD-1 耐药复发性胶质瘤。
此外,一项II期临床试验发现,PD-1 mAb的疗效可能与使用时机有关。本研究比较了手术前使用 PD-1 mAb(新辅助治疗)和术后辅助使用 PD-1 mAb 在可手术切除的复发性 GBM 中的效果,结果表明 PD-1 新辅助治疗显着改善了患者的 OS。
针对其他免疫检查点分子的临床试验也在进行中,例如同步放疗和辅助 PD-L1 抑制剂治疗新诊断的 MGMT 启动子未甲基化 GBM 的 II 期临床试验,涉及 40 名患者。Bit OS 15.1 个月以上,优于历史数据。肿瘤疫苗是另一种具有临床转化前景的免疫疗法。基于肿瘤特异性抗原靶点产生的肽序列,可刺激机体免疫系统杀死肿瘤细胞,属于主动免疫疗法的范畴。
肿瘤疫苗包括单靶点疫苗、多靶点疫苗和个体化疫苗,靶点如、IDH1-。它是一种靶向肽疫苗。在其治疗新诊断GBM的II期临床试验中,患者的中位PFS和OS分别达到15.5和30.5,已被美国FDA批准为一种治疗GBM的孤儿药。
它是一种由完全灭活的肿瘤细胞和肿瘤细胞裂解物组成的肿瘤疫苗。2020年美国神经肿瘤学年会公布了其治疗复发性GBM的II期临床试验初步结果,发现接受治疗的13名患者中位OS接近1年,与安慰剂相比效果显着团体。
2019年,《》杂志报道了两项新抗原疫苗治疗GBM的临床研究。采用基因测序方法鉴定突变位点和新抗原表位后生产的个体化肿瘤疫苗是安全的,可以产生明显的特异性免疫。功效; 在疗效方面,中位 PFS 为 14.2 个月,中位 OS 为 29 个月,初步结果令人鼓舞。
此外,以往对嵌合抗原受体T细胞(CAR-T)和溶瘤病毒等其他免疫疗法的研究也显示出良好的抗神经胶质瘤作用。例如,它是一种重组脊髓灰质炎病毒,GBM广泛表达脊髓灰质炎病毒受体,两者具有结合力。肿瘤内注射病毒治疗复发性 GBM 的临床试验结果显示,61 名入组患者中有 21% 的患者存活了 3 年以上。
总的来说,胶质瘤的分子靶向和免疫治疗仍处于临床探索阶段,相关临床试验结果需要持续关注。少数完成III期临床试验且有效的新药(如瑞格非尼等)可在充分知情的情况下用于临床试验。
7.功效评价与MDT模型
20%-30%接受放疗联合TMZ等烷化剂治疗的胶质瘤患者在治疗过程中会出现影像学假性进展,尤其是在治疗初期,表现为强化病灶暂时扩大,易相关对疾病。真正的肿瘤进展令人困惑。另外,由于贝伐单抗提高了肿瘤血管的通透性,在影像学上往往能有效缓解强化病灶和水肿症状,但这并不等同于真正的抗肿瘤反应,T2/上的病灶可以持续. 进展,最终证明是肿瘤复发。因此,目前推荐使用RANO标准来评价胶质瘤的疗效,需要结合磁共振T1增强序列,
RANO援助组还针对胶质瘤免疫治疗、儿童胶质瘤治疗、神经功能量化等具体情况提出了一系列疗效评价建议,可以指导临床实践。由于胶质瘤病理分型、治疗方法和疗效评价的复杂性和多样性,组建多学科团队(m,MDT),采用多学科综合治疗也是国内外胶质瘤诊疗模式。
胶质瘤MDT是根据不同患者的病情和实际情况,由神经外科、影像科、病理科、放疗科、神经肿瘤科的多学科专家共同讨论确定。给出治疗方案,并定期对治疗方案进行疗效评价和必要的调整。可在患者管理全过程中多次组织MDT,克服单一专科诊疗的局限,为患者提供更加系统、持续的个性化综合治疗,进一步提高患者的治疗效果和生活质量。
8.总结
近十年来,我国胶质瘤的治疗并没有太大的突破,传统的手术、放疗、化疗“三驾马车”仍是胶质瘤的标准治疗方法。分子病理学的引入和肿瘤分类的更新具有革命性意义,越来越多的分子标志物可用于肿瘤诊断、预后评估和指导个体化治疗。
TTF等脑肿瘤物理治疗是胶质瘤治疗的一个新方向,也取得了一定的成功。有必要继续推动其在中国的普及。靶向治疗和免疫治疗发展相对缓慢,这与恶性胶质瘤的高异质性、免疫抑制特性和获得性耐药机制有关。,以阐明肿瘤治疗耐药的分子机制,发现新的分子治疗靶点。
多靶点和多种疗法的组合可能是克服胶质瘤异质性的一种方法,目前许多临床试验都在探索联合疗法的实际作用。中国临床试验的发展越来越受到重视。临床试验是验证新疗法真正疗效的主要方式。需要进一步完善临床试验的设计、合作和实施管理。同时,新疗法的开发要注重多学科合作,基础研究与临床研究相结合。相信神经胶质瘤的诊治现状将得到进一步改善。
资料来源:李德培,陈忠平。胶质瘤治疗现状与进展[J]. 实用医学杂志, 2021, 37(18):2312-2316.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话