欢迎光临吉康旅!
1月25日,国家食品药品监督管理总局发布了吉非替尼片说明书修订公告(2021年第17号),对吉非替尼片说明书【不良反应】和【注意事项】项目进行了修订。
详情如下:
一、【不良反应】
添加以下内容:
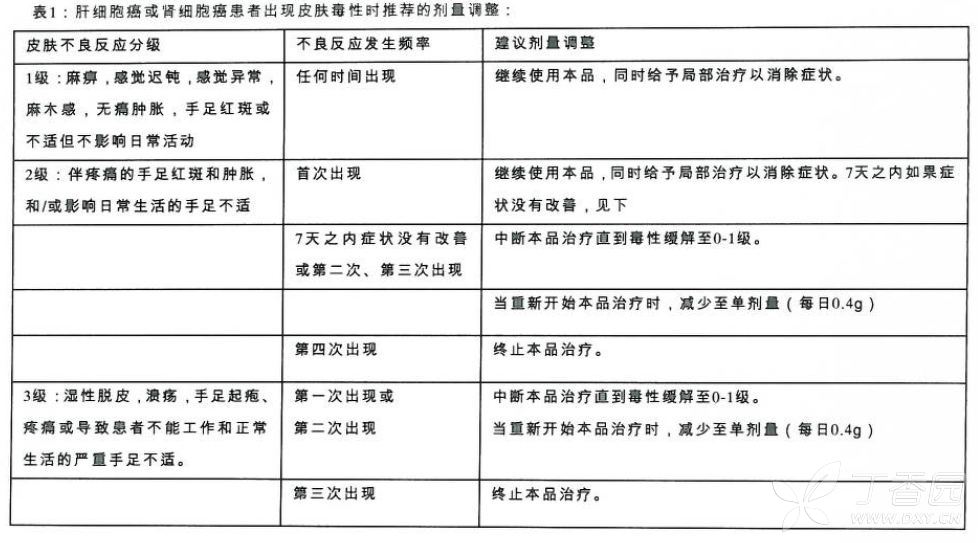
上市后经验:
吉非替尼片上市后观察到以下不良反应。这些不良反应来自不确定样本量的自发报告,因此难以准确估计其发生频率。
皮肤及皮下组织异常:皮肤不良反应是吉非替尼片非常常见的不良反应之一,可发生于全身任何部位,多表现为轻中度皮疹、干燥、瘙痒等。上市后不良反应监测曾收到掌跖红斑综合征(手足综合征、手足皮肤反应)的报告,表现为手足感觉异常、红斑、脱屑、水疱、出血、皲裂、水肿或角化过度等。 .
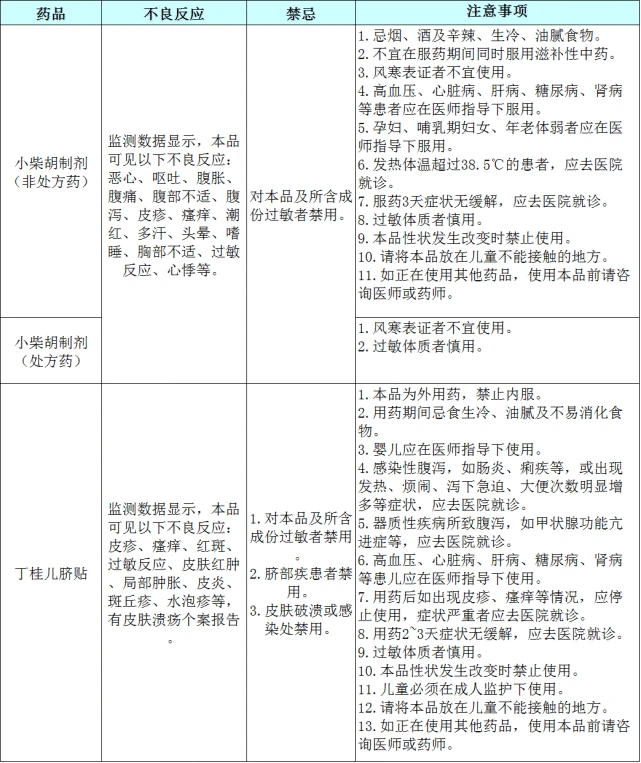
二、【注意事项】
添加以下内容:
皮肤毒性:严重的皮肤不良反应(NCI 3级或以上)需要停药(见【用法用量】)。皮肤反应的早期干预有利于吉非替尼的持续治疗。治疗期间出现感觉异常、红斑、脱屑、水疱、出血、皲裂、水肿或角化过度的患者应立即就医。
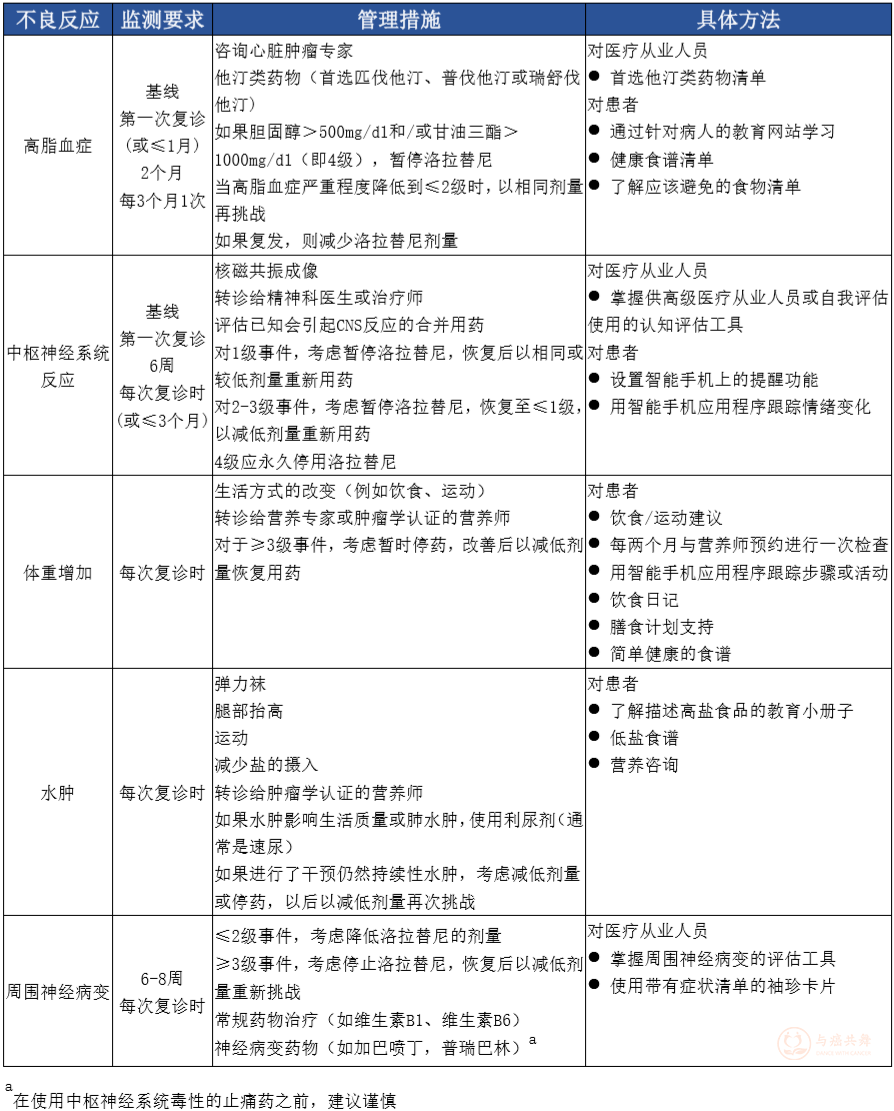
上市后不良反应监测已收到掌跖红斑综合征(手足综合征,手足皮肤反应)的报告,患者用药时应注意减少皮肤压力和摩擦力,尤其要防止对手掌和足底造成压力。脚。
(注:本手册其他内容与上述修订要求不一致的,应一并修订。)
国家食品药品监督管理总局要求各吉非替尼片生产企业按照《药品注册管理办法》等相关规定,按照吉非替尼片说明书修订要求,提交补充说明书修订申请,并于2021年4月20日前报国家药品审评中心局或省级药品监督管理部门备案。
修改内容涉及药品标签的,一并修改;标签的使用说明等内容应与原批准内容一致。所有已出厂的药品说明书和标签,应在补充申请后9个月内更换。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话
帕纳替尼(Ponatinib)是阿瑞雅德(Ariad)开发的三代BCR-ABL酪氨酸激酶抑制剂(TKIs),商品名为Iclusig。其经过一期和二期临床试验,...
伏立康唑属三唑类抗真菌药物,其抗菌谱广,抗菌活性高。美国感染疾病协会( IDSA) 2016年最新更新的指南中将伏立康唑作为侵袭性曲霉菌、...
瑞戈非尼/瑞格非尼(Regorafenib)是VEGFR酪氨酸激酶小分子抑制剂,是第一个证实的对生存有益的酪氨酸激酶抑制剂,可特异性与多个酪氨酸激酶...
商品名:Lynparza(利普卓) 通用名:olaparib(奥拉帕尼/奥拉帕利) 靶点:PARP 原研厂家:阿斯利康 规格:150/100mg ...
随着分子生物学技术的飞速发展,学术界对髓母细胞瘤的分子分型有了较为深入的研究。2016年WHO分类标准将髓母细胞瘤分为三个亚型,即WNT型...








