欢迎光临吉康旅!
今年8月20日是诺贝尔医学和生理学奖得主、德国科学家保罗·埃利希博士逝世106周年。除了以在免疫学理论和血清疗法方面的工作而闻名之外, 博士是第一个发现“血脑屏障”现象的人。1895年,他发现外周注射染料后,大脑无法染色。虽然当时他没有对这一现象给出准确的解释,但他的发现直接开启了后续对血脑屏障(-,简称“BBB”。)的深入研究。到现在,深入研究血脑屏障物质转运蛋白,探索其潜在利用价值,对于寻找治疗中枢神经系统疾病的新药靶点,更有效地治疗中枢神经系统疾病具有重要意义。因此,对其结构、功能以及如何克服脑血屏障的研究在学术界和制药业(尤其是中枢神经系统药企)都有广泛而深入的研究。
中枢神经系统疾病/药物简介
中枢神经系统疾病是指影响大脑或脊髓结构和功能的神经系统疾病,主要包括神经退行性疾病、功能障碍、结构障碍和中枢神经系统感染等。最广为人知的中枢疾病包括阿尔茨海默病(又称阿尔茨海默病,AD)、帕金森病(',PD)、抑郁症()、精神分裂症()、癫痫()、中风(又称中风),如以及在肿瘤学领域经常听到的原发性脑肿瘤和脑转移瘤( )。更准确地说,约翰霍普金斯研究所对中枢神经系统的损害分类如下:
中枢神经系统药物(CNS)通常是指治疗功能障碍或神经退行性疾病的药物。这些损伤涉及神经系统的致病性破坏,往往难以治愈,需要患者长期服药。但随着基因和细胞疗法的兴起,对于帕金森病、肌萎缩侧索硬化症和亨廷顿病等疾病,单次或长期间歇给药有可能实现临床治愈,近年来取得了突破性进展。性进步。
中枢神经系统药物研发现状
据联合国卫生组织估计,全球约有 1/6 的人口患有神经系统疾病。中国中枢神经系统药物销售收入从2015年的1440亿元增长到2019年的2043亿元,年复合增长率9.1%。%复合年增长率将进一步提高,到2024年以更高的增长率达到2509亿元。
尽管近年来中枢神经系统药物的市场规模不断扩大,但与其他治疗领域相比,中枢神经系统具有高风险、高效益的特点。高风险主要是因为中枢神经系统药物的研发难度很大,从临床I期到上市的成功率只有8.4%。因此,鉴于中枢神经系统药物研发人员流失率高,不少药企决定减少中枢神经系统研究,有的甚至直接关闭了中枢神经系统药物研发中心。例如,葛兰素史克于2017年关闭了中国的全球神经药物研发中心。具体来说,中枢神经系统药物研发的难点主要在于:
但令人欣慰的是,尽管中枢神经系统药物研发面临诸多挑战,但仍有大量拥护者继续在该领域工作。在中枢神经系统领域,如专注于原发性脑肿瘤/肿瘤脑转移药物研发的赞荣医药、碧晨医药,以及植根于中枢神经系统药物研发的恩华医药。
血脑屏障简介
如前所述,1895年,埃利希博士在研究染料时意外发现了“血脑屏障”现象。他和他的学生埃德温·戈德曼( )给动物静脉注射了蓝色染料,发现除了大脑之外几乎所有器官都变成了蓝色。随后,其他科学家在 1900 年观察到了类似的现象,并首先提出了“血脑屏障”的概念。
后来经过近20年的研究,大脑与外周组织之间存在血脑屏障这一事实基本被广泛认可,但直到电子显微镜在1960 年代。,科学家们能够直接观察到所谓的血脑屏障。以下是血脑屏障发现历史上的一些里程碑
纪念碑事件:
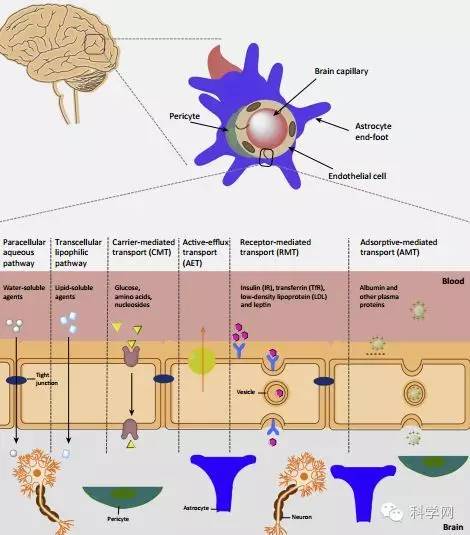
血脑屏障(-,简称“BBB”)是指由脑毛细血管壁和神经胶质细胞形成的血液与脑组织之间的屏障。、星形胶质细胞、周细胞、基底膜等成分。脑毛细血管内皮细胞排列紧密,通常只允许气体分子和分子量相对较小的脂溶性分子通过。不幸的是,它也是治疗药物进入大脑的主要障碍,阻止了大多数治疗中枢神经系统CNS疾病的药物通过BBB到达大脑中的有效治疗浓度。
药物分子主要通过以下途径进入脑实质:一是被动扩散,大部分小分子化合物通过这种方式通过血脑屏障进入脑内,但可能受到主动外排的限制;另一种是通过细胞间隙。,这种方法通常只适用于一些极性低分子化合物;三是脑内皮细胞表达的转运蛋白介导的摄取;第四种是由脑内皮细胞表达的受体蛋白介导的转运。
BBB的另一个重要特点是它在脑毛细血管内皮细胞膜上含有多种物质转运蛋白,其中大部分与脑营养物质的跨膜转运有关,如葡萄糖转运蛋白、肽转运蛋白、转铁蛋白受体等。为外周血和大脑之间的物质交换提供了必要的条件。体内生理生化环境的变化可能会影响这些蛋白质的表达或功能。反之,这些转运蛋白的异常表达或功能也会影响大脑乃至全身的功能,甚至诱发严重的疾病。一些治疗脑病的药物血脑屏障通透性低,容易产生耐药性。可以调节这些转运蛋白的功能或表达,或者对药物结构进行修饰和修饰,以增加药物与这些转运蛋白的亲和力,从而提高药物的疗效。在大脑中分布。
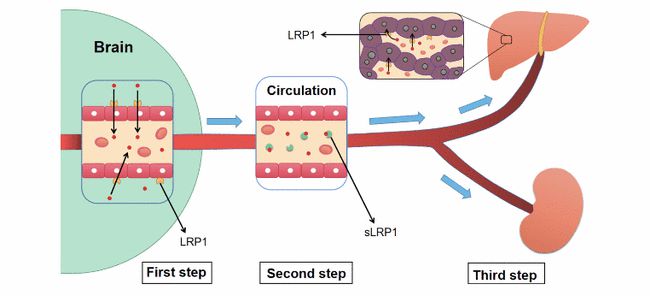
同时,BBB实现防止外来有害物质进入脑实质的另一个重要因素是BBB相关外排转运蛋白的参与。外排转运蛋白是指位于细胞生物膜上,具有将分子从细胞内外排出到细胞外的能力的转运蛋白。已知的外排转运蛋白是 P 糖蛋白 (P-gp)、多药耐药性药物相关蛋白 (MRP)、乳腺癌耐药性蛋白 (BCRP) 和肺耐药性蛋白 (LRP)。这些蛋白质广泛分布于正常组织,如脑、肝、肾、肠、胰腺等,具有分泌和排泄功能的组织,在血脑屏障、血睾丸屏障和血液中起着重要的屏障作用。 - 胎儿屏障。
疾病对血脑屏障的影响
在 BBB 里程碑的介绍中已经提到了疾病状态对 BBB 的影响,即在颈动脉内施用高渗溶液后短暂的 BBB 打开或中断。下面总结了常见的中枢神经系统疾病对 BBB 的影响:
可见,上面总结的大部分疾病都可以降低或破坏血脑屏障的完整性,例如通过降低紧密结合蛋白和P-gp的表达,或者直接导致血脑屏障的渗漏,所以很自然认为 BBB 是一种药物分子的通透性实际上在这些患者中更大,临床上可以观察到药物在患者大脑中的暴露量会高于动物模型预测的药物进入大脑的能力. .
例如,拉帕替尼(它是 P-gp 和 BCRP 的底物,但在高浓度时抑制两种外排转运蛋白)也被发现在患有脑转移的乳腺癌患者中具有更高的脑暴露量。定量地,PET 研究还表明,拉帕替尼在有肿瘤转移的脑中高于正常脑。此外,脑转移瘤患者的脑脊液中也能检测到一些大分子抗体药物(如抗肿瘤药赫赛汀),且蓄积量也较高,进一步说明脑肿瘤可破坏血脑屏障的完整性。
基于这一现象,可以推测,对于脑灌注药物的开发,临床前评价标准可以降低。例如,对于脑灌注的化合物,临床前动物通常需要 Kp, uu(即脑中游离药物与血液的比率)。值为1表示药物可以从血液中自由进入大脑。进不了大脑)大于0.5,当然这个值会因公司而异,但总的原则是越接近1越好,至少应该大于0.3。
在目前的临床前试验中,当Kp和uu确定时,所有的健康动物都被使用,它们的BBB是完整的。因此,与临床相比,对化合物进入大脑的限制更为严格,因此应考虑适当降低临床前要求,如设置0.2或更低。
血脑屏障的物种差异
在新药开发中选择合适的动物模型对药物评价起着至关重要的作用,因此有必要从翻译的角度分析物种差异。例如,在筛选化合物入脑时,大鼠实验是最常用的动物模型,通过比较化合物在大脑中与血液的浓度比来判断入脑程度。如果化合物被动扩散较好且不是人 P-gp 底物,则在该模型中未在大鼠中发现足够的脑暴露,很可能是因为该化合物是大鼠 P-gp 底物而不是人 P-gp 底物。
中枢神经系统药物穿透血脑屏障的策略
1、小分子药物
根据血脑屏障的生理结构,比较容易推导出进入大脑的小分子化合物的一些基本理化性质,如亲油性高、分子量不太高、电负性低等。这些性质是为了保证药物分子可以很容易地通过血脑屏障释放出来。有科学家总结了 48 种 CNS 和 45 种非 CNS 小分子化合物在理化性质上的差异。可以看出,两类化合物在脂溶性、氢键供体数和可旋转键数等方面存在显着差异。在中枢神经系统药物方面,高于非中枢神经系统药物。同时,符合理论,CNS药物具有更高的渗透性和更低的成为P-gp底物的概率。
物理和化学特性
中枢神经系统
非中枢神经系统
百分比(CNS/非CNS)
分子量
319
330
97
被动扩散渗透系数
474
331
143
%P-gp底物比例
15
42
35
3.43
2.78
123
2.08
1.07
194
PSA
40.5
56.1
72
氢键供体数
0.85
1.56
54
氢键受体数
3.56
4.51
79
可旋转键数
1.27
2.18
58
芳香环数
1.92
1.93
99
BBB的生理结构导致其密度较高,渗透性较低,因此要求该化合物具有更高的渗透性或膜渗透性。对于口服药物,要求它们可以通过肠细胞膜到达全身血液系统。与药物分子在肠道的通透性相比,对血脑屏障的要求更高。原因是:一是血管-脑内药物浓度梯度远低于肠道内;第二,大脑的蛋白质结合率普遍较低。三是与其他组织相比,由于TJ的存在,药物分子在脑血管中缺乏细胞间运输,也缺乏有间隙的毛细血管;第四,药物分子在大脑血管中的停留时间更短。
在非外排转运蛋白底物方面,P-gp、BCRP等外排转运蛋白在血脑屏障上高表达,是许多药物分子(如化疗药物)不能通过血脑屏障进入大脑的原因。作为此类外排转运蛋白底物的化合物分子需要从早期药物筛选中剔除。为了评估药物分子是否是外排转运蛋白的底物,通常需要评估外排速率 ( , ER)。以P-gp为例,如果ER大于2,则该化合物是转运蛋白的底物。
以奥希替尼()为例,作为第三代EGFR抑制剂,可克服第一代的耐药性,已广泛应用于EGFR突变的一线和二线非小细胞肺癌症治疗。也取得了不错的成绩。下表总结了不同 EGFR 抑制剂在小鼠模型中的入脑情况。可以看出,奥希替尼比第一代吉非替尼、第二代阿法替尼和第三代表现出更好的入脑能力,最高浓度(Cmax)的Kp可以达到3.41,是十倍以上吉非替尼。
剂量(mpk)
25
6.25
100
Cmax(μM)
0.82
0.82
3.32
Cmax(μM)
2.78
0.17
BLQ
/
3.41
0.21
同时,虽然在临床前动物模型中未发现吉非替尼和阿法替尼具有理想的脑穿透能力(Kp临床研究也证实了这一点,但吉非替尼和另一代EGFR抑制剂厄洛替尼的脑内药物浓度)远高于阿法替尼,药物入脑的效果也如预期体现在临床疗效上,阿法替尼对脑转移患者的疗效低于阿法替尼吉非替尼和厄洛替尼,如果反应率为35% vs 80%,且无进展生存期为 4 个月 vs > 6 个月,虽然不同研究中直接比较临床疗效不够准确,但仍能看出对脑肿瘤疗效的大致差异。
前面也提到过脑肿瘤会破坏血脑屏障,所以虽然吉非替尼在临床前没有被证明符合中枢神经系统药物的标准,但临床上已经证明它对脑转移患者有益,当然。与奥希替尼相比,临床疗效更差。
2、由转运体/受体介导的大脑
除了开发可以直接穿透血脑屏障的化合物外,研究人员还希望通过脑血管表面的转运蛋白/受体介导药物转运来增加脑组织中的药物浓度。研究发现,脑血管内皮细胞上有多种转运蛋白和受体,如转铁蛋白受体和胰岛素受体。
以往基于提高血脑屏障通透性的药物开发策略并不理想,因此使用血脑屏障内源性转运系统似乎是一种合理的方法,可以在不破坏血脑屏障完整性的情况下调节药物转运。根据类型,内源性血脑屏障转运系统可分为:载体转运、主动转运和受体介导转运。其中,载体转运蛋白和主动转运蛋白系统负责小分子(如葡萄糖、氨基酸、脂肪酸等)在血液和脑组织之间的转运;受体介导的转运系统负责特定内源性大分子跨血脑屏障的转运(如胰岛素、转铁蛋白、低密度脂蛋白等)。
血液系统中的分子可以与 BBB 表面的特定受体结合。结合后,通过受体介导的作用,复合分子通过血管内皮细胞进入大脑。这被认为是最成熟的脑靶向药物递送策略之一,具有高特异性、选择性和亲和力。
3、 mAb 穿透 BBB
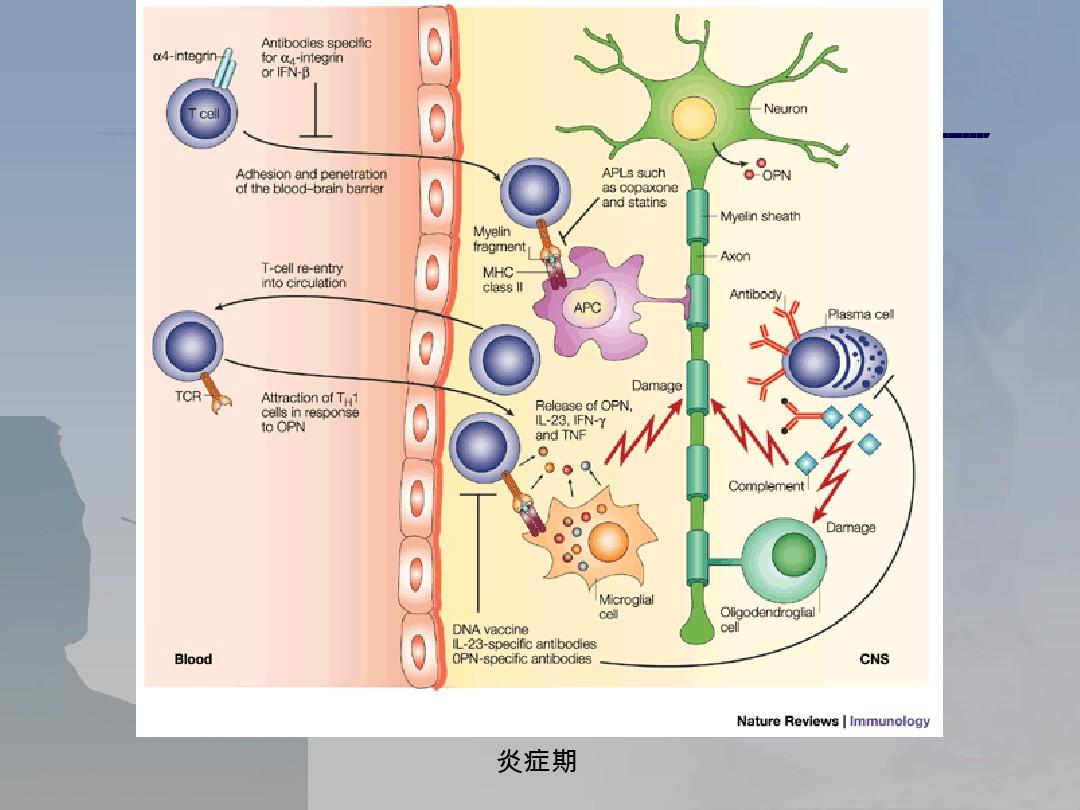
艾伯维德国研发中心主任 Hann 博士曾表示,“只有不到 5% 的小分子药物可以穿透血脑屏障,生物药几乎不可能穿透血脑屏障。” 与小分子化合物相比,单克隆抗体等分子量巨大的药物无法直接通过血脑屏障到达大脑。因此,对于中枢神经系统抗体药物的开发,主要策略是:一是间接发挥药效,如多单克隆抗体。性硬化症(MS)的治疗一般通过抑制外周免疫反应来实现;二是通过BBB上表达的受体的内吞作用,设计双靶抗体(Bi-),即靶向BBB的片段。
近期,单克隆抗体药物治疗AD出现了巨大突破,即抗β-淀粉样蛋白抗体已获得FDA有条件批准上市,但其疗效仍存在较大争议。据报道,不同于其他临床失败的β抗体自然能够穿过血脑屏障进入脑实质,但具体原因不明。高浓度的抗体药物有可能直接破坏血脑屏障的完整性。
4、药物进入预测
中枢神经系统药物的临床需求量巨大,但难点在于中枢神经系统药物的开发非常具有挑战性。需要解决的问题之一是如何在临床前找到一种准确预测中枢神经系统药物作用的方法。目前,我们对准确预测中枢神经系统药物作用的认识还有很多空白,对药物在大脑中的分布也缺乏足够的认识。
未来展望
为了让更多的药物进入人脑发挥更好的疗效,研究人员采用了多种方法来增加药物对血脑屏障的通透性。临床治疗首先采用的方法是血脑屏障破坏法,即向颈内动脉注入高渗糖溶液,通过渗透作用将脑血管内皮细胞中的水分吸出,使其收缩,从而增加血管通透性。 BBB。但这种方法具有侵入性,即使外周血循环中的无毒白蛋白进入脑组织,也会造成严重后果,并因副作用大而逐渐退出公众视野。
受体和载体介导的药物转运的优势在于它可以采用灵活的治疗方案。然而,由于治疗药物能否特异性结合受体和载体,以及受体和载体的数量和转运能力的限制,目前只有少数治疗药物可以通过这种方法递送至脑组织,但这方面的研究也受到了很多关注。
此外,需要强调的是,中枢神经系统疾病的治疗不应局限于药物分子必须通过血脑屏障才能发挥功效的假设。如上所述,许多大分子抗体药物实际上作用于外围靶点。为了间接治疗脑部疾病,我们再举一个可以说是中枢神经领域讨论最多的例子:绿谷药业的抗AD药物“GV-971”,一种来源于海藻的寡糖药物,由于其因由于其高分子量和高极性,理论上不可能穿过血脑屏障到达大脑。因此,在对其疗效机制的研究中,研究人员采取了不同的方法,从肠道微生物的角度对其进行研究,
最后,随着生物技术的蓬勃发展,越来越多的旧机制被发现是错误的或不是唯一的。一个典型的例子是有几十年历史的糖尿病药物二甲双胍,近年来发现了新的适应症。此外,肠道菌群和免疫反应等新兴研究也有望为药物研发开辟新方向。因此,可以说对生物体的探索没有尽头。相信在科研人员的努力下,中枢神经系统疾病的困境将逐渐得到改善。
作为专注于医疗健康产业的投资机构,2018年,固特佳投资获深圳市人力资源和社会保障局批准设立博士后创新实践基地,旨在响应政府号召,吸引来自行业和高校的优秀博士加盟,助力医疗健康与科技金融的深入专项研究与成果转化。同时,国泰君安立足中国,面向世界,借助博士后创新实践基地平台,为中国医疗健康产业的转型发展不断贡献力量。
关于国泰君安投资
2001年,国特嘉投资在深圳成立,专注于医疗健康产业投资,以战略股权投资为主,涵盖并购、PE、VC、天使等各个阶段。拥有国内最大的专业医疗投资团队之一,搭建医疗健康产业投资生态平台,致力于成为具有全球影响力的医疗健康投资机构。
资产管理规模超200亿元,拥有医疗健康产业基金(含美元基金)25只,投资企业150余家(其中医疗健康企业80余家),推动公司成功上市27家公司。
的投资业务立足中国,面向世界。在深圳、上海、北京、南京、香港等地设有运营中心。致力于在全球范围内投资优秀的医疗健康企业,为全球资本和医疗企业嫁接中国力量,助力创业者成就伟大企业。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话