欢迎光临吉康旅!
乳腺癌试验的长期随访提供了对有希望的联合治疗疗效的进一步了解。…
自从奥希替尼被美国食品药品监督管理局(FDA)批准作为最常见的 EGFR 激活疗法的一线治疗药物以来,对 EGFR 突变非小细胞肺癌()的获得性耐药的管理发生了显着变化。在 2020 年 12 月之前,对厄洛替尼、吉非替尼和 α 等一线老一代 EGFR 酪氨酸激酶抑制剂 (TKI) 最常见的耐药性是 EGFR 突变,发生在接受治疗的患者中超过一半早期EGFR-TKI。1 最初被批准作为携带 EGFR 突变的 EGFR 患者的二线治疗,其响应率约为 70%,无进展生存期 (PFS) 约为 10 个月。2 研究表明奥希替尼作为一线治疗的优越性,与厄洛替尼或吉非替尼相比,奥希替尼具有改善的 PFS 和总生存期,现在是 IV 期肺病患者的一线治疗癌症携带者和癌症的事实上的护理标准。3 奥希替尼还于 2020 年 12 月获得 FDA 批准,用于辅助治疗 IB-IIIA 期 EGFR 突变后手术切除和标准辅助化疗——当有指征时——基于研究中使用奥希替尼辅助治疗观察到的无病生存获益.
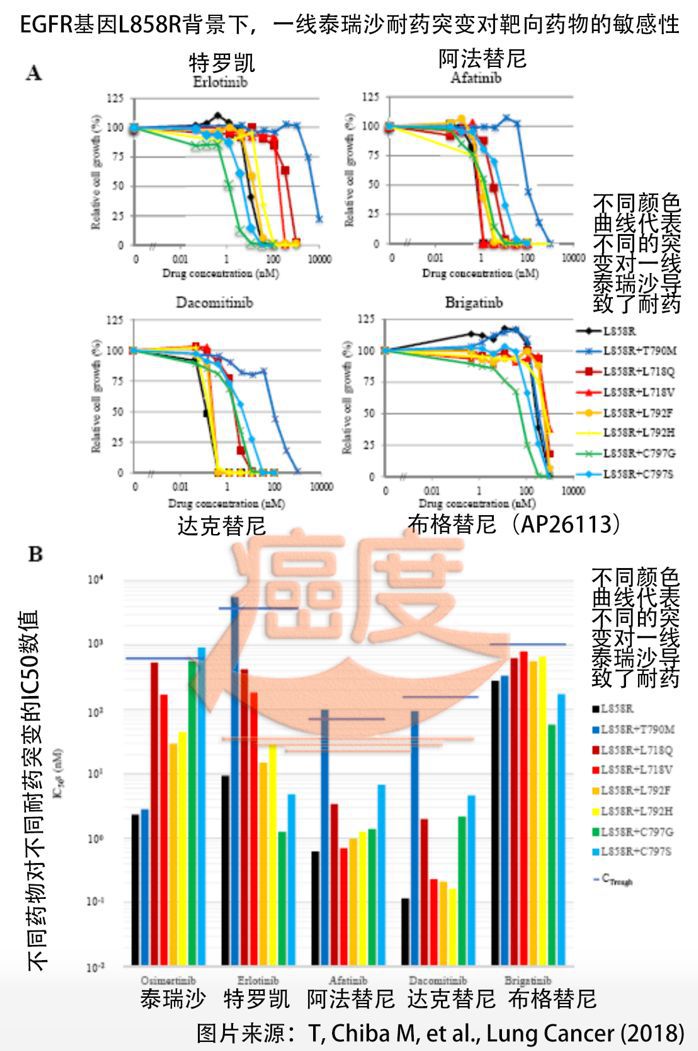
EGFR-被一线奥希替尼完全抑制,与第一代和第二代EGFR-TKI不同,没有机会发展。因此,EGFR突变耐药机制的频率和谱发生了变化。这些抗性机制可分为几大类(例如靶向抗性,例如替代途径,例如 MET 扩增、RAS-RAF-MAPK 改变、RET 融合等)和组织学转化,例如细小细胞和神经内分泌分化。5,6 绕过区域,例如 MET 扩增,最常发生,其次是靶向 EGFR 突变,例如。
目前,没有 FDA 批准的针对这些耐药机制的靶向治疗组合。批准的二线治疗主要包括使用铂类化疗的非靶向治疗,如卡铂和培美曲塞。EGFR突变的患者被排除在-189试验之外,该试验将派姆单抗添加到基于铂的培美曲塞中。PD-L1 抑制剂作为 EGFR 突变的 EGFR 的单一药物通常是无活性的,尽管在化学免疫疗法中添加贝伐单抗的方案(卡铂/紫杉醇/阿特珠单抗)似乎通过抑制血管生成治疗活性和 PD-L1.7 来增强化学免疫性。虽然尚未批准用于 EGFR 突变,但该方案确实在这些患者中显示出稳健的总体缓解率和 PFS,尽管需要在事后亚组分析中在未来的试验中进行验证。
我的方法是首先检查血浆循环肿瘤 DNA,看看是否可以检测到可操作的变化,以便将治疗与临床试验或其他靶向治疗相匹配。一些奥希替尼耐药性改变已被证明在小型案例研究和临床试验中是可行的,例如 RET 与目前批准的 RET 抑制剂和 MET 扩增或外显子 14 跳跃突变剂融合情况下的 MET 抑制。
特别是在 p53 和 Rb1 突变或疾病进展迅速的患者中,我进行组织活检以排除小细胞/神经内分泌转化。p53 和 Rb1 的突变对于神经内分泌转化是必要的,但还不够,但确实提供了一个有价值的信号,表明转化是可能的。10I 用铂/依托泊苷治疗小细胞高级别神经内分泌转化患者。目前尚不清楚在铂类依托泊苷中添加 PD-L1 抗体(例如,或)是否会改善由于对 EGFR-TKI 的获得性耐药而导致的小细胞癌的预后,类似于新发小细胞肺癌。
总之,随着采用奥希替尼作为一线治疗,EGFR-TKI 耐药机制的范围和频率发生了变化。EGFR- 不是用一线奥希替尼开发的,也没有 FDA 批准的靶向治疗。然而,奥希替尼耐药机制似乎是可行的,无论是通过 MET 或 RET 抑制靶向这些旁路,还是通过具有潜在等效靶向突变活性且目前处于临床试验中的新型 EGFR 靶向药物。除了检查血浆循环肿瘤 DNA 中的耐药机制外,重要的是要考虑组织活检以排除小细胞/组织学转化或检测血浆中可能无法检测到的可操作变化。
乐伐替尼治疗不可切除的胸腺癌效果如何?……
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话