欢迎光临吉康旅!
一、中枢神经系统肿瘤分类
2000 年,WHO 对中枢神经系统肿瘤进行了分类。在神经上皮来源的肿瘤中,胶质瘤占所有颅内肿瘤的 40-50%。所谓恶性胶质瘤,包括间变性星形细胞瘤,是侵袭性细胞瘤(III),胶质母细胞瘤是星形细胞瘤(IV)。
间变性星形细胞瘤(AA)是美国最常用的分级方法,具有中等多形性的细胞,具有很强的增殖活性和不同程度的血管增生而没有坏死。在多形性胶质母细胞瘤 (GBM) 中,肿瘤已经坏死。
根据提出的现代组织病理学分级,根据细胞的变性和肿瘤的侵袭性分为1~4级。等级越高,恶性程度越高。间变性星形细胞瘤(AA)是一种浸润性细胞瘤(III),多形性胶质母细胞瘤是一种浸润性细胞瘤(IV),两者都是恶性胶质瘤。
二、恶性胶质瘤的治疗原则
恶性胶质瘤的治疗原则是尽可能切除肿瘤,减轻肿瘤负担,提供病理诊断,以便进行进一步的分子检测,最终指导后期的个体化治疗。术后化疗、放疗、分子靶向治疗等,是最基本的原则。
三、综合治疗
综合治疗包括手术、放疗、化疗和分子靶向治疗。恶性胶质瘤(MG)主要通过手术治疗,可以参考神经外科齐树斌教授的讲座。然而,单独手术后的复发率非常高,中位生存期 (MST) 为 9 至 15 个月。在其他患者中,由于肿瘤的位置不能完全切除肿瘤,手术后肿瘤会复发。因此,综合治疗是当前治疗的主要方法,也是未来治疗的发展趋势。
(一)化疗
化疗可以采用局部化疗,即在手术过程中将药物直接注射到肿瘤内或将聚合物缓释药物植入肿瘤腔内。也可以在肿瘤腔内植入晶片,一种可降解的含 BCNU 的聚合物。还有介入方法,其中化疗药物直接从动脉注射。但仍常用全身静脉化疗或口服化疗。
(TMZ) 是一种口服烷化剂,可穿透血脑屏障,已用于高级别胶质瘤和转移性黑色素瘤。与放疗同时使用可提高缓解率并提高生存率。TMZ口服生物利用度接近100%,可通过血脑屏障,中枢神经系统药物浓度为血浆浓度的40%。在恶性胶质母细胞瘤 (GMB) 的治疗中,联合放疗可提高生存率。与放疗组相比,放疗加TMZ组死亡率降低37%,中位生存时间分别为14.6个月、12.1个月,2年生存率分别为26.5%,10.4%。说明TMZ能显着提高胶质母细胞瘤患者的生存率。
(二)同步放化疗
III-IV级恶性胶质瘤CTv为GTv,周围水肿区放射2.0-3.0cm范围。计划靶区(P1Tv)是CTv加上外照射0.5~1.0cm的范围,主要考虑摆位误差和患者移动的可能性。也可采用6MV X线三维适形放疗,常规分割照射,每次1.8-2.0 Gy,总DT:50-60 Gy/5-6周。对于所有化疗,在放疗的第一天加用替莫唑胺 (TMZ) 75 mg/m2/d。
同步放化疗后,TMZ应单独使用3至6个周期。剂量可为/m2/天或/m2/天,可根据患者不同情况连续口服5天,每28天为一个周期。
(三)PCV 方案
另外,还有一个非常经典的PCV方案,今天还在使用,使用丙卡巴肼加CCNU加VCR,是一种很常用的方法。
(四)亚硝基脲
亚硝基脲在恶性胶质瘤的治疗中是必不可少的。常用的亚硝基脲类包括卡莫司汀、洛莫司汀、司莫司汀、福莫司汀和新的ACNU也称为盐酸尼莫司汀。
盐酸尼莫司汀(ACNU),是通用名,英文名称为:N'-[(4--2--5-)]-N-(2- )-N- 。分子式: ,分子量309.15。下图显示了它的化学结构。
可以通过烷基化细胞内 DNA 来抑制 DNA 合成,从而降低 DNA 的分子量。本品为肿瘤细胞周期非特异性药物,脂溶性强,可通过血脑屏障,血浆中浓度为原药及代谢物的40%。
ACNU单药给药,一般为2~3mg/kg,按每5mg溶于1ml注射用水的比例。然后将溶解的ACNU注入5%葡萄糖注射液中,2~6小时内完成静脉滴注。一般根据患者情况使用4~6个周期。
也可以在第一天和第二天结合ACNU,也是4到6个周期。
(五)尼莫司汀联合替尼泊苷
尼莫司汀联合替尼泊苷的方案,这是一个老方案,治疗效果很好,主要是替尼泊苷(VM)26,静脉滴注,前至三天,然后每4周重复一次,~3mg/kg,静脉滴注点滴,第一天,重复4~6周,4~6个周期。
四、术后辅助治疗
关于术后辅助治疗,在2008年NCCN指南中,AA和GBM恶性胶质瘤都有明确记载,包括BCNU、替莫唑胺等。
五、复发的治疗
复发的治疗方法也很清楚,可以参考指南,这里就不过多解释了。
六、靶向治疗
靶向治疗,即脑肿瘤中EGFR的表达,即表皮生长因子受体EGFR,在多形性胶质母细胞瘤中过度表达,占40%~50%。
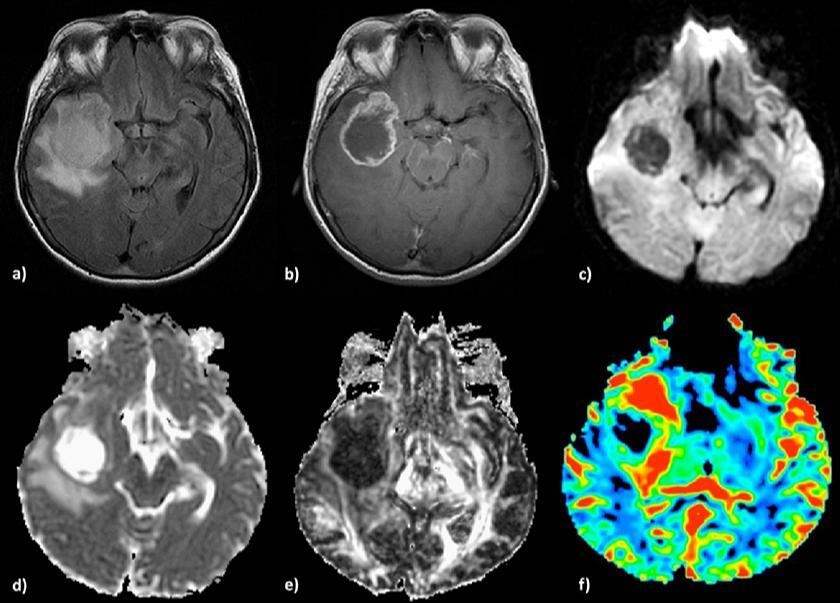
虽然血脑屏障会阻碍大分子单克隆抗体药物向脑病灶的输送,但手术、放射和肿瘤本身都会影响血脑屏障的完整性。因此,可以实现单克隆抗体对脑病灶的递送,药物可以被肿瘤有效吸收。下图是2006年出版的。在影片中间可以看到。免疫影像学检测太心生颅内分布显示,原发肿瘤的放射性活性是选择性蓄积的。
2007 年 ASCO 发表的一项德国研究。尼妥珠单抗治疗儿童胶质瘤,共有 47 名患者入组,儿童和青少年患有难治性和复发性恶性胶质瘤。研究中使用尼妥珠单抗单药治疗/m2/周,持续 6 周,随后进入无进展巩固期/m2,每 3 周 4 次。主要终点是客观的肿瘤反应,次要终点是无病。进展时间,以及主要神经系统症状的安全和缓解。
经过客观疗效分析,中位生存时间为4.4个月。
七、典型案例
一名患有弥漫性内源性脑桥胶质瘤 (DIPG) 的 10.5 岁女性患者。下图显示治疗前(左)和治疗后(右)肿瘤明显缩小。
该研究得出结论,重复使用尼妥珠单抗是安全的,并且患者耐受性良好。尼妥珠单抗对复发性恶性胶质瘤,尤其是脑桥胶质瘤仍然有效。建议启动尼妥珠单抗联合放疗治疗弥漫性内源性脑桥胶质瘤的III期临床试验。
八、尼妥珠单抗联合放疗治疗古巴高级别胶质瘤
该研究招募了 80 例组织学恶性胶质瘤患者,按照 1:1 的比例随机分组。在实验组中,尼妥珠单抗 200 mg 每周 6 周,然后维持治疗 200 mg 每 21 天,直至疾病进展,再加上 50-60 Gy 的放疗。对照组接受安慰剂加放疗 60 Gy,主要结局指标是生存率。
从生存时间分析,多形性胶质母细胞瘤27例。加入尼妥珠单抗后生存期显着延长。间变性星形细胞瘤共入组20例,生存时间也明显延长。
九、抑制剂
VEGF是血管内皮细胞生长因子,贝伐单抗是人源化单克隆抗体,是第一个进入临床的抗血管生成单克隆抗体。贝伐单抗结合并阻止VEGF与其受体结合,从而减少肿瘤中新血管的形成,从而抑制肿瘤细胞的生长。研究表明,贝伐单抗和伊立替康联合治疗胶质母细胞瘤,对近90%的患者有疗效。目前,贝伐单抗联合放化疗治疗恶性胶质瘤的临床研究仍在进行中。
简要描述抑制剂的工作原理?
十、其他治疗的进展
(一)靶向治疗药物
其他靶向治疗药物,如小分子激酶抑制剂,目前也在研究中。单克隆抗体,如尼妥珠单抗、贝伐单抗等,以及其他一些正在研究的单克隆抗体。还有基质金属蛋白酶(MMPs)抑制剂,可以抑制恶性胶质瘤的浸润,脑肿瘤干细胞的研究也在进行中。
(二)放射治疗
目前,一些改进的放射治疗技术也在被使用。一是利用三维适形调强放疗技术有助于增加肿瘤靶区的剂量,有效降低肿瘤周围正常组织的剂量,提高治疗增益比,使增加肿瘤靶区的剂量成为可能。同时局部给药。另一种是利用肿瘤组织和迟发反应组织对改变剂量分割的敏感性差异,缩短治疗时间,提高肿瘤生物剂量,如超分割和加速超分割技术。
然而,尚未证明改进的照射技术可以提高患者的存活率和局部控制率。目前复发性肿瘤的近距离放射治疗大多已被立体定向放射治疗所取代。立体定向放疗通常只适用于肿瘤较小的患者,如肿瘤直径≤3cm。
立体定向放疗适用于( )
A. 肿瘤不能完全切除的患者
B. 多次复发或传播的患者
C. 无法切除肿瘤的患者
D. 肿瘤较小的患者
正确答案:D
分析:立体定向放疗通常只适用于肿瘤较小的患者,如直径≤3cm的肿瘤。
现阶段放射治疗的改进技术有哪些?简述它们的特点。
十个一、总结
在恶性胶质瘤的治疗方面,手术切除程度、患者年龄、KPS评分和病理分化程度是恶性胶质瘤的独立预后因素。治疗原则为综合治疗、最大限度切除肿瘤、术后放化疗、分子靶向治疗。如果肿瘤难以切除,还应采用立体定向活检等方法进行活检以明确诊断,有助于下一步制定更好的个体化放化疗治疗方案。
复发性恶性胶质瘤的治疗原则是尽可能再次手术,术后酌情放化疗。对于多发复发或播散性病变,优先考虑化疗,同时进行对症和支持治疗。其他,包括分子靶向治疗和抗肿瘤血管生成治疗,将是未来治疗研究的方向。
恶性胶质瘤的治疗非常复杂,目前的治疗仍以综合治疗为主。希望通过所有现有的医疗手段,获得更好的治疗效果,改善患者的预后。但是,从理想的角度来看,目前的待遇还远远不能满足人们的期望,未来的发展还有很长的路要走,需要全体同仁的共同努力。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话