欢迎光临吉康旅!
今天分析的这家公司有点奇怪。这是一家尚未盈利的公司。不仅没有盈利,而且这些年经营活动产生的现金流量净额都是负数。2016-2019年1-6月-5672.02万元、-16万元、-75万元、-8942.85万元。
那么这家公司有投资价值吗?看看市场对它们的估值,就很清楚了:
泽晶生物是一家以肿瘤、出血、血液病、肝胆疾病为目标的创新化学和生物制药公司。其最接近商业销售的核心产品是多纳非尼和外用重组人凝血酶。多那非可用于多种实体瘤的靶向治疗。外用重组人凝血酶主要用于外科手术中局部出血的治疗。两者的细分市场分别是抗肿瘤小分子靶向药物和生物药物。
从上述药企的市场估值及其对应的获批药品或临床试验药品数量来看,两者并无直接关系。例如,格瑞药业(-HK)的获批产品数量为3,但其目前市值(2019年6月30日)仅为30.38亿。华医药(-HK)虽然只有一款临床III期药物,但其对应的市值却达到了65.3亿元。
由此可见,创新药企的市场估值取决于其自身上市药品或潜在上市药品的市场容量。另一方面,市场对港股上市的创新药企有有效定价。产生这种怀疑的原因在于,加莱特制药和华医药的日均交易量远低于药明康德等在香港上市的制药相关公司。康德 (-HK)、药明康德 (-HK)。
当然,投资者最终应该明白,泽精生物没有获批上市的药物,但不代表它没有价值,而是泽精生物有投资价值吗?需要进一步观察。
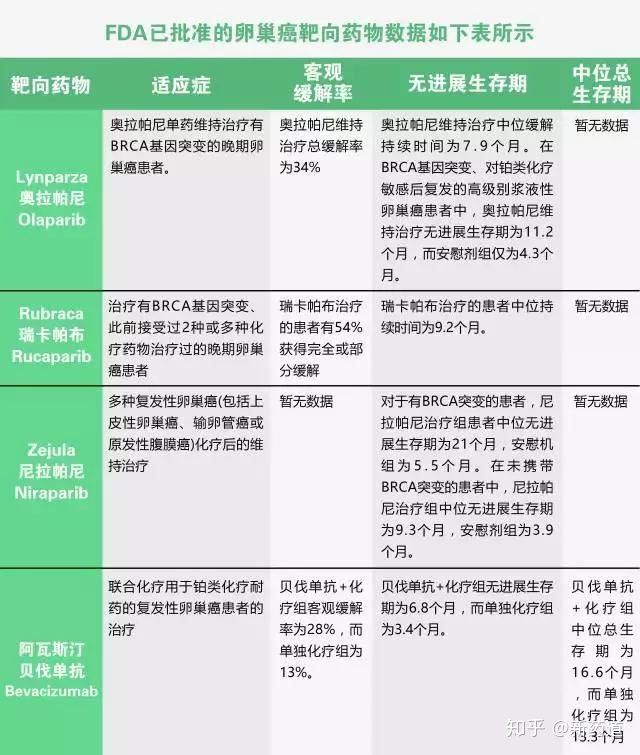
泽晶生物预计于2019年底或2020年初完成多那非用于晚期肝癌的一线III期临床试验,并计划于2020年第一季度提交nda(上市申请);预计2020年完成多纳非尼三线治疗晚期结直肠癌III期临床试验,并提交给nda;多纳非尼预计将于 2021 年完成,用于局部晚期/转移性放射性碘难治性分化型甲状腺癌。
研发风险在于晚期肝细胞异质性高,缺乏治疗肝癌的有效生物标志物,且多数患者在发病时已处于局部晚期肝癌或转移,全身治疗的发展晚期肝癌药物进展缓慢。
该领域包括舒尼替尼、布瑞尼、纳武单抗等小分子靶向药物,以及肿瘤免疫治疗药物,与现有一线标准治疗药物索拉非尼头对头临床研究失败,研发风险相对较大高的。
同时,多纳非尼片用于晚期肝癌一线治疗的III期临床试验进展可能因以总生存期为主要终点而无法达到预期的时间表。如果推迟多纳非尼片上市,泽精生物的利润释放时间点也将推迟。
此外,由于多纳非尼片在治疗直肠癌、甲状腺等方面处于多个适应症同时开发的状态,如果任何一个适应症的临床开发延迟或失败,至少市场水平会有较大的提升。对投资者的心理影响。大的负面影响。
基于初步了解,投资者需慎重考虑泽晶生物的投资。
以上都是负面假设,那么如果泽景生物的多纳非尼片成功进入药品市场,其面临的市场空间和药品竞争条件如何?
目前,全球获批的一线肝癌靶向药物只有德国拜耳的索拉非尼和日本卫材的乐伐替尼两种。索拉非尼()是拜耳公司生产的全球首个肝癌靶向药物。它是目前肝癌一线治疗的标准疗法之一。索拉非尼2007年在美国获批肝癌适应症,2008年在中国获批肝癌适应症。截至2019年6月底,索拉非尼涵盖的适应症包括晚期肝癌的一线治疗,第一晚期肾细胞癌和碘难治性分化型甲状腺癌的一线治疗。一线治疗。
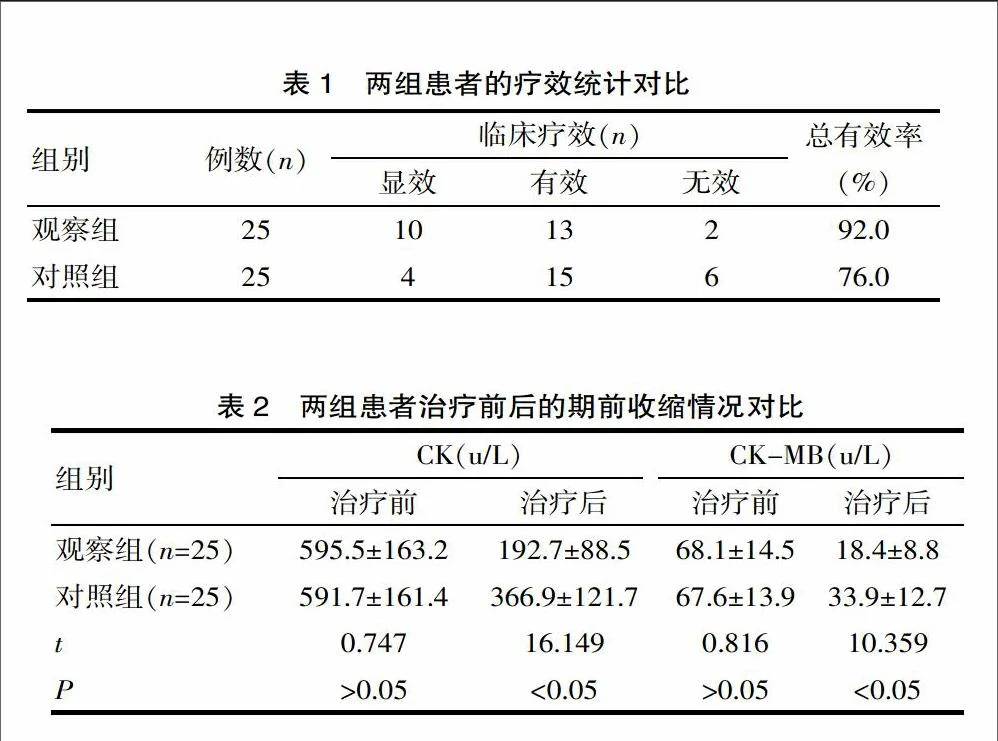
据&报告显示,2018年索拉非尼全球销售额7.12亿美元,其中中国销售收入7.1亿,2018年全球市场份额为87.7%。
复方舒拉非尼中国专利2020年到期,晶型专利2025年到期。截至2019年6月底,石药集团(-HK)、山湘药业、药友药业等7家企业已完成索拉非尼的生物等效性试验。
乐伐替尼()于2015年在美国FDA获批用于甲状腺癌,其非劣效性试验于2018年8月获得成功,并被FDA批准用于肝癌的一线治疗适应症。2018年9月获批肝癌适应症。截至2019年6月底,乐伐替尼在美国涵盖的适应症包括碘难治性分化型甲状腺腺癌的一线治疗、晚期肾癌的一线治疗。癌症,以及晚期肝癌的一线治疗。仅在中国获批用于肝癌的一线治疗。
伦伐替尼于2018年9月在中国上市,2018年第四季度开始销售。2018年中国销售收入达到1亿元人民币,同期全球收入为4.7亿美元,占1 全球市场份额2.3%。
乐伐替尼化合物的中国专利将于2021年到期,晶型专利将于2024年到期。 截至2019年6月底,正大天晴、科伦药业(-CN)等公司已完成或正在实施乐伐替尼生物等效性试验。
根据乐伐替尼的一项全球多中心临床试验研究,乐伐替尼在提高总生存率(OS)方面与索拉非尼相似,而且乐伐替尼在 os 方面并不逊色于索拉非尼。 组的中位 os 为 13.6 个月, 组的中位 os 为 12.3 个月。
除了已经上市的索拉非尼和乐伐替尼外,一些用于晚期肝细胞癌一线治疗的创新靶向疗法也正在临床开发中。非尼布和乐伐替尼仿制药从部分支付能力较低的客户群中分流,也将面临潜在的肝癌一线治疗新药的竞争。

同时,以索拉非尼2018年的全球市场份额计算,全球一线治疗晚期肝癌药物的市场规模约为12亿美元,这对泽京生物来说并不是一个有吸引力的市场。
泽晶生物正在研发的外用重组人凝血酶是一种重组蛋白药物,目前处于治疗外科手术出血止血的III期临床试验阶段。外用重组人凝血酶采用更复杂的基因重组技术,对工艺和产品质量控制要求高,生产成本高,生产失败风险高。
外用重组人凝血酶是新一代局部止血药物,其竞争对手包括蛇毒血凝素、人血源性凝血酶和纤维蛋白粘合剂。由于外用重组人凝血酶的抗出血药物市场较为成熟,其中蛇毒凝血酶和人血/畜血凝血酶已纳入医保,故推测泽靖研发的重组人凝血酶Bio 未来将进入市场,其定价和市场接受度将受到负面影响。
据&报告显示,2018年我国蛇毒血凝素销售额总计57.7亿元,占抗出血药市场份额的79.1%,凝血血来源于人同期血液/畜血酶销售额5.3亿元,纤维蛋白粘合剂(凝血剂)同期销售额10亿元。
与多那非国内市场相比,外用重组人凝血酶国内市场规模更大,但从泽景预期的上市进度来看,他预计2021年提交nda,即利润释放时间。晚于 Dona Fini 利润释放的时间点。
虽然除了多纳非尼和外用重组人凝血酶产品外,泽晶生物还有小分子靶向药物如盐酸杰克替尼、奥卡替尼、、、、、等小分子靶向药物在临床试验中,但由于其预期的应用nda时间较晚,不确定性较大,因此暂时忽略该市场空间的影响。
一般而言,多纳非尼和外用重组人凝血酶之间的竞争格局、市场份额和上市时间具有很大的负面影响。投资者需要更多时间耐心等待更确定的上市时间。,为进一步判断泽晶生物是否具有投资价值。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话