欢迎光临吉康旅!
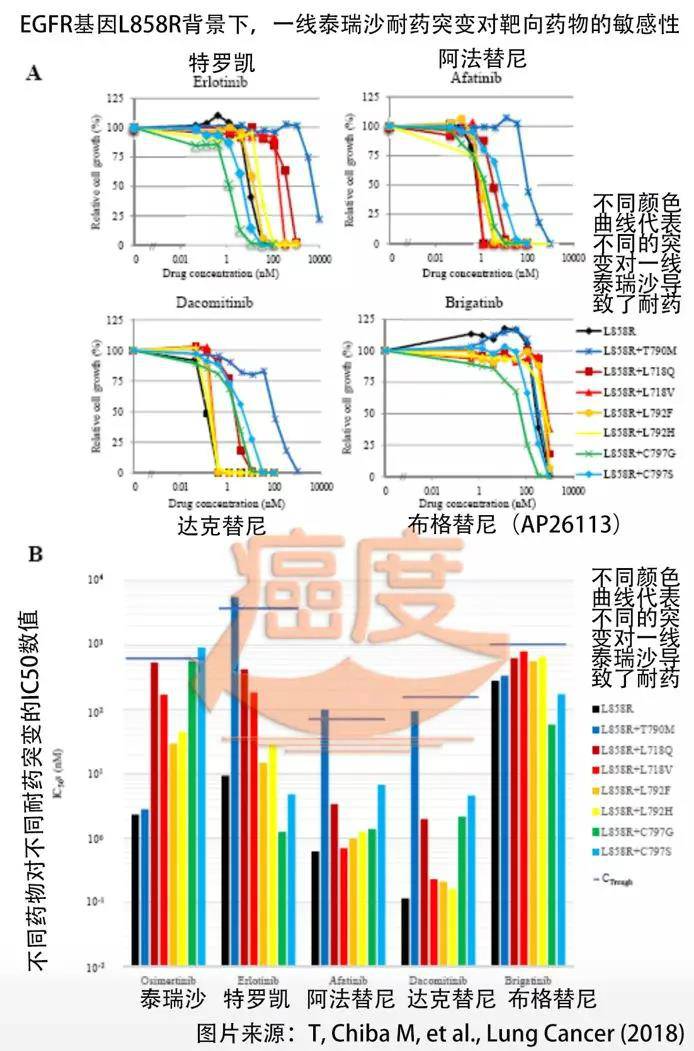
EGFR突变型肺癌是晚期肺癌患者中最幸运的类型。目前开发的第一代、第二代和第三代TKI靶向药物口服治疗可以让患者实现长期、高质量的生存,是目前肿瘤精准治疗的典范。尤其是随着2018年奥希替尼在国内上市,这种生存优势被提升到了一个新的高度。作为EGFR的第三代靶点,奥希替尼(,),作为初始治疗的首选,可达到18.9个月的无进展生存期,为历史最高,目前被广泛应用于肺癌症患者。然而,随着使用者数量的增加,目前奥希替尼的耐药性已成为临床急需解决的问题。但实际上,
失去
在处方正确的药物之前确定奥希替尼耐药的机制
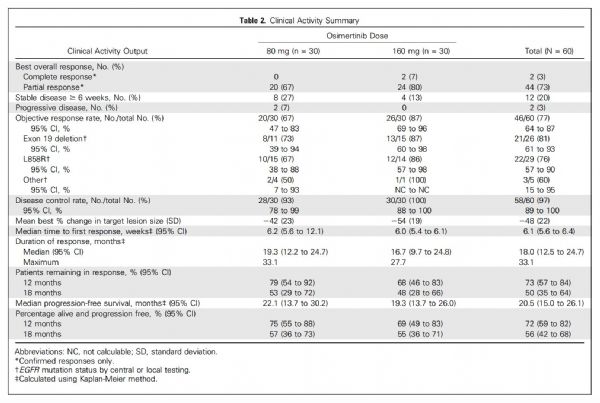
要选择最合适的方案,首先要了解耐药后的突变情况。以下是2018年欧洲肿瘤学会议(ESMO)报告的一线和二线奥希替尼耐药的遗传状态。数据来自和研究。
1. 一线使用奥希替尼耐药后的突变
在 91 名患者中,最常见的耐药机制包括 MET 扩增(15%)和 EGFR 突变(7%)。其余为(7%)、HER2扩增/突变(3%)、-ALK(1%)、BRAF(3%)、KRAS(3%)、细胞周期基因改变等。每个突变可以同时存在。没有发现突变。
2. 二线使用奥希替尼耐药后的突变
73例患者中,最常见的突变为EGFR获得性突变(21%)和MET扩增(19%),其中以EGFR获得性突变为主(15%)。其他包括细胞周期基因改变(12%)、HER2扩增(5%)、(5%)、癌基因融合(4%)和BRAF(3%)等。所有突变都是顺式结构。此外,49% 的患者有缺失。
结果分析:
1. 奥希替尼耐药的原因主要与旁路的激活、下游信号的上调、其他位点的突变以及小细胞肺癌的转化有关。
2. 无论一线还是二线用药,奥希替尼耐药后的突变大多是MET扩增和共突变,后续的治疗方案也主要集中在这两种基因突变的用药上。
3. 突变确实是产生耐药性的主要原因,表明肿瘤细胞在体内的分布发生了变化。
下面详细介绍耐药后的治疗方案。
失去
NCCN 指南推荐奥希替尼耐药的治疗方案
进度也分为类型。在NCCN指南中,进展缓慢或孤立的患者仍可继续使用奥希替尼,同时配合局部治疗。对于多发转移,考虑停止奥希替尼治疗并改用其他全身治疗。
①在以下三种情况下,最新的2019年第二版NCCN指南建议考虑根治性局部治疗(如立体定向放疗或手术),同时继续使用奥希替尼:
无症状进展;有症状的脑转移(配合脑转移,如全脑放疗、培美曲塞、替莫唑胺、鞘内注射等);有症状的全身(颅外)孤立病变。
②对于全身多发病变,指南推荐采用全身治疗(全身化疗)。
③指南中备注阿法替尼联合西妥昔单抗可考虑作为TKI耐药后的治疗。该方案用于第一代和第二代TKI耐药后出现阴性突变的患者,以及奥希替尼耐药后没有可用靶向治疗方案的药物选择。此外,无论PDL1的表达如何,PD1免疫疗法作为EGFR/ALK突变肺癌靶向耐药后的二线治疗效果并不理想。
虽然指南不推荐靶向治疗作为奥希替尼耐药的解决方案,但已有多项研究结果证实靶向药物可用于克服耐药,临床上也常用。因此,小编也列出了数据和案例供参考。
失去
耐药后新突变的靶向药物治疗策略
从奥希替尼耐药的机制来看,虽然并非所有患者在继发基因层面都有明确的耐药原因,但仍有约30%-40%的患者仍能发现基因的继发变化,并继续采用靶向治疗继续有针对性的做法。下面根据目前已知的基因变化对治疗方法进行说明。
1. MET扩增治疗:奥希替尼联合MET靶向药物
从比例上看,MET扩增是奥希替尼耐药最常见的原因,约占20%。因此,对奥希替尼耐药的患者应积极检测MET基因。目前对此的处理方法是比较明确的。它可以通过使用奥希替尼联合 MET 抑制剂来成功克服。有许多相关的成功研究和案例报告。建议您将其作为常规考虑。而且目前MET的靶向药物有很多,比如克唑替尼、卡博替尼()、伏瑞替尼、替波替尼()等,大家可以根据自己的能力选择。列出一些大型研究的结果。
①奥希替尼联合沃利替尼有效率33%。
根据1b期研究的分析,对于之前使用奥希替尼的阳性治疗,耐药后奥希替尼+伏立替尼的客观缓解率(ORR)可以达到33%。联合方案在后线治疗中的疗效仍然相当可观。
②吉非替尼联合用药,控制率高达73%
吴一龙教授团队联合吉非替尼治疗吉非替尼耐药后MET+患者。总缓解率(ORR)为29%,疾病控制率高达73%,中位缓解时间5.6个月。
功效水平与MET扩增程度或MET蛋白表达水平成正比。MET基因扩增GCN≥6组有效率最高,达到47%,中位PFS5.49个月。免疫组化MET蛋白表达3+组ORR为32%,中位PFS达到5.45个月。
虽然本研究中吉非替尼是第一代TKI,但结果也提示EGFR-TKI耐药后的MET阳性患者,与MET靶向药物联合使用可以获得良好的获益。
③病例报告:联合用药成功减焦,但后线治疗仍有效
一名女性患者,44 岁,IV 期肺腺癌,吉非替尼阳性。耐药后改用奥希替尼,19个月后病情进展。基因检测突变,突变和MET扩增阳性,再用克唑替尼联合奥希替尼治疗,肺部病变达到部分缓解(PR),腹膜后淋巴结和右侧肾上腺病变减少90%!同时,疼痛、乏力、水肿等症状得到缓解,身体素质得到改善。三个月后,病灶再次增大。基因检测揭示了 4 个新的 MET 突变(/H,和)。患者改用卡博替尼 + 奥希替尼。一周内症状改善,肺部病变减少。
图A为克唑替尼与奥希替尼治疗前后对比,图B为克唑替尼+奥希替尼治疗前后对比,1个月后缓解,3个月后再次进展,图C为卡唑替尼+奥希替尼治疗前后对比和治疗后。
2. 突变分为顺式和反式结构,两种突变的用药完全不同
奥希替尼耐药的第二大原因是继发耐药突变(主要是类型),发生率约为15%。但在治疗中要注意是单放还是共放,共放是顺式还是反式。对于单次拍摄,可以解决第一代TKI。但是co-比较常见,需要明确区分顺式和反式。当突变和突变位于同一条染色体上时,我们称其为顺式构型(cis);当突变位于相反的染色体上时,称为反式构型()。两种方法的治疗策略完全不同。对于反式突变,治疗方式为第一代EGFR靶向药物联合第三代EGFR靶向药物,并且有很多成功的案例。但是如果是顺式突变的话,上面的方法是不行的,但是目前有一些成功的治疗案例,下面就和大家分享一下。至于如何知道顺反形式,这份基因检测报告会明确告诉你。
①跨结构,一代三代案例
患者,男性,41 岁,患有肺癌纵隔和骨转移,EGFR-(+),服用特罗凯(厄洛替尼)。七个月后 (+)、(+),用奥希替尼控制。12个月后,患者病情加重转化疗控制,后来病情进展转用药物O()。4个周期发生多发转移,化疗无效。检测发现,和反式突变(),患者接受易瑞沙(吉非替尼)联合奥希替尼治疗。症状缓解后不到3天,他就出院了。胸片显示淋巴管炎在 2 周后有所改善。
②顺式结构,布加替尼起关键作用
患者,女,66岁,肺腺癌晚期,口服吉非替尼,病情得到控制。二十个月后,病变开始进展,换用奥希替尼后,肺部病变明显减少。一年后,CT显示肺部病变再次增大,进行基因检测,结果显示:21-、20-和顺式突变(cis)。患者使用奥希替尼联合贝伐珠单抗,肺部病变缩小,症状缓解,3m后进展。患者添加布加替尼以达到 PR。目前患者无明显不良反应,仍维持三药联合治疗。
另一名晚期女性患者,66岁,原发左肺、右肺转移,胸腔和心包积液,多发骨转移,多线治疗,奥希替尼耐药后,肺结节增多,胸水增多,呼吸困难,无法walk,胸水检测发现EGFR Del 19//cis突变,开始试用联合易瑞沙1个月,病情稳定。之后开始布加替尼/天,联合爱必妥(西妥昔单抗)/周,病情明显好转。两个月后,CT复查显示左肺结节和胸腔积液较之前略好,心包积液无变化。,骨转移稳定,但痛苦。
作用机制:(布加替尼)通过与ATP竞争结合EGFR激酶区域起作用,不受位阻或位阻影响。最近的试验表明, 联合 EGFR-TKI 可以克服第三代 TKI 耐药性的出现和顺式突变。
③单突变(无),第一代EGFR靶点药物成功控制
一名 78 岁女性晚期肺腺癌患者,服用阿法替尼,部分缓解(PR),30 个月后耐药。在测试中发现了突变。使用奥希替尼后,7个月后病情进展,基因检测阳性,阳性,无突变。患者基于未发生突变,再次挑战1代吉非替尼(/天),1周后症状缓解,之后CT检查部分缓解。
图A为阿法替尼治疗前后对比,图B为奥希替尼治疗前后对比,图C为吉非替尼治疗前后对比。
总结:突变是奥希替尼耐药的主要机制。没有大规模的临床数据可以证明。只有跨结构治疗方案更加统一,顺式和单突变的临床病例较少。目前,针对靶点的第四代EGFR靶点药物已经处于开发阶段,可期。
3. HER2扩增案例:多西他赛联合曲妥珠单抗
HER2的二次扩增也是具有一定发生率的耐药性原因。这方面的研究数据较少,但也有病例报告。以下是使用 HER2 单克隆抗体曲妥珠单抗 + 多西他赛成功治疗的示例。一名男性患者,54岁,晚期肺腺癌,放疗+含铂化疗9个月后进展,阳性,服用吉非替尼。耐药后发生突变,改用奥希替尼,部分缓解。14个月后,病情进展,出现HER2扩增。给予多西他赛+曲妥珠单抗治疗,病情得到控制。
4. RET :奥希替尼联合BLU-667的案例
一名 60 岁女性晚期非小细胞肺癌突变和阿法替尼耐药患者,积极服用奥希替尼 18 个月,发生 RET 融合。患者接受奥希替尼联合 RET 抑制剂—BLU-667(/天)。2周后,BLU-667增加至/天,肿瘤缩小78%。该程序具有良好的耐受性。
上图为奥希替尼联合BLU-667治疗前后对比。
5. BRAF突变案例:奥希替尼+()
男性,42岁,晚期肺腺癌,EGFR突变,连续使用培美曲塞+顺铂,吉非替尼,厄洛替尼,吉西他滨,疾病进展。发现突变并通过服用奥希替尼实现了部分缓解。经过 13 个月的耐药性,基因检测发现 BRAF 和三重突变呈阳性。患者在一个月后死亡,并没有幸运地服用该药。但从患者胸腔积液的贴壁细胞培养中发现,使用MEK抑制剂()联合奥希替尼治疗可显着降低癌细胞的增殖。
上图显示了附着在细胞培养物上的患者胸水。用BRAF和三重突变治疗癌细胞可以最有效地抑制癌细胞的增殖。
6. KRAS突变
目前尚无奥希替尼耐药后发生KRAS突变的临床试验报告或相关病例。这里以阿法替尼治疗罕见EGFR突变和KRAS突变患者的线后治疗为例,供参考。一名 74 岁男性晚期肺腺癌患者,卡铂 + 贝伐珠单抗 + 、培美曲塞 + 抗血管药物(未知)二线化疗失败。检测发现EGFR-(外显子18)、EGFR-(外显子20)和KRAS突变。患者接受阿法替尼治疗超过 12 个月。
图A显示了癌胚抗原CEA的变化。实线箭头表示患者开始服用阿法替尼,虚线箭头表示阿法替尼的 2 次剂量减少(40 至 30 毫克、30 至 20 毫克)。图 B 和 C 显示了阿法替尼治疗前后的比较。
失去
奥希替尼耐药后的化疗和免疫治疗策略
1. 回归化疗,重新挑战EGFR靶向药物
在没有可用的靶向药物的情况下,奥希替尼耐药的患者理论上应该积极转为化疗。Mok TS研究表明,化疗对治疗阳性患者的有效率为31%,中位PFS(无进展生存期)为4.4个月。除了常规化疗外,研究表明,干预治疗和重新挑战EGFR靶点药物的方法也有一定的临床效果。小编会一一介绍。
①介入治疗:化疗和靶向药物轮换治疗
-2 研究得出结论,在晚期非小细胞肺癌患者的一线治疗中,采用化疗联合厄洛替尼介入治疗可延长无进展生存期,EGFR突变患者获益更显着。另一项前瞻性II期研究发现,27例EGFR靶标药物获得性耐药后,在化疗第1天和化疗第2至16天接受靶标药物治疗。效果较好,有效率25.9%,中位PFS7.0个月。
②化疗后挑战奥希替尼
多项临床研究发现,EGFR靶向药物耐药患者在化疗后再次对靶向药物治疗敏感。以下是一些案例。男性,68岁,肺腺癌骨转移,无症状脑转移,阳性。厄洛替尼耐药后发生突变,患者接受奥希替尼治疗。耐药后,患者改用培美曲塞+顺铂化疗。维持培美曲塞治疗。期间验血为阴性,病情得到控制。在停止化疗 8 个月后,他再次进步。胸腔积液检测为阳性,由阴性转为阳性。患者返回奥希替尼进行长期稳定控制。
图A显示奥希替尼耐药后右肺出现严重胸腔积液,图B显示化疗后胸腔积液控制,图C和D显示停止化疗后疾病进展,图E显示再次使用奥希替尼后病灶明显缩小。
本案中的穿插化疗有可能根除奥希替尼耐药相关癌细胞的增殖,让对EGFR靶向药物治疗敏感的癌细胞重新生长,扭转局面,让患者再次受益于奥希替尼治疗。.
2. 转化小细胞肺癌的治疗:除了结果化疗,奥希替尼的病例轮换治疗也有效
病理类型的转变也是产生耐药性的原因之一,尤其是在某种单一治疗的长期诱导下,患者可以从非小细胞中衍生出一些小细胞病变。这种现象在奥希替尼耐药后也存在。2018年8月,哈佛大学的R.教授对41名接受奥希替尼耐药的患者的组织和血液样本进行了检测,并进行了全面的基因分析。结果显示,6名患者已转化为小细胞肺癌。这类患者的突变都消失了(说明它们独立于小细胞),但通常伴随着TP53、RB1等小细胞中常见的基因突变。对于这一类人群,治疗方案需要结合EP等小细胞肺癌化疗方案。患者组多次遇到此类患者,对症用药效果良好。
这是奥希替尼轮换治疗的一个例子。一名 61 岁女性脑转移晚期肺腺癌患者,阳性,接受吉非替尼、厄洛替尼、卡铂 + 培美曲塞 + 贝伐珠单抗和阿法替尼治疗。4.2 年。患者右侧胸膜转移灶检测出突变(组织为腺癌),但发现右侧膈肌附近的胸膜肿瘤已转化为小细胞肺癌。患者采用奥希替尼和化疗(卡铂+伊立替康)轮换治疗,病灶进展后立即换方案,如下图所示。
上图为患者交替使用奥希替尼和化疗期间两种不同病理类型病变的变化,以及SLX(唾液酸X抗原)和Pro-GRP(小细胞标志物)水平的变化。肺癌)。
3. 免疫疗法:PDL1高表达,吸烟者是受益者
对于EGFR阳性患者,大多数研究表明免疫治疗没有化疗优势。但情况并非绝对如此。研究结果表明,对于PDL1≥25%的患者,EGFR阳性患者≥3线(PDL1单克隆抗体)治疗的有效率(ORR)为12.2%。
此外,意大利()的一项研究表明,对于EGFR阳性治疗的患者,吸烟与不吸烟的有效率分别为20.6% vs 1.9%。两项研究表明,PDL1 高表达和吸烟可能是 EGFR 突变患者免疫治疗有效性的预测因素。
这是免疫疗法的一个例子:
一名亚洲女性患者,69 岁,肺腺癌突变,厄洛替尼在 13 个月后进展,通过积极服用奥希替尼实现了部分缓解(PR)。12 个月后,出现了一个新的病变,带有阳性和顺式突变。PDL1 表示为 70%。患者在卡铂+培美曲塞化疗3个周期后病情进展,随后入组()联合IDO-1抑制剂()治疗组,达到部分缓解。
失去
总结
1.无论是作为一线还是二线治疗,奥希替尼的主要耐药突变包括共突变、MET扩增,其他原因包括KRAS突变、HER2扩增、BRAF突变、小细胞转化等等。因此,耐药后仍应积极开展常规基因检测。
2. NCCN指南建议对奥希替尼耐药且进展缓慢或孤立病灶的患者可继续服用奥希替尼联合局部治疗(放疗或手术),仍应仔细分类耐药迹象。过早停止 9291 治疗。
3.对于继发性耐药突变,以上具体处理方法已经有明确说明。大家可以参考一下实现。
4.不明原因或无靶向药物的患者应转为化疗,化疗后可再次尝试靶向药物。部分患者可以选择免疫治疗。
参考:
1. 等。案例:在一个有肺的
两个 EGFR 和一个 KRAS .Lung .2016.9.
2. 等。对于 EGFR-非 .2018.12.
3. Ho CC, Liao WY, Lin CA, et al. BRAF 一样。J. 2017 年 3 月;12(3):567–572.
4. 等。- 肺
5. 和 EGFR-Lung 与 MET-Site to。
6. Ib/II of () Plus of (EGFR) with EGFR-, MET-Non--Cell Lung。
7. 和 EGFR 非细胞肺
8. of,, and cis-, and: 一例
9. 等。一例肺到 .2018.6
10. J 等人。Cis--EGFR in and in a on: a case and of the .2018.8
11. 等。为 EGFR- 和 EGFR 和 RET 以及 BLU-667 用于 RET .2018.9.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话