欢迎光临吉康旅!
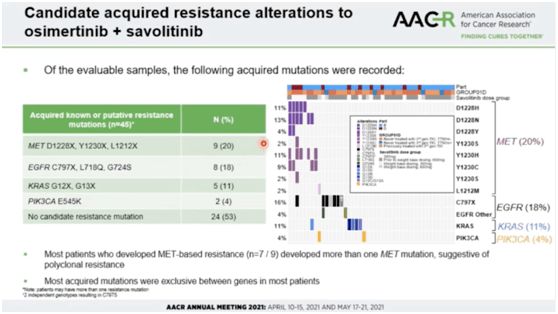
奥希替尼自2017年在中国上市以来,因成功解决了第一代靶向耐药问题,成为众多EGFR阳性晚期肺癌患者的“救命稻草”。同时公布了奥希替尼一线使用的结果。中位无进展生存期 (PFS) 和中位总生存期 (OS) 分别为 18.9 个月和 38.。 6个月,打破靶向药物约一年的中位耐药时间,大大延长了患者的总体生存期,创造了历史上最长的PFS和OS记录。但奥希替尼无法避免耐药,而且耐药后的机制复杂,难以应对。奥希替尼一线耐药后,约15%的患者会出现MET扩增(约5-10%的一、二代耐药)。 MET基因扩增是导致EGFR-TKI耐药的罪魁祸首之一。因此,同时阻断 MET 和 EGFR 靶点成为解决 EGFR 患者耐药,尤其是对奥希替尼耐药的主要解决方案,具有重要价值。今天,我们分享一篇近期发表在《》杂志上的“奥希替尼+沃利替尼治疗EGFR靶向耐药后MET扩增”的研究。
耐药机制-理解
将EGFR-TKI耐药分为4类,包括:①出现耐药突变,如突变; ②旁路激活,如C-MET扩增; ③ 表型改变,如从腺癌转化为小细胞肺癌,上皮细胞转化为间充质细胞(to,EMT); ④下游信号通路的激活,如BIM多态性导致对EGFR-TKI的原发性耐药,并通过扩增直接激活下游增殖信号通路产生EGFR-TKI获得性耐药。
2007年首次提出原癌基因MET扩增是第一代EGFR-TKI的继发耐药机制。 5% 到 20% 的 EGFR-TKI 耐药是由 C-MET 引起的。 MET扩增的耐药机制是MET结合,绕过EGFR激活下游PIK3/AKT介导的信号通路,促进肿瘤细胞增殖,抑制细胞凋亡。 MET扩增可引起EGFR-TKI耐药,但此时EGFR通路仍处于活跃状态。为克服耐药性,可在原有EGFR-TKI基础上联合MET通路抑制剂。
研究方法 本研究为多臂、多中心、开放标签的IB期临床研究;它招募了年龄≥ 18 岁、患有 EGFR 致敏突变/MET 扩增的局部晚期或转移性疾病的患者,这些患者在先前的治疗中取得了进展。共有四个队列,本出版物是两个扩展队列 B 和 D 的初步研究。队列 B 包括 144 名患者,药物治疗剂量为奥希替尼 80mg/d + /d(方案修订后,如果体重不超过 55kg),具体入组人群为: B1:既往接受过第 3 代 EGFR TKI 治疗的患者(69 例) B2:之前未接受过第 3 代 EGFR TKI 治疗且阴性的患者(51例)B3:既往未接受过第三代EGFR TKI阳性患者(18例))队列D包括42名既往未接受过第三代EGFR TKI治疗的阴性患者,药物治疗剂量为奥希替尼80mg/d + 萨沃替尼/d。

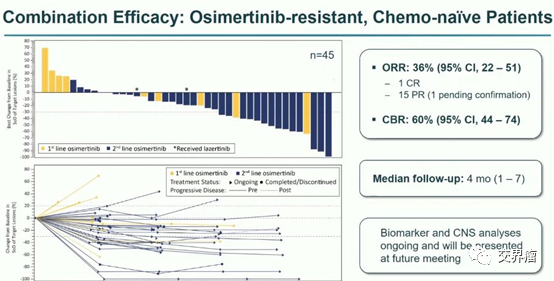
研究结果 B组总人群客观缓解率(ORR)为48%,其中B1为30%,B2为65%,B3为67%;中位无进展生存期 (PFS) 为 7. 6 个月,其中 B1、B2 和 B3 分别为 5.4、9.0、@ >11.0个月;中位反应持续时间 (DOR) 为 9.5 个月,B1、B2 和 B3 分别为 7.9、9.0、@>12.@ >4 个月。总生存期 (OS) 数据不成熟。 D组总人群的客观缓解率(ORR)为64%;中位无进展生存期 (PFS) 为 9.1 个月;中位缓解持续时间 (DOR) 为 8 个月;总生存期 (OS) 数据不成熟。
PFS:B1、B2 组
PFS:B3、D组
队列 B 中的 79 名 (57%) 患者和队列 D 中的 16 名 (38%) 患者发生了安全级别 3 或更高的不良事件。队列 B 中的 115 名 (83%) 患者发生了可能与 相关的不良事件,并且队列 D 中有 25 名(60%)、队列 B 中有 62 名(45%)和队列 D 中有 11 名(26%)患者报告了严重的不良事件。导致死亡的两种不良事件(急性肾功能衰竭和不明原因的死亡)可能与队列 B 的治疗有关。
总结
1.靶向药物耐药后,建议及时进行基因检测,明确耐药原因,指导下一步治疗。
2. MET扩增是EGFR-TKI耐药的主要原因。对于这样的患者,除了化疗几乎没有其他选择。萨沃替尼+奥希替尼为此类患者提供了另一种选择。
3. 沃利替尼+奥希替尼联合方案的副作用较为常见,但不良反应总体可控。希望能给我们带来更多的临床数据,供后续研究参考。
参考文献
DOI:10.1016/-2045(19)-5
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话