欢迎光临吉康旅!
第 41 期新闻 |派姆单抗在中国获批新适应症,乳腺癌双靶点治疗,疗效可翻倍
临床动态
2019年第41期
1、派姆单抗在中国获批用于新适应症
10 月 24 日,默沙东 (MSD) 宣布,中国国家药品监督管理局 (NMPA) 已批准其 PD-1 抑制剂药物 ( ) 用于 NMPA 批准的评估 PD 的测试 - -用于 L1 肿瘤比例评分 (TPS) ≥ 1% 表皮生长因子受体 (EGFR) 基因突变阴性和间变性淋巴瘤激酶 (ALK) 阴性的局部晚期或转移性非小细胞肺癌 () 的单线治疗,并且具有获得 NMPA 论文批准。新适应症的批准是基于3期临床试验-042研究的总生存期(OS)数据,其中包括来自中国亚组和中国扩展队列的数据。
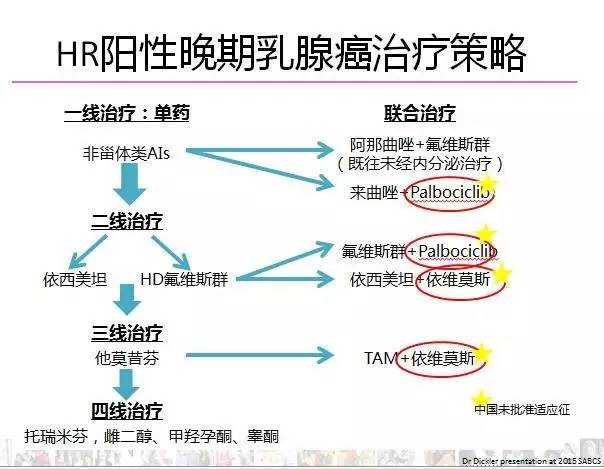
2、乳腺癌双靶点治疗可使疗效翻倍
10月24日,复旦大学附属肿瘤医院乳腺外科邵志民教授团队联合其他23家医疗中心进行的一项研究证实,曲妥珠单抗和帕妥珠单抗这两种靶向药物具有“更强”的“双靶点” “强联合”的新辅助治疗方案,将使HER2阳性易复发转移的乳腺癌新辅助治疗疗效提高近一倍,在乳腺癌“双靶点”领域发出“亚洲声音”方案研究。研究成果在线发表于国际权威期刊《 of the -》(“JAMA”),影响因子为22.4。
3、免疫联合治疗肝癌一线治疗取得突破
10月21日,罗氏()宣布,重磅炸弹PD-L1抑制剂()和VEGF抗体()联合用于治疗不可切除的肝细胞癌,一期达到两个共同主要终点3 HCC 患者的临床试验。与标准疗法索拉非尼相比,无进展生存期 (PFS) 和总生存期 (OS) 具有统计学意义和临床意义的改善。这一进展是肝癌一线治疗的重大突破,也显示出抗血管生成药物与免疫治疗联合应用的广阔前景。
4、乳腺癌治疗达到临床终点
10 月 22 日,公司宣布其 HER 特异性口服小分子酪氨酸激酶抑制剂在局部晚期或转移性 HER2 阳性乳腺癌次要终点患者的一项关键试验中取得了初步和关键意义。公司计划于2020年第一季度向美国FDA提交新药申请(NDA),为口服酪氨酸激酶抑制剂,对HER2具有高选择性,但对EGFR无明显抑制作用,属于人表皮生长因子受体家族。此前,美国FDA已授予治疗乳腺癌脑转移患者的孤儿药资格。
5、PLK抑制剂在KRAS阳性结直肠癌患者中的阳性临床结果
10月23日,公司宣布其在研PLK1抑制剂(PCM-075),与()联用,作为KRAS基因转移性结直肠癌(CRC)治疗的二线疗法)突变)在 1b/2 期临床试验的患者中,初步数据为阳性。在第一次患者分析中,观察到肿瘤 KRAS 突变负荷水平降低。 KRAS突变负荷是一种定量的生物标志物,它反映了肿瘤细胞携带的突变总数,可以预测患者对治疗的反应。它是“-in-”第三代口服高选择性丝氨酸/苏氨酸polo样激酶1(PLK1)。PLK1,Polo样激酶家族成员,在多种实体瘤中高表达和血液系统癌症,如乳腺癌、前列腺癌、卵巢癌、肺癌和直肠癌。
6、 扩大适应症
10 月 24 日,FDA 批准了尼拉帕尼 () 的扩大适应症,用于治疗同源重组缺陷 (HRD) 阳性的晚期卵巢癌、输卵管癌或原发性卵巢癌并接受 3 次或以上化疗的患者腹膜癌患者。 是一种 PARP 抑制剂。 的扩大适应症基于一项多中心、单臂、II 期研究,旨在评估 在四线及以上卵巢癌中的疗效。
7、在加拿大获批用于晚期肾癌的一线治疗
近日,法国制药公司 ( ) 宣布,加拿大卫生部 ( ) 已批准靶向抗癌药 ( ) 20mg、40mg、60mg 片剂用于成人晚期肾细胞癌 (aRCC) 患者的一线治疗。是最常见的肾癌类型。该批准基于研究结果。
8、免疫联合治疗可延长肺癌患者的总生存期
10月23日,百时美施贵宝(-)宣布其关键的3期临床试验-9LA达到了试验的主要终点,为其一线肺癌药物奠定了基础。该试验评估了 PD-1 抑制剂 ( ) 联合低剂量阻滞剂 ( ) 联合两个周期化疗治疗一线晚期非小细胞肺癌 ( ) 的安全性和有效性。在预先指定的中期分析中,与化疗相比,联合治疗在患者治疗中显示出显着的总生存期(OS)获益。
9、治疗胃癌,HER2修饰单克隆抗体疗法启动3期临床试验
10月26日,宣布其免疫增强单克隆抗体候选药物已完成2/3期试验的首例患者给药。旨在评估联合免疫检查点抑制剂联合或不联合化疗作为人表皮生长因子受体 2(HER2) 阳性晚期/转移性胃癌或胃食管癌)潜在一线治疗在交界处患者中的疗效的试验癌症。再鼎医药将协助在中国进行临床试验。
研究新闻
2019年第41期
1、《》:癌细胞消耗营养的方式
十月。 1 月 23 日,由芝加哥大学的研究人员领导的一项新研究回答了为什么癌细胞消耗和使用营养物质的方式与健康人不同,以及这种差异如何促进它们的生存和生长。发表在该杂志上的研究结果指出,乳酸是新陈代谢的最终产物,它改变了称为巨噬细胞的免疫细胞的功能,从而改变了它们的行为。
2、《》:引起乳腺癌转移的激酶
10月23日,医学所的研究人员发现了乳腺癌激酶(BRK)对这对的抑制作用,并确定该通路的激活是导致乳腺癌转移的关键因素,为乳腺癌转移开辟了机会。开发新的乳腺癌治疗方法的潜在途径。研究人员发现BRK和BRK在乳腺癌细胞中反向表达。激活的 BRK 可以通过与 . BRK可以被磷酸化,被磷酸化的进入泛素-蛋白酶体途径降解。他们指出,活化的BRK还可以通过限制性表达下调肿瘤抑制因子Fyn相关激酶(FRK)的表达,从而减少与细胞粘附分子的相互作用,上调EMT标志物和SLUG,最终诱导肿瘤的发生。 EMT,而EMT是乳腺癌转移的前兆。
3、《》:三阴性乳腺癌可以一组确诊
10 月 24 日,博士乔治敦大学伦巴第综合癌症中心的同事们发现,这些表达水平的高低可能部分解释了为什么三阴性乳腺癌的发病率会有所不同。拉丁裔女性的三阴性乳腺癌发病率往往高于白人女性。研究结果于本周发表在该杂志上。研究人员发现,与其他形式的乳腺癌患者相比,三阴性乳腺癌患者的基因拷贝发生了特定的改变,直接影响了 17 的表达。他们还发现,它们中的大多数的表达水平与肿瘤的临床侵袭性相关。
企业新闻
2019年第41期
1、宣布完成7520万美元B轮融资
近日,宣布完成7520万美元的B轮融资。这是一家生物技术公司,致力于通过靶向 DNA 修复和合成致死机制来开发癌症和自身免疫性疾病的创新疗法。公司表示,这笔资金将用于扩大公司的抑制剂和先导化合物 CYT-0851的临床研究,并使用其自己的新型功能获得性合成致死筛选平台确定新的靶点。
2、英国监管机构提议阻止收购
10 月 24 日,英国监管机构提议阻止以 12 亿美元收购该公司,以保持该国和全球测序市场的竞争。 CMA 表示,该机构“初步得出结论”,该公司计划中的收购将“导致英国下一代测序系统市场的竞争大幅减少”。在现阶段,CMA 认为唯一可能有效的结构性补救措施是禁止拟议的合并。除此之外,CMA 还评估了可能缓解其担忧的其他补救措施,包括迫使两家公司剥离或许可相关知识产权。但 CMA 表示将考虑采取多项措施,并要求和公众采取其他补救措施。
3、获得5000万美元融资
近日,宣布获得5000万美元融资。投资方包括20/20、三生制药、、宏辉资本、.、The Mark和永华投资。该公司的专有药物发现平台专注于开发新型巨噬细胞检查点调节剂 (MCM),用于治疗各种疾病,包括癌症、免疫和炎症。
4、扩大KRAS抑制剂布局,诺华再次达成合作
近日,诺华宣布与(6EC)和英国癌症研究中心达成长期合作协议,共同开发用于治疗难治性癌症的新型 KRAS 抑制剂。此次合作是诺华今年第二次合作开发 KRAS 抑制剂。根据协议条款,诺华将为此次合作向 6EC 的 CRT 基金 (CPF) 支付预付款,并为该研究所的 KRAS 抑制剂研发提供资金。诺华将有权获得共同开发药物的独家许可,CPF 基金会还将有权获得潜在的里程碑付款和共同开发药物未来销售的份额。返回搜狐,查看更多
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话