欢迎光临吉康旅!
WCLC最新回顾性研究显示重组人内皮抑素联合卡瑞利珠单抗和化疗的DCR高达100%!
世界肺癌大会 (WCLC) 由国际肺癌研究协会 (WCLC) 组织,是世界上最大的致力于肺癌和其他胸部恶性肿瘤的多学科肿瘤学会议之一。今年的WCLC刚刚落下帷幕,报告了非小细胞肺癌()最前沿的治疗进展。与此同时,我国抗血管生成药物联合免疫治疗的研究进展也备受关注。关注小编,看看最新进展如何!
抗血管生成药物如何帮助患者在免疫时代进一步受益?
以铂类双药化疗为基础的晚期患者传统治疗方案生存率低,副作用明显;靶向药物的出现显着提高了驱动基因阳性的晚期患者的生存率[1],但对于驱动基因阳性的患者,基因阴性的患者并没有明显的益处。改善治疗状态、谋求长期生存是晚期患者最迫切的临床需求。目前,抗血管生成药物的应用已广泛应用于各行各业,国内外多项权威指南和共识都强调了抗血管生成药物对患者治疗的重要性。
免疫疗法的出现从根本上改变了治疗格局。与传统化疗相比,免疫治疗具有疗效持久、治愈率高、毒副作用小、患者生活质量高等优点。疗效有限,并非所有患者都能从免疫治疗中受益,仅约 20% 的受众[2]。如何进一步提高免疫治疗疗效,扩大免疫治疗受益人群成为研究热点。
目前国内批准的抗血管生成药物如贝伐单抗、重组人内皮抑素和小分子抗血管生成药物安罗替尼均作用于血管内皮生长因子(VEGF)通路,可以逆转VEGF的免疫抑制作用,也可使肿瘤血管正常化。另一方面,免疫检查点抑制剂可以恢复免疫支持的微环境,增加效应T细胞的浸润和杀伤功能。并且有利于药物的输送,减少免疫检查点抑制剂的用量,降低不良事件的风险[3,4]。临床前研究证实,免疫治疗与抗血管生成药物联合使用具有协同机制,可发挥1+1>2的强联合作用[5]。
WCLC研究进展:重组人内皮抑素联合免疫治疗DCR达100%
在今年的WCLC会议上,一项抗血管生成药物联合免疫治疗的多中心、回顾性研究表明,重组人内皮抑素联合卡瑞利珠单抗和化疗可达到100%的DCR,显示出令人惊讶的疗效(摘要编号:P4< @0.14).
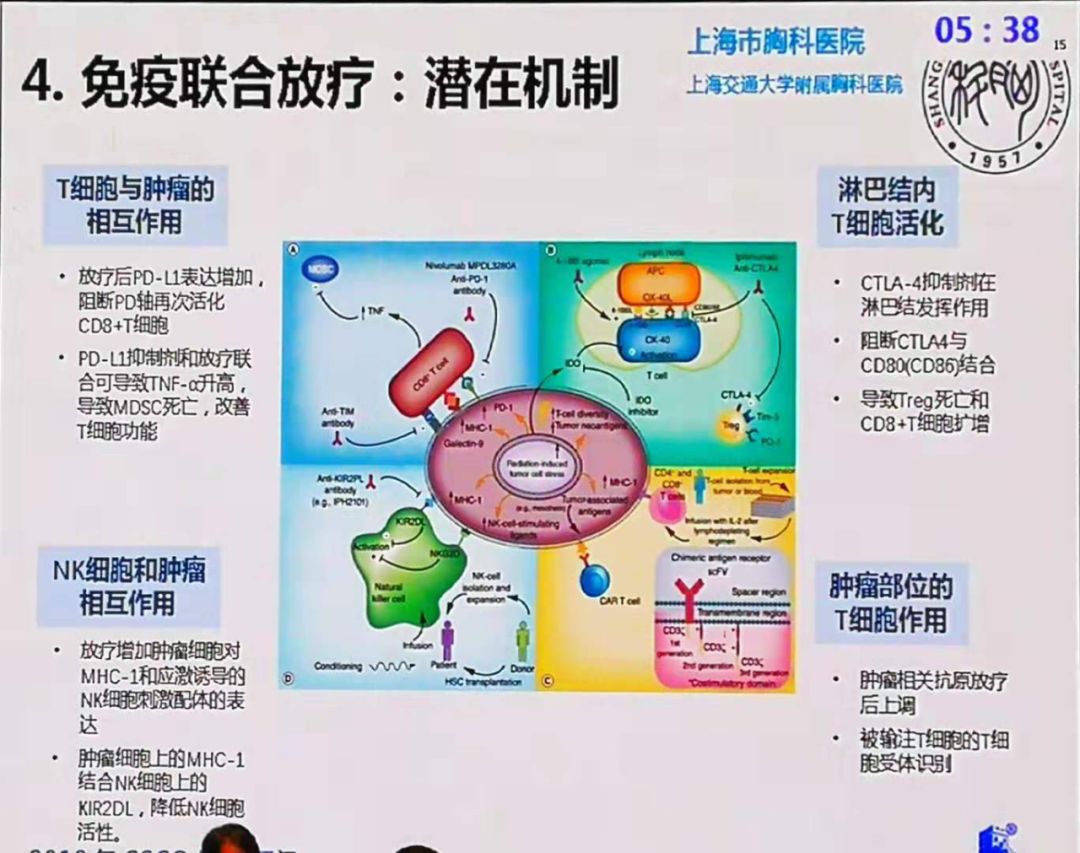
重组人内皮抑素是我国自主研发的抗血管生成药物。基础研究表明,PD-1单克隆抗体联合重组人内皮抑素具有协同作用,可显着抑制肿瘤生长,且效果优于单用PD-1 mAb[5]。
该研究于 2019 年 12 月开始,收集了接受重组人内皮抑素 + 卡瑞利珠单抗和化疗至少两个疗程的晚期患者。截至 2021 年 3 月,共有 21 名患者入组,17 名患者被纳入分析,中位年龄为 55 岁,71% 为男性,90% 为 IV 期诊断,76% 为腺癌,19% 为鳞状细胞癌,67% 接受过一线治疗。
研究结果显示,客观缓解率(ORR)为71%,疾病控制率(DCR)为100%,1例患者达到完全缓解(CR)。 52%(11 名患者)未达到中位无进展生存期 (PFS) 的患者正在接受治疗。
图1.P4<@0.14项研究成果
安全性结果显示,最常见的不良事件 (AE) 是血小板减少症 (24%, ≥ 3 级 10%)、恶心和呕吐 (24%, ≥ 3 级 5%) 和肝损伤 (19%)。一名患者被认为患有免疫相关性肝炎。卡瑞利珠单抗引起的反应性毛细血管增生 ( ) 为 10%,并且在 ≥3 级 AE 中没有。本回顾性研究表明,该联合方案的ORR高于化疗联合免疫,对晚期非小细胞肺癌患者具有良好的疗效和耐受性。
与其他单靶点或多靶点抗血管生成药物不同,重组人内皮抑素是一种泛靶向抗肿瘤血管靶向治疗药物。肿瘤血管生成的多种信号通路包括: 广泛的抑制或调节作用。此外,重组人内皮抑素的重要优点是安全性较好,主要不良反应为血液学毒性,严重不良反应发生率低。
重组人内皮抑素和卡瑞利珠单抗均为国产药物,已获批治疗适应症。本回顾性研究表明,联合方案有望解决目前免疫治疗的瓶颈。
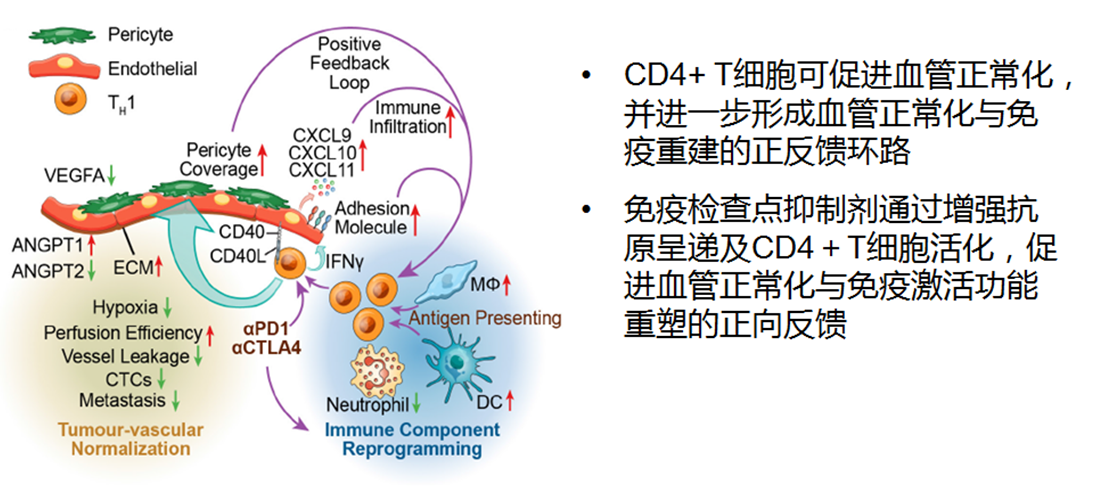
IV期患者的ORR达到58%
今年的 WCLC 还报道了一项回顾性研究,评估了 IV 期非鳞状细胞患者的方案(阿特珠单抗 + 贝伐单抗 + 卡铂 + 紫杉醇)的结果(摘要编号:P16.02),一项研究评估了 2018 年 7 月至 2021 年 4 月期间在澳大利亚 12 个地点接受方案治疗的 54 名非鳞状 IV 期患者,中位随访时间 7.8 个月,15 名 (28%) 患者为一线治疗,11 (20%)患者为二线治疗,28例(52%)为三线及以上。31例(57%)患者报告PD-L1表达水平:65%患者为PD-L1阳性,且其他突变也发生了。 23 名 (43%) 患者有基线肝转移,23 名 (43%) 患者有脑转移,11 名 (43%) 有脑转移。 20%) 患者有软脑膜转移。
在总体人群中,ORR 为 58%,包括 2 个 CR。肝转移患者的 ORR 为 61%,脑转移患者为 57%,软脑膜转移患者为 36%。进展后,15 名 (28%) 患者接受了后续治疗。 PFS 和总生存期 (OS) 分别为 5.1 个月和 8.3 个月。大多数毒性事件为 1-2 级,占 27 例 (49%)。有 25 例 (45%) 3 级、2 例 (4%) 4 级和 1 例 (2%) 5 级治疗相关死亡。
小分子抗血管生成药物联合免疫疗法达到92% DCR
小分子抗血管生成药物阿帕替尼联合卡瑞利珠单抗一线治疗晚期患者的多中心、开放标签研究(摘要编号:MA13.01) A今年WCLC的小型口头报告,该研究招募了EGFR/ALK野生型晚期非鳞状细胞癌患者,旨在探索阿帕替尼联合卡瑞利珠单抗治疗初治晚期患者的疗效,主要研究终点为ORR。 2020 年 12 月 11 日,25 名患者入组,中位随访时间为 15.24 个月(范围:2.0-2<@0.1 7),中位年龄为61 岁。12 名 (48%) 患者在分析时仍在接受治疗,其中 4 名患者在疾病进展后接受治疗。
结果显示,10 名 (40%) 患者达到部分缓解 (PR),13 名 (52%) 患者疾病稳定 (SD),1 名 (4%) 患者疾病进展,1 名 (4%) 未评估. ORR 为 40%,DCR 为 92%。亚组分析显示PD-L1阳性和阴性患者的ORR相似,均为40%(P
未来可期待抗血管生成药物联合免疫治疗
随着医学的发展,肿瘤的治疗选择已经涵盖了传统的放疗和化疗,以及近年来流行的靶向治疗、抗血管治疗和免疫治疗。晚期治疗如何选择治疗方案?抗血管生成联合免疫治疗有1+1>2的效果吗?在今年WCLC报道的几项研究中,抗血管生成药物与免疫疗法的结合确实在该领域交出了令人满意的答案,也证明了两者结合的协同效应。

以重组人内皮抑素为例,作为我国自主研发的抗血管生成药物,在免疫治疗+抗血管生成药物+化疗的“三联疗法”中一直在积极探索。这项单克隆抗体联合化疗的研究显示出令人鼓舞的疗效和安全性,为晚期患者提供了新的治疗选择。此外,重组人内皮抑素+化疗+一线免疫治疗驱动基因阴性晚期非癌性疾病。该鳞状细胞研究更新了陆军军医大学大坪医院肿瘤科在今年中国临床肿瘤学会(CSCO)会议上的初步单中心研究数据。目前,中心共入组患者24例,其中重组人内皮抑素联合PD-1单克隆抗体联合化疗组7例(29%),重组人17例(71%)内皮抑素加化疗组。重组人内皮抑素联合PD-1单克隆抗体联合化疗治疗组中,6例患者接受了至少1次CT疗效评价,4例患者为PR(67%),2例患者为SD(33%)。 4 名 PR 患者的平均收缩率为 64%。研究初步结果提示重组人内皮抑素联合PD-1单克隆抗体加化疗一线治疗驱动基因阴性晚期非鳞状非小细胞肺癌具有缓解率高、疗效显着的特点肿瘤缩小。我们也期待重组人内皮抑素联合免疫治疗和放射治疗的数据收集和临床研究。未来,这种“三联疗法”有望推向一线,让更多患者受益。
未来还有很多探索方向。先前的几项研究表明,抗血管生成治疗与免疫微环境密切相关。然而,并非所有患者都能从免疫治疗中受益,需要更系统的评估方法来确定受益人群。对于驱动基因阳性的患者,抗血管生成药物联合免疫治疗能否成为靶向耐药后的有效治疗方法也值得探索。此外,抗血管生成药物的耐药机制尚不清楚。是否涉及旁路的激活和促血管生成因子的参与,还需要基础研究和临床实践来回答。
参考资料:
[1] 中国医师协会肿瘤医师分会、中国抗癌协会肿瘤临床化疗专业委员会。中国表皮生长因子受体基因敏感突变及间变性淋巴瘤激酶融合基因阳性非小细胞肺癌诊疗指南(2015年版)[J].中国肿瘤学杂志, 2015, 37(10):796-799.
[2]赵莎,姜涛,周才村。抗PD-1/PD-L1免疫治疗疗效预测标志物在非小细胞肺癌中的研究进展[J].肿瘤, 2016, 7: 823-82 8.
[3] 宋雨晓,张碧诚。免疫联合抗血管生成:肿瘤治疗的新策略[J].医学导报, 2020, 8:1068-1072.
[4]齐瑞丽,张永丹,王华清,刘凤亭。免疫检查点抑制剂联合抗血管生成治疗恶性肿瘤的作用机制[J].临床肿瘤学杂志, 2020, 25(7):664 -668.
[5] C、A M C、格雷 J E 等。的和为的[J].的, 2017, 12(2): 194-207.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话