欢迎光临吉康旅!
速读:
2020年1月,“T+A”免疫联合疗法一线治疗晚期不可切除肝细胞癌向国家药品监督管理局提交了生物制品许可申请。 “T+A”联合治疗的客观反应达到25%,是目前治疗方法的2倍以上。联合治疗通常耐受性良好且毒性可控。 “T+A”方案有望成为全球首个获批治疗肝细胞癌的免疫联合治疗方案。
原发性肝癌是全球第五大常见癌症,也是全球死亡率最高的癌症,占全球癌症死亡率的9.1%。根据2016年公布的肝癌流行病学数据,中国是肝细胞癌(HCC)发病率最高的国家,占全球病例总数的55%。
中国 HCC 患者往往被诊断为晚期,约 85% 的患者失去手术机会,总体 5 年生存率仅为 10%。
对于失去手术机会的晚期肝癌患者,介入治疗的缓解期已不能满足其长期生存愿望。肝癌患者迫切需要新的药物和治疗方法。
日前,罗氏在ESMO-ASIA会议上宣布,PD-L1抗体()联合贝伐单抗()用于治疗一期阳性前未接受过全身治疗的不可切除肝细胞癌患者3 次试用。
成为全球首个成功进行肝癌一线治疗的免疫联合治疗III期研究,将为晚期肝癌患者的一线治疗带来新的选择。
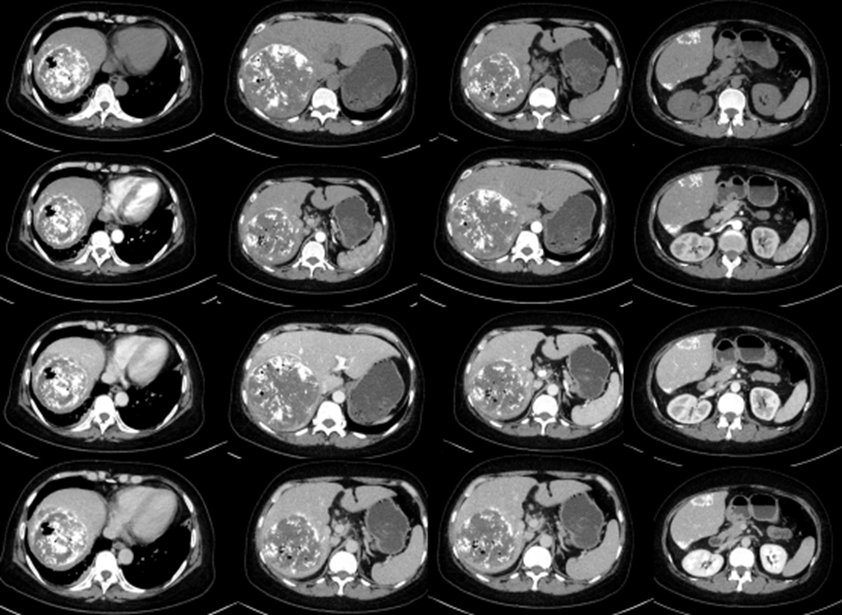
但是,我国肝癌患者的致病因素与HBV感染和饮食中曲霉菌源黄曲霉毒素的接触高度相关,与欧美国家存在较大差异。联合免疫治疗对中国肝癌患者有何影响?患者更关心。
本月初,罗氏在欧洲肝脏研究协会 (EASL) 主办的 2020 年肝癌峰会 ( ) 上公布了 150 项研究的中国队列数据,结果仍然令人惊讶。
免疫联合治疗中国亚组数据公布
本研究共纳入194例中国患者(137例来自全球研究,57例来自中国扩展研究),133例患者按2:1随机分配接受阿特珠单抗联合贝伐单抗治疗耐药,61例患者接受了索拉非尼。
比较中国队列和全球研究的患者数据可以发现,我国肝癌患者的中位年龄更年轻,乙肝病毒感染比例更高。
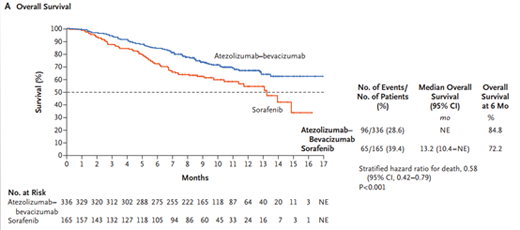
临床获益非常明显
在研究的主要终点总生存期(OS)方面,可以看出阿特珠单抗联合贝伐单抗(“T+A”)作为一线治疗方案的疗效明显优于索拉非尼。中国患者生存期延长,索拉非尼组仅11.4个月,而“T+A”组的中位OS尚未达到。治疗6个月后总生存率分析显示,“T+A”组vs索拉非尼组也有明显改善(87% vs 64%),“T+A”一线治疗也降低了风险死亡人数减少了 56%。 %。
在无进展生存期(PFS)方面,与索拉非尼相比,“T+A”也显着延长(5.7 vs 3.2),6个月效果相同治疗总生存率分析,“T+A”为48%,索拉非尼仅为31%,“T+A”使疾病进展风险降低40%。
对比全球研究数据可以看出,中国队列中OS和PFS的获益与全球趋势和程度基本一致,但在OS和降低死亡风险方面,“T+A”降低中国队列的死亡风险降低了56%,全球研究降低了42%,这似乎给中国患者带来了更大的好处。

在之前发表在ESMO-ASIA上的OS亚组分析中也可以看出,在日本以外的亚洲患者亚组中,“T+A”使死亡风险降低了47%,其受益程度也高于全球数据。
在客观缓解率(ORR)方面,研究的次要终点索拉非尼仅为7%,“T+A”联合治疗的ORR达到25%,翻了一番多,5例患者达到完全解脱。
安全性好,毒性可控
在安全性方面,“T+A”组总体耐受性良好,与全球研究数据基本一致。与索拉非尼组相比,“T+A”组中国患者的治疗相关不良事件发生率更高。 90% 对 93%,但主要是 1-2 级不良事件。 44% 接受“T+A”联合治疗的患者发生 3-4 级不良事件,38% 接受索拉非尼治疗的患者发生 3-4 级不良事件。同时,联合治疗总体耐受性良好,毒性可控,常见不良事件与全球研究基本一致。除阿特珠单抗和贝伐单抗已知的安全事件外,未发现新的安全事件。安全问题。
过去十年左右,只有索拉非尼和乐伐替尼被纳入晚期不可切除肝癌的一线治疗,患者一线治疗选择非常有限。
基于中国队列研究的数据,我们期待“T+A”计划早日获批,让更多患者受益。
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话