欢迎光临吉康旅!
纳米医学的研究可以追溯到1964年脂质体的出现,然后迅速发展。目前市场上的纳米药物主要包括4种类型[2-3]:脂质体、白色蛋白质、聚合物和氧化铁纳米颗粒。阿霉素脂质体(1995 年获批)是美国 FDA 批准的第一种用于治疗癌症的纳米药物。此后,在美国、欧盟和加拿大推出的其他6种脂质体纳米药物包括伊立替康脂质体()、长春新碱脂质体()、米瓦星脂质体()、阿霉素脂质体()等。药物 可显着改善化疗药物在生物体内的药代动力学特性和分布。目前市场上的纳米药物主要包括4种类型[2-3]:脂质体、白色蛋白质、聚合物和氧化铁纳米颗粒。阿霉素脂质体(1995 年获批)是美国 FDA 批准的第一种用于治疗癌症的纳米药物。此后,在美国、欧盟和加拿大推出的其他6种脂质体纳米药物包括伊立替康脂质体()、长春新碱脂质体()、米瓦星脂质体()、阿霉素脂质体()等。药物 可显着改善化疗药物在生物体内的药代动力学特性和分布。目前市场上的纳米药物主要包括4种类型[2-3]:脂质体、白色蛋白质、聚合物和氧化铁纳米颗粒。阿霉素脂质体(1995 年获批)是美国 FDA 批准的第一种用于治疗癌症的纳米药物。此后,在美国、欧盟和加拿大推出的其他6种脂质体纳米药物包括伊立替康脂质体()、长春新碱脂质体()、米瓦星脂质体()、阿霉素脂质体()等。药物 可显着改善化疗药物在生物体内的药代动力学特性和分布。阿霉素脂质体(1995 年获批)是美国 FDA 批准的第一种用于治疗癌症的纳米药物。此后,在美国、欧盟和加拿大推出的其他6种脂质体纳米药物包括伊立替康脂质体()、长春新碱脂质体()、米瓦星脂质体()、阿霉素脂质体()等。药物 可显着改善化疗药物在生物体内的药代动力学特性和分布。阿霉素脂质体(1995 年获批)是美国 FDA 批准的第一种用于治疗癌症的纳米药物。此后,在美国、欧盟和加拿大推出的其他6种脂质体纳米药物包括伊立替康脂质体()、长春新碱脂质体()、米瓦星脂质体()、阿霉素脂质体()等。药物 可显着改善化疗药物在生物体内的药代动力学特性和分布。
白蛋白-紫杉醇()纳米药物是2005年FDA批准的新型抗肿瘤药物,可有效包封疏水性化疗药物,降低纳米药物赋形剂的毒副作用,提高生物相容性。目前市场上的聚合物纳米药物主要有两种:一种是2007年在韩国上市的紫杉醇聚合物胶束纳米药物(-PM),用于治疗乳腺癌和非小细胞肺癌;另一种是在日本上市的新型制瘤素聚合物纳米药物()用于治疗肝癌和肾癌。氧化铁纳米药物()于2010年首次被欧盟批准用于癌症的热疗治疗,是目前抗肿瘤纳米药物的研究热点。此外,有大量纳米药物进入临床试验阶段,主要包括脂质纳米药物(化疗、基因治疗和免疫治疗)、二氧化铪纳米颗粒(放射治疗)、聚乙烯亚胺纳米药物(基因治疗)和胶体金纳米药物(免疫治疗)等。通过靶向纳米药物表面的特定修饰或直接使用具有靶向作用的材料开发的靶向纳米药物。与传统化疗药物相比,靶向纳米药物在肿瘤治疗中显示出极大的优势,如减少对正常组织的损伤、提高治疗效果、逆转肿瘤的多药耐药性等[4]。目前靶向肿瘤的策略主要包括被动靶向、主动靶向和理化靶向三种[5]。
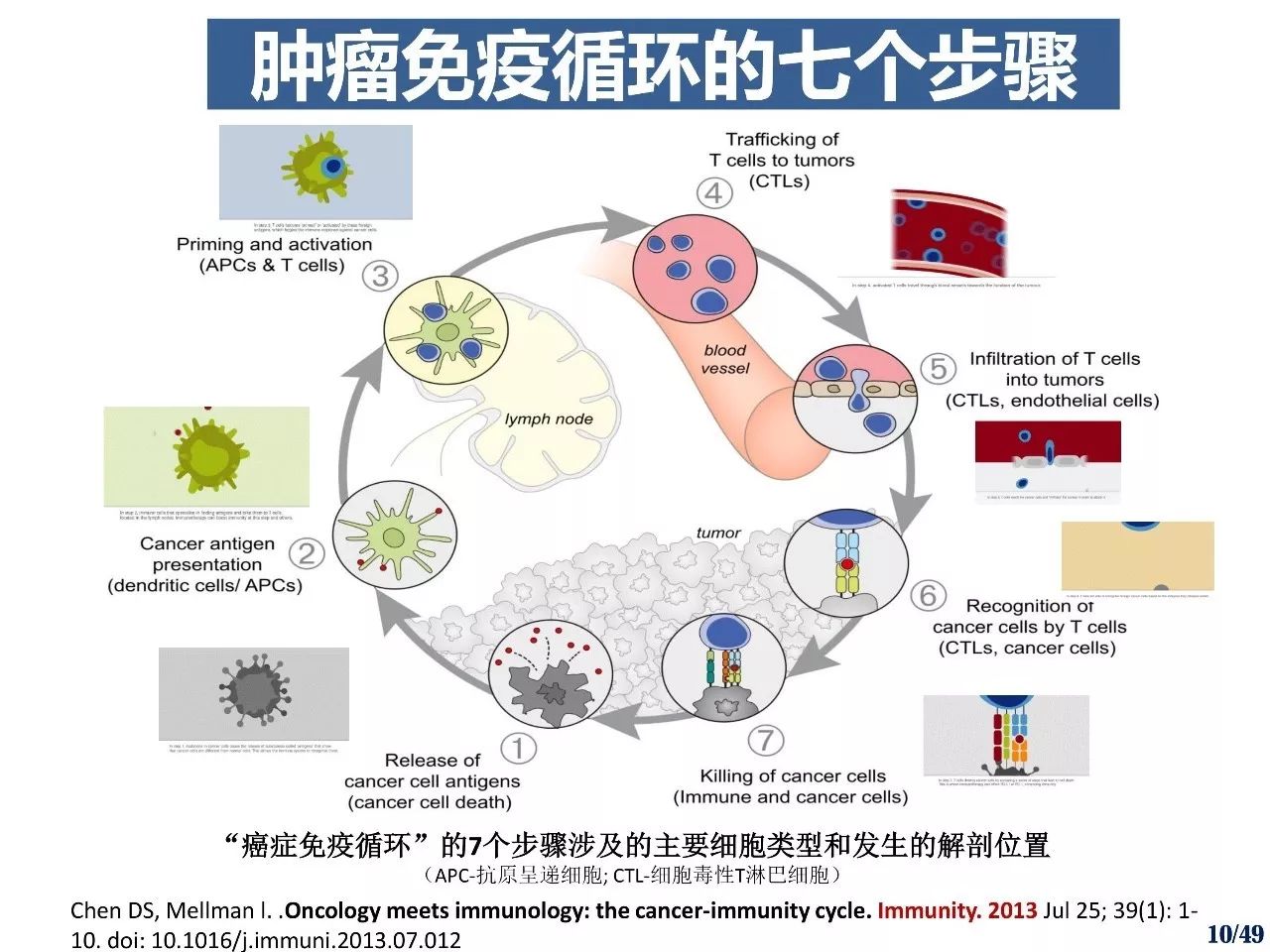
被动靶向主要依靠网状内皮系统或肿瘤部位增强的渗透和滞留效应(和EPR)来实现纳米药物在肿瘤部位的积累。肿瘤部位的异质性和高组织间液压力(,IFP)是纳米药物被动靶向效率低的主要限制因素。主动靶向主要是用特定的配体修饰纳米药物的表面来实现靶向功能。目前,常用的靶向配体主要包括小分子叶酸和碳水化合物,以及大分子肽、蛋白质、抗体、适体和寡核苷酸。主动靶向提高了纳米药物靶向肿瘤的效率,但容易被体内免疫系统清除。如何平衡两者的关系是当前主动靶向研究的重点。理化靶向是利用一定的物理化学方法,使纳米药物特异性聚集在肿瘤部位,释放药物,发挥治疗作用。目前研究的理化因素分为内源性和外源性[6]:内源性因素主要来自肿瘤组织特定的病理生理环境,如pH、氧化还原势能、酶、氧含量、离子强度和剪切力等。 .; 外因主要是物理刺激,如磁、热、光、声、电等。药物渗漏、循环稳定性和治疗效率是此类靶向纳米药物研究的热点。
目前进入临床试验的靶向纳米药物主要以基因治疗和化疗为主。第一个进入临床试验的靶向纳米药物是2008年获批的TfR靶向聚合物纳米粒(-01) 随后,多种基于化疗的脂质体靶向纳米药物迅速出现,其靶向受体为TfR, HER2、PSMA 和 EGFR [2]。虽然近年来抗肿瘤靶向纳米药物发展迅速,但仍存在临床转化率低的问题。市场,瓶颈问题可能主要包括以下几个方面[7-8]:1)靶向纳米药物的结构组成复杂,合成方法一般为多步反应,导致纳米的重现性较差- 药物准备,影响其体内生物学效应;2)靶向纳米药物的体内外生物学评价筛选模型不能完全模拟人体内复杂的肿瘤微环境,导致临床治疗效果低于预期;3)靶向纳米药物往往采用先进的纳米技术,相应的大规模生产设备无法满足纳米药物工业化生产的需要而受到限制;4) 靶向纳米药物的开发多采用一些新材料,其安全性和生物相容性研究数据不足,限制了纳米药物的临床应用;5) 缺乏管理部门 详细明确的纳米药物质量控制和表征指南和标准。2 本期文章的评论和影响。鉴于纳米医学在肿瘤治疗中的重要性,本期《抗肿瘤纳米医学》特别邀请了3位纳米医学专家。在肿瘤治疗药物应用领域颇有研究的知名专家从基础研究、机制探讨、临床转化等多个角度撰写文章。
冯峰教授的《两亲透明质酸衍生物的合成及其在抗肿瘤纳米给药系统中的应用》讨论了两亲透明质酸衍生物的合成方法及其在抗肿瘤纳米给药系统中的应用。讨论了靶向肿瘤的应用和机制。透明质酸具有多个修饰位点,易于合成多样化的两亲性衍生物,扩大了其应用范围。两亲性透明质酸衍生物的应用包括以下三个方面:透明质酸与药物偶联形成前药,自组装形成胶束或核壳结构的纳米颗粒,作为肿瘤靶向配体修饰脂质体。两亲性透明质酸衍生物的肿瘤靶向机制与CD44受体有关。接枝材料的类型、接枝率和表面基团等因素都会显着影响对 CD44 的亲和力。本文对两亲性透明质酸衍生物的设计以及如何平衡各种因素使纳米药物具有良好的载药量和药物释放降解速度,并保持较高的主动靶向作用具有重要启示。. 本文对两亲性透明质酸衍生物的设计以及如何平衡各种因素使纳米药物具有良好的载药量和药物释放降解速度,并保持较高的主动靶向作用具有重要启示。. 本文对两亲性透明质酸衍生物的设计以及如何平衡各种因素使纳米药物具有良好的载药量和药物释放降解速度,并保持较高的主动靶向作用具有重要启示。.
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话