欢迎光临吉康旅!
欧盟委员会(EC)批准贝伐单抗联合特罗凯用于表皮生长因子受体(EGFR)激活突变的不可切除晚期、转移性或复发性非小细胞肺癌成人患者的一线治疗。
ESMO大会公布了贝伐单抗联合或不联合特罗凯治疗中国EGFR突变非小细胞肺癌患者的III期临床数据。共有 311 名患有 EGFR 突变的晚期转移性或复发性非小细胞肺癌患者参加了该试验。所有患者随机分组,接受特罗凯(每次,每天一次)单药治疗或贝伐单抗(每次15 mg/kg,每3周一次)+特罗凯治疗。
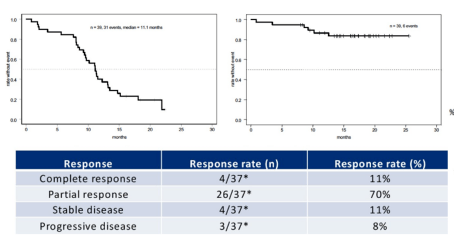
该试验的主要观察终点是独立审查委员会评估的无进展生存期 [PFS (IRC)],次要观察终点是无进展生存期 [PFS (INV)]、客观缓解率 (ORR) ,由研究者评估,疾病反应率 (DCR)、持续反应时间 (DOR)、总生存期 (OS)。两组患者(贝伐单抗+特罗凯VS特罗凯)的人群特征为:中位年龄57岁VS 58岁;男性(38.2% VS 37.7%),女性(61.8% VS 62.3%);所有患者均为肺腺癌;IIIb期患者占2.6% VS 3.9%,IV期患者占89.8% VS 87%,复发患者占7.6% VS 9.1%。EGFR外显子19缺失突变患者占52.2% VS 51.3%,EGFR外显子21突变患者占47.8% VS 48. 7% ; ECOG 分数为 0 (15.9% VS 11%) 或 1 (84.1% VS 89%);基线时脑转移患者占28% VS 30%,基线时无脑转移患者占72% VS 70%。检测结果显示,两组患者(贝伐单抗+特罗凯VS特罗凯)的中位PFS(IRC)为18个月VS 11.3个月。基线无脑转移的患者占72% VS 70%。检测结果显示,两组患者(贝伐单抗+特罗凯VS特罗凯)的中位PFS(IRC)为18个月VS 11.3个月。基线无脑转移的患者占72% VS 70%。检测结果显示,两组患者(贝伐单抗+特罗凯VS特罗凯)的中位PFS(IRC)为18个月VS 11.3个月。
两组患者(贝伐单抗+特罗凯VS特罗凯)的中位PFS(INV)为18个月VS 11.2个月。在EGFR外显子19缺失突变的两组患者(贝伐单抗+特罗凯VS特罗凯)中,中位PFS(IRC)为17.9个月VS 12.5个月,中位PFS(INV) ) 是 18 个月 VS 12.6 个月。在EGFR外显子21突变的两组患者(贝伐单抗+特罗凯VS特罗凯)中,中位PFS(IRC)为19.5个月VS9. 7个月,中位PFS(INV)是 18 个月 VS 9.7 个月。IRC评估的两组患者(贝伐单抗+特罗凯VS特罗凯)ORR为86.3% VS 84.7%,DCR为95. 9% VS 9 6.5%,中位 DOR 为 16.6 个月 VS 11.1 个月。
贝伐珠单抗+特罗凯最常见的不良反应有:皮疹(68.8%)、蛋白尿(59.9%)、高血压(45. 9%)、丙氨酸升高转氨酶(44.6%)、天冬氨酸转氨酶升高(43.9%)、腹泻(39.5%)、血胆红素升高(33.1%) )、贫血 (29.9%)、低白蛋白血症 (28.7%)、低钾血症 (24.8%)。
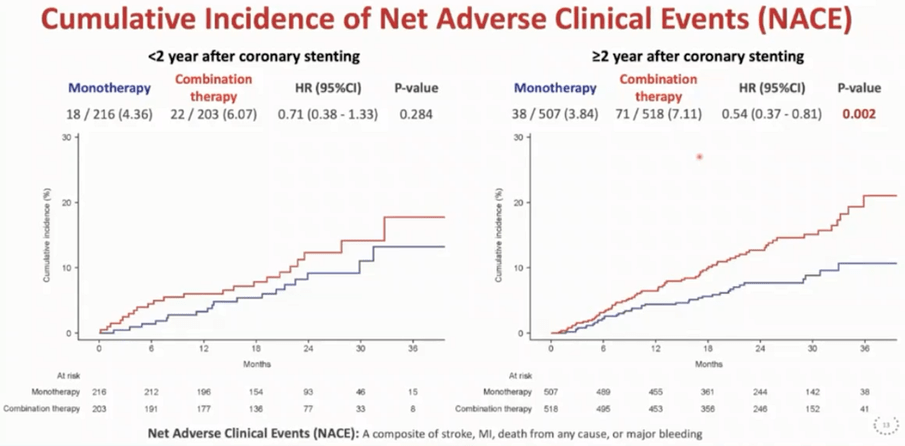
贝伐珠单抗+特罗凯最常见的3级及以上不良反应为:高血压(18.5%)、蛋白尿(8.3%)、皮疹(5.1%) , 丙氨酸转氨酶升高 (2.5%), 腹泻 (2.5%), 天冬氨酸转氨酶升高 (1.9%), 贫血 (1.3%), 低钾血症(1.3%)。
概括:
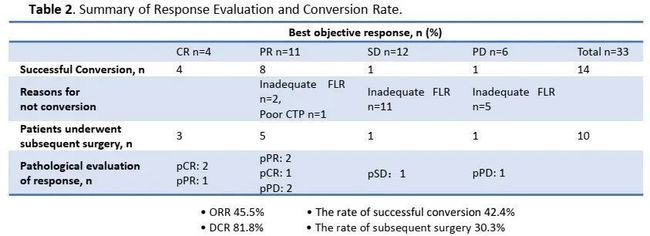
1.本研究表明,贝伐单抗联合特罗凯可显着延长PFS,具有统计学意义和临床意义:中位PFS(IRC)为18个月VS 11.3个月,中位PFS(INV) ) 是 18 个月 vs 11.2 个月。
2. 联合治疗的毒性可控可耐受,未发现新的不良反应。
3.贝伐单抗联合特罗凯有望成为晚期EGFR突变患者的新一线标准治疗。如有需要,请咨询康必星海外医疗顾问:或扫码加下方微信,我们将竭诚为您服务!点击展开阅读:特罗凯/厄洛替尼()或易瑞沙哪个治疗效果更好?
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话