欢迎光临吉康旅!
它与贝伐单抗在难治性 GBM 患者中的最小活性有关。由于缺乏疗效,该研究在第一阶段后提前结束。GBM 中的临床前模型仅使用单个细胞系 (),这是次优的。然而,迄今为止,对于贝伐单抗治疗进展的 GBM 患者,没有任何治疗显示出生存获益。添加贝伐单抗双脱水半乳糖醇(VAL-083),挽救再照射已显示出中等的初始活性,但需要进一步研究以确认其潜在益处。
循环生物标志物数据表明它具有预期的强抗活性。有趣的是,作为缺氧生物标志物的碳酸酐酶 IX (CAIX) 在第 2 天显示出微不足道的增加,但在治疗结束时没有变化。在第 2 天和治疗结束时,多种炎性细胞因子(包括血浆可溶性 IFN-g、TNF-a、IL-6、IL-8 和 IL-10)就是免疫调节。总之,对普那替尼的抵抗可能不是主要与/FGFR抑制后血管变薄引起的缺氧有关——而是与炎症细胞因子的增加有关。事实上,一些临床前数据表明某些免疫细胞因子可能发挥作用在抗血管生成治疗中的作用。
帕纳替尼在贝伐单抗难治性 GBM 中缺乏疗效的另一个可能解释是药物在肿瘤中的不良分布。GBM异位模型(侧腹)与原位(颅内)模型对比表明,每日口服普那替尼(30mg/kg)可有效减少侧腹肿瘤的生长,但不能有效减少颅内肿瘤的生长。生长,这可能是由于颅内肿瘤药物暴露的地区差异所致。事实上,颅内肿瘤浸润边缘的总药物浓度并不总是超过体外细胞毒性浓度(IC50)。关于普那替尼在人体中的血脑屏障渗透的数据有限。
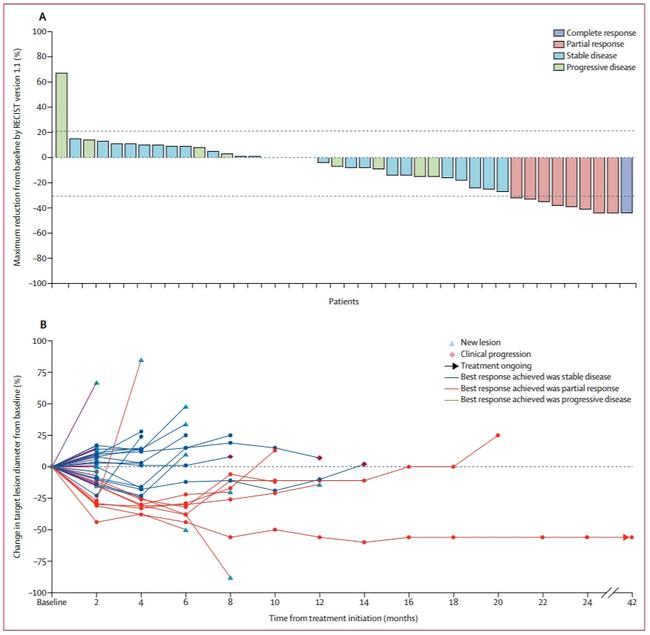
据报道,贝伐单抗停药后出现反弹性肿瘤进展。由于停止贝伐单抗而导致的肿瘤进展反弹是否导致较差的 RR 和 PFS3,以及是否有可能提前终止普纳替尼治疗尚不清楚。研究中最后一剂贝伐单抗与第一次给予普拉那替尼之间的中位时间为 34 天。第一个脑部 MRI 程序发生在普拉那替尼后 28 天,因此肿瘤进展可想而知反弹。然而,研究中患者的较差的中位 OS 表明,无论贝伐单抗停药的潜在反弹效应如何,这些不良结果都可能发生。
除了靶向和 Src 外,它还是一种有效的泛 FGFR 抑制剂。大约 3. 1% 的 GBM 患者具有致癌染色体易位,这些易位将 FGFR 基因的酪氨酸激酶编码域与转化酸性卷曲螺旋 (TACC) 编码域融合在一起。FGFR-TACC 融合蛋白显示出致癌活性,并且使用 FGFR 抑制剂来抑制这种活性已被证明可以延长颅内胶质瘤小鼠的生存期。尽管我们曾希望研究普那替尼在该分子亚组中的作用,但通过测序或阵列比较基因组杂交进行分子检测研究的 12 名患者中,没有人有 FGFR-TACC 融合的证据。

总之,普拉那替尼在对贝伐单抗耐药的 GBM 患者中疗效有限。循环生物标志物数据表明免疫调节可能在治疗抵抗中发挥作用,尽管需要进一步研究来阐明血管生成与这些免疫细胞因子之间的相互作用。目前尚不清楚普纳替尼是否对贝伐单抗初治患者或 FGFR-TACC 融合的 GBM 患者有益,因为本研究未对这两个人群进行检查。鉴于普纳替尼的累积心血管毒性、可能的血脑屏障渗透受限以及选择性脑渗透性 FGFR 抑制剂的近期药物开发,不建议在 FGFR-TACC 融合的 GBM 中进一步评估普纳替尼。详情请扫描二维码咨询:
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话