欢迎光临吉康旅!
() 抑制 PARP 的催化活性,捕获受损的 DNA 并导致 /2 突变细胞中的细胞死亡。我们在这项由两部分组成的 I 期首次人体试验中评估了 () 治疗。在一项开放标签、多中心、剂量递增研究中确定了每日一次的抗肿瘤活性、MTD、药代动力学和药效学。MTD 1.0 mg/天,消除半衰期为 50 小时。治疗相关的不良事件包括疲劳(26/71 名患者;37%)和贫血(25/71 名患者;35%)。3 至 4 级不良事件包括贫血(17/71 名患者;24%)和血小板减少症(13/71 名患者;18%)。在剂量≥0.60mg/天时观察到持续的PARP抑制。在 14 名 (50%) 和 12 (42%) 名 BRCA 突变相关的乳腺癌和卵巢癌患者中观察到 7 名,和胰腺癌和小细胞肺癌 1.0 毫克/天 对确认的反应。 () 显示单药抗肿瘤活性,推荐剂量1.0 mg/day 患者耐受良好。
()是一种有效的口服/2抑制剂,其催化活性与之相当,但相比之下,它在捕获DNA损伤部位的PARP-DNA方面更胜一筹。第一项人体研究表明, () 对具有生殖系有害 BRCA 突变的患者或其具有其他对 PARP 抑制敏感的突变的肿瘤具有单药治疗活性。使用 () 观察到的临床活性表明,靶向 /2 也可能是肿瘤具有其他参与 DNA 修复机制的基因组异常的患者的有效策略。
() 一般耐受性良好。他拉唑帕利()的主要毒性为血液学毒性,伴有一过性和可逆性血细胞减少症(血小板减少症、中性粒细胞减少症和贫血症),主要通过药物中断和/或剂量减少等常规医学干预来控制;输血并不常见。DLT 的所有发作都涉及无出血的短暂血小板减少症。非血液学毒性作用的严重程度是轻微和可控的。相对剂量强度高达97.2%,总体剂量耐受性良好。此外,在本研究的第 1 部分或第 2 部分中,没有患者因毒性而永久退出 治疗。
() 显示出良好的 PK 特性,具有良好的口服生物利用度、快速吸收和总暴露量 (AUC),在很宽的剂量范围内(0.025–1.@ >1 mg/天)与剂量成正比增加。每日给药开始后大约 2 周达到稳态。报告了每日给药的线性尿动力学。在推荐的II期剂量1.0 mg/day,多次给药后的t1/2约为2天;的血浆谷浓度维持在10 nmol/L以上,表明()的全身浓度足以抑制PARP活性。
在药效学(PD)试验中,()在相对较宽的剂量范围内证明了对PBMC的PARP抑制作用。对于0. 6 毫克/天及以上的剂量,所有评估患者的 PARP 活性始终受到抑制。PD 结果表明,在降低的剂量水平下仍然可以实现有效的 PARP 抑制。
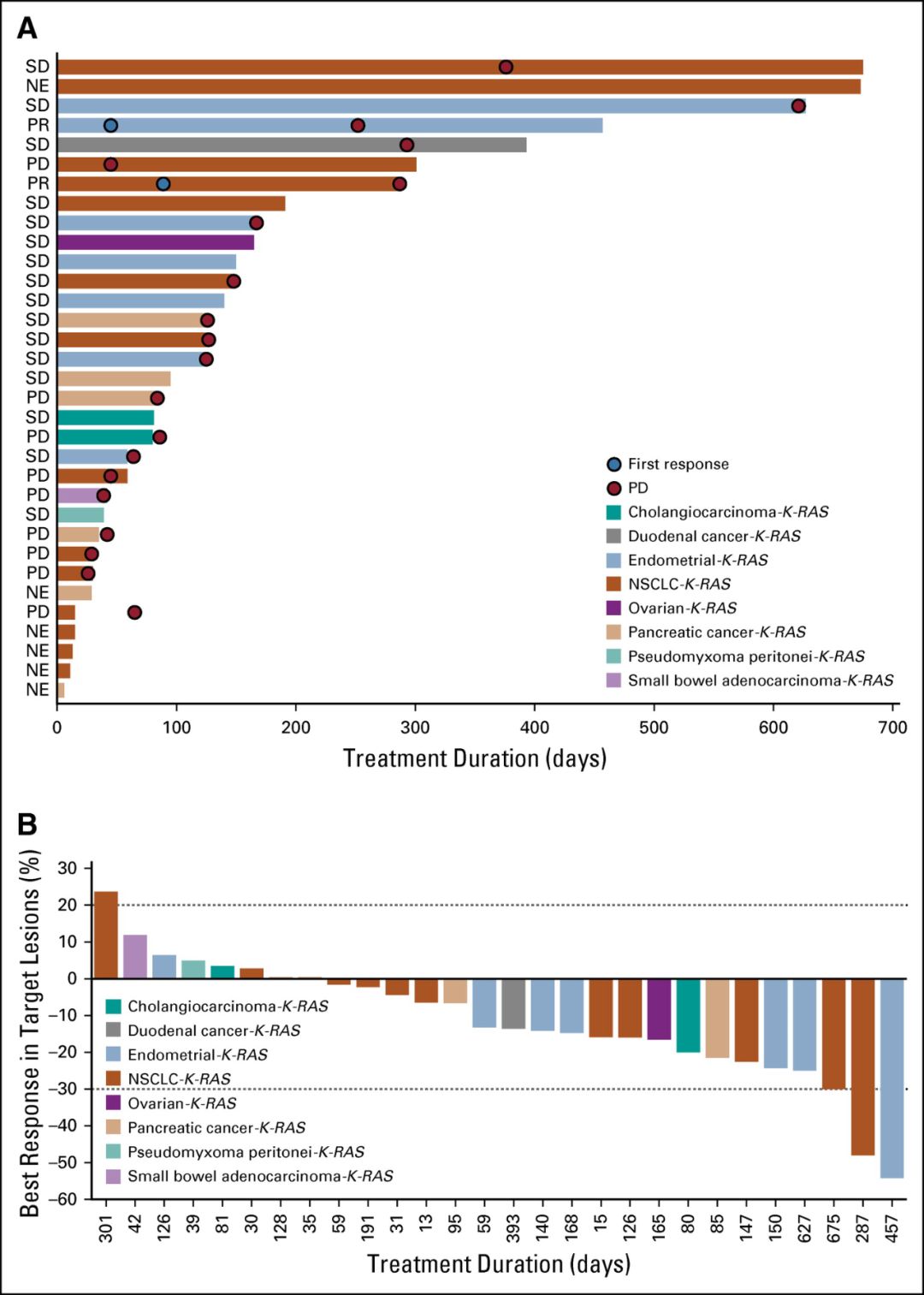
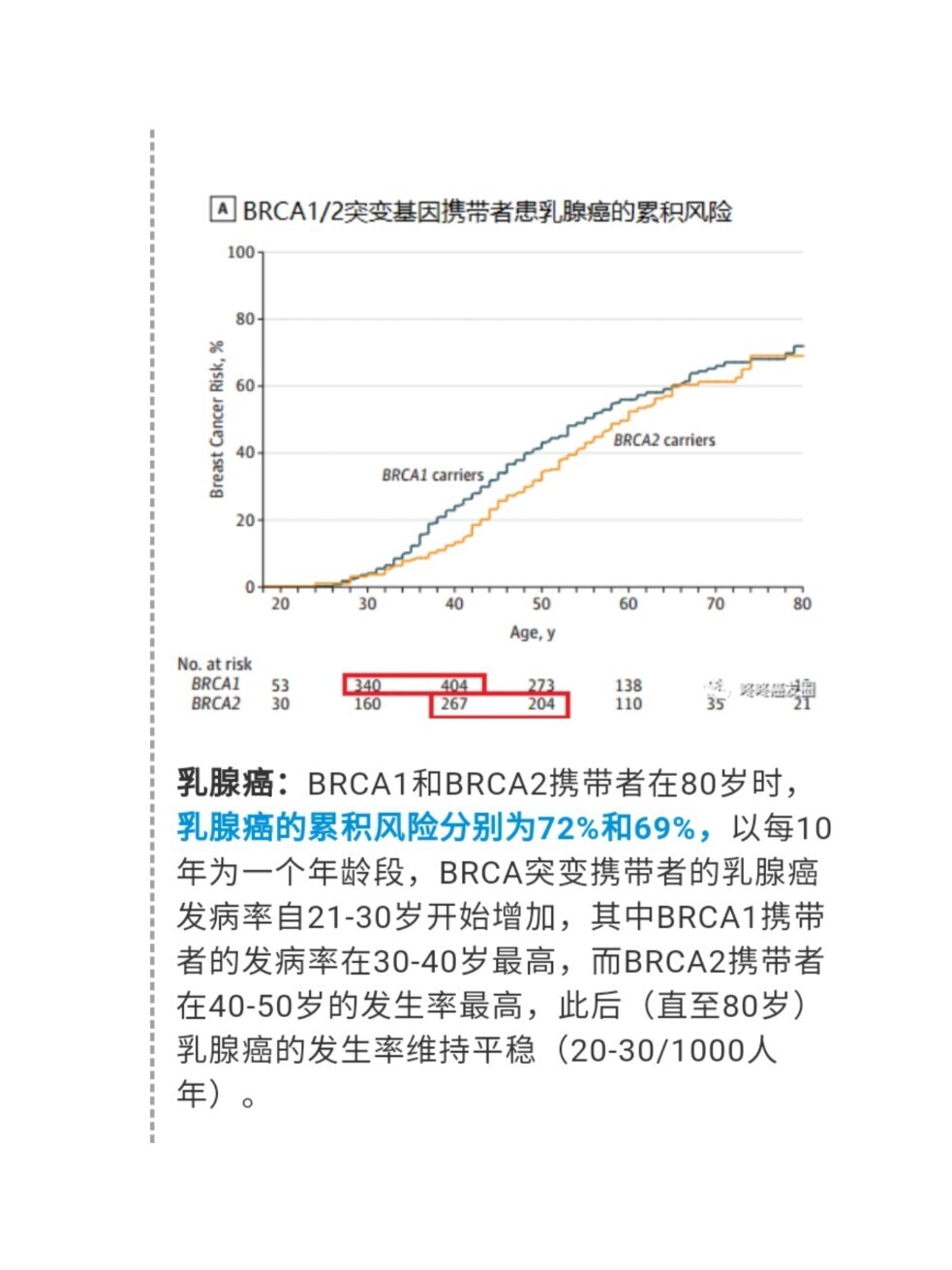
() 在与有害生殖系/2 突变相关的严重预先治疗的乳腺癌和卵巢癌患者中显示出有希望的抗肿瘤活性。晚期乳腺癌患者(包括三阴性患者)的单药活性等于50%(ORR)和86%(CBR)。同样,在接受1.0 mg/day ()治疗的 12 名 BRCA 突变卵巢癌患者中,ORR 和 CBR 分别等于 42% 和 67%。
值得注意的是,有反应的胰腺癌患者携带了突变;由于已知这种突变会被招募到 DNA 断裂中,因此这些发现支持在更广泛的人群中进行测试(而不是单独的 BRCA 突变)。有额外 DNA 修复缺陷的人),这可能会扩大 PARP 抑制剂治疗的应用。
总之,本研究的结果证明了单药 () 在治疗卵巢癌、乳腺癌、小细胞肺癌和胰腺癌中存在和不存在生殖系/2 突变的患者中的有效性。()在许多已接受治疗2年以上的患者中具有可耐受的安全性。他拉唑帕利 () 的 PK 特性支持每日一次给药。该 I 期试验的数据支持 () 在治疗晚期肿瘤(具有 DNA 修复缺陷的遗传性和散发性癌症)患者中的作用。 () 目前正在对多种肿瘤类型进行进一步的临床研究,包括一项针对有害转移性乳腺癌患者的 III 期试验突变/2。扫描下方微信二维码了解更多:
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话